ハイライト
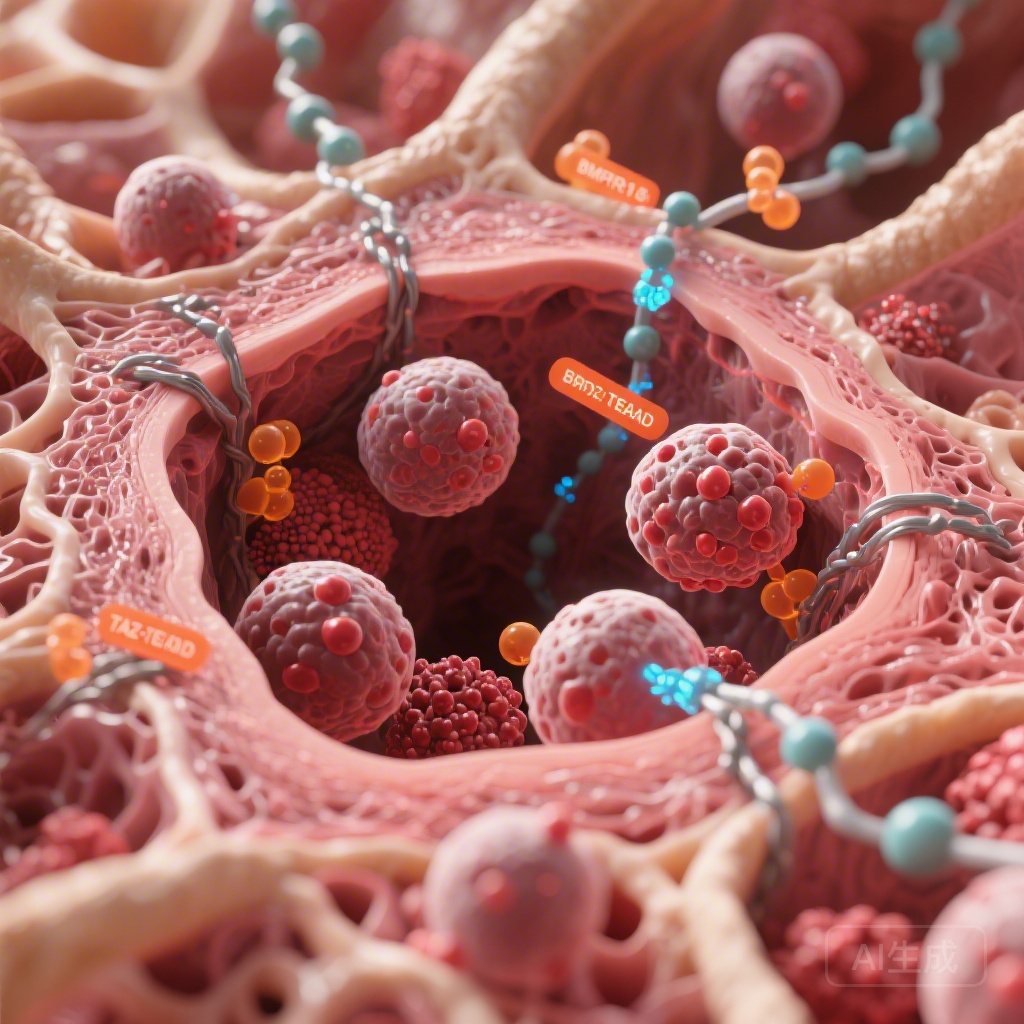
- 再発性AML患者およびシタラビンまたはベネトクラクスに抵抗性の細胞において、BMPR1BおよびTAZ/TEADの発現レベルが有意に上昇しています。
- 細胞外基質の硬化や髄腔圧力の上昇などの骨髄の物理的変化が、白血病の持続を促進します。
- 高閉塞状態にある間葉系幹細胞(MSCs)はBMP4を分泌し、これが特に化学療法抵抗性のAML細胞を活性化します。
- BMPR1BまたはTAZ/TEADの併用阻害とシタラビンの併用投与により、3Dヒト骨髄モデルでのAML一次細胞を効果的に除去できます。
序論: AMLのバイオメカニカルな環境
数十年にわたり、急性骨髄性白血病(AML)の管理は、主に白血病芽球の遺伝子およびエピジェネティックな側面に焦点を当ててきました。FLT3阻害剤やベネトクラクスなどの標的療法の導入にもかかわらず、5年生存率は依然として20%という厳しい数字です。この臨床的な停滞は、化学療法抵抗性の理解が不十分であることを示唆しています。最近の証拠は、骨髄(BM)微小環境が単なる細胞の受容庫ではなく、疾患進行の能動的な物理的参加者であることを示しています。
白血病芽球がクローン増殖すると、骨髄の物理的特性が根本的に変化します。この「バイオメカニカルリモデリング」には、細胞外基質(ECM)の硬化、髄腔圧力の上昇、および宿主細胞が利用できる物理的空间の大幅な減少が含まれます。これらの変化は長年にわたって固形腫瘍で観察されてきましたが、血液悪性腫瘍の生存に果たす役割は最近になって明らかになりつつあります。Barralらの研究(2026年)は、メカノトランスデュクション——細胞が機械的刺激を化学信号に変換する過程——がAMLの化学療法抵抗性の主要な駆動因子であることを特定した重要な突破をもたらしました。
研究設計と方法論的枠組み
研究者は、機械的ストレスがAMLに及ぼす影響を調査するために、多角的なアプローチを採用しました。本研究では、診断時と再発時に採取された一次AMLサンプルや、標準治療薬シタラビン(Ara-C)およびベネトクラクスに対する耐性が特別に設計された細胞株を使用しました。
白血病骨髄の物理的制約をシミュレートするために、チームは3Dヒト骨髄のようなモデルを開発しました。このプラットフォームは、マトリックスの硬さや細胞の閉塞を精密に操作でき、従来の2D培養よりも生理学的に関連性の高い環境を提供します。本研究では、骨形態形成タンパク質(BMP)経路とヒッポ経路のエフェクター、TAZとYAPの2つの主要なメカノトランスデュクション経路に焦点を当てました。トランスクリプトーム解析やタンパク質定量を通じて、著者らはこれらの経路が白血病微小環境の機械的ストレスにどのように反応するかを検討しました。
主要な知見: BMPR1BとTAZ/TEAD軸
抵抗性におけるBMPR1BとTAZの上昇
分析の結果、メカノトランスデュクションシグナル伝達と臨床的アウトカムとの間に著しい相関が見られました。化学療法後に再発した患者では、初期診断時の状態と比較して、BMPR1B(BMPレセプター)とTAZ、ならびにその転写パートナーTEADのレベルが有意に高かったことが明らかになりました。興味深いことに、TAZは上昇していましたが、他の組織で中心的なメカノセンサーとされるYAPは同様の増加を示しませんでした。これは、白血病骨髄の文脈においてTAZが特定の非冗長な役割を果たしていることを示唆しています。
このパターンはin vitroでも確認されました。シタラビンとベネトクラクスに抵抗性のAML細胞株では、TAZ/TEAD複合体が持続的に活性化していました。これらの抵抗性細胞は単に遺伝的に異なるだけでなく、機械的にも異なりました。彼らはフィブロネクチンやラミニンなどの微小環境成分への接着能力が向上し、内在的な変形性が向上していたため、過密化した骨髄内の高圧力、狭い空間を移動し、生存することができました。
パラクラインシグナル伝達: MSCとの関連
本研究は、白血病細胞と常在間葉系幹細胞(MSCs)との間の重要なクロストークを強調しました。白血球で満たされた髄腔を模倣する高物理閉塞条件では、MSCsがBMP4の発現レベルが上昇することがわかりました。このMSC由来のBMP4は、化学療法抵抗性のAML細胞表面のBMPR1Bを特異的に活性化するパラクラインシグナルとして作用しました。この相互作用は、疾患の物理的ストレスが化学療法誘発アポトーシスから芽球を保護する「ニッチ効果」を作り出すようです。
メカノミクスを標的化して芽球を感作する
おそらく最も臨床的に重要な知見は、薬理学的阻害の効果でした。3Dヒト骨髄モデルを用いて、研究者はBMPR1BまたはTAZ/TEAD複合体のいずれかを標的化することで、抵抗性のサイクルを打破できることを示しました。これらのメカノトランスデュクション阻害剤をシタラビンと組み合わせると、AML一次細胞の持続性がシナジー的に低下しました。細胞が硬化し、高圧力の環境を感知し、反応する能力を遮断することで、治療は従来の細胞毒性療法に対して再び脆弱な白血病細胞を「剥き出し」にしました。
専門家のコメント: 機序の洞察と臨床的意義
Barralらの知見は、難治性AMLに対するアプローチのパラダイムシフトを表しています。従来、私たちは骨髄を液体コンパートメントとして捉えていましたが、この研究はそれを固形腫瘍微小環境のように扱うことを余儀なくされます。物理的力が細胞の運命を支配するという観点からです。
TAZがYAPより具体的に関与していることは、特に興味深い生物学的なニュアンスです。多くの上皮癌では、YAPとTAZはしばしば共に活性化されますが、白血病微小環境は細胞に固有の機械的要件を課し、TAZ-TEAD転写プログラムを好む可能性があります。この特異性は、薬物開発におけるより狭く、そしておそらくより効果的な治療窓を提供します。
しかし、考慮すべき制限もあります。3D骨髄モデルは大きな前進ですが、免疫系の役割を含む人間患者の全身的な複雑さを完全に再現することはできません。さらに、AMLの髄腔圧力は動的であり、誘導療法や強化療法の各段階でのこれらの経路の変動を理解することは、メカノトランスデュクション標的治療介入のタイミングにとって重要です。
健康政策と臨床試験の観点からは、これらの結果は、AMLのリスク分類にバイオメカニカルマーカー——高度な画像診断や専門的な生検分析を通じて——を組み込むべきことを示唆しています。特に硬いまたは高圧力の骨髄を呈する患者は、BMPR1BまたはTAZ阻害剤による早期介入の最良の候補となるでしょう。
結論: AML治療の新たな柱
BMPR1BとTAZ/TEADが化学療法抵抗性のメディエーターであることが特定されたことで、血液腫瘍学の新時代が開かれました。白血病骨髄の物理的現実に対処することで、長年にわたってAML治療を悩ませてきた環境依存的な薬物抵抗性を克服することができるかもしれません。従来の細胞分裂抑制薬とメカノトランスデュクション阻害剤を組み合わせた将来の治療戦略は、現在選択肢の少ない患者にとって、より深い寛解と低い再発率を約束します。2026年以降に向けて、生物物理学の臨床腫瘍学への統合は、個別化医療の基盤となることでしょう。
参考文献
- Barral L, Lespinasse N, Martin Cardozo C, et al. Targeting BMP and TAZ/TEAD mechanotransduction pathways impairs acute myeloid leukemia chemoresistance. Leukemia. 2026-03-18. PMID: 41851473.
- Lampi MC, Reinhart-King CA. Targeting extracellular matrix stiffness to attenuate disease progression. Sci Transl Med. 2018;10(422).
- Passaro D, et al. Increased Bone Marrow Pressure Drives Hematopoietic Stem Cell Loss and Myeloid Neoplasia. Cell Stem Cell. 2021.
- Dupont S, et al. Role of YAP/TAZ in mechanotransduction. Nature. 2011;474(7350):179-183.