ハイライト
MGMT未メチル化新規診断の膠腫に対する二重免疫チェックポイント遮断(イピリムマブとニボルマブ)は、標準的なテモゾロミド化学療法と比較して無増悪生存期間を改善しなかった。第II相試験は主要エンドポイントを達成せず、早期終了となり、第III相に進行しなかった。安全性プロファイルは既知の効果と一致し、新たな有害事象信号は見られなかった。
分子関連研究や持続的な生存追跡調査により、この治療が難しいサブグループに対する将来の治療戦略が示される可能性がある。
研究背景と疾患負荷
膠腫(GBM)は、成人で最も一般的かつ侵襲性の高い原発性脳悪性腫瘍であり、多様な治療にもかかわらず予後が不良である。現在の標準治療は、最大限の安全な手術切除に続いて、放射線療法とテモゾロミド(TMZ)化学療法の併用が行われる。しかし、O6-メチルグアニン-DNA-メチルトランスフェラーゼ(MGMT)プロモーターが未メチル化(’uMGMT’)である患者は、内在性の抵抗性によりTMZから著しく少ない利益を得るため、このサブグループは特に短い無増悪生存期間(PFS)と全生存期間(OS)を持つ。これは、新しい治療法に対する重要な未充足の需要を示している。
CTLA-4(イピリムマブ)とPD-1(ニボルマブ)を標的とする免疫チェックポイント阻害剤は、いくつかの悪性腫瘍の治療パラダイムを変革したが、膠腫に対する明確な利益はまだ示されていない。前期第I相研究、特にNRG Oncology BN002試験では、新規診断のGBMに対するイピリムマブとニボルマブの併用の安全性が確立され、潜在的な有効性の兆候が示された。この理由から、uMGMT GBM集団を対象としたNRG Oncology BN007ランダム化第II/III相試験が設計され、二重免疫チェックポイント遮断が標準的なTMZよりも成績を改善できるかどうかを検討した。
研究デザイン
NRG Oncology BN007は、新規診断のMGMT未メチル化膠腫を有する成人を対象としたランダム化、対照、オープンラベルの第II/III相臨床試験である。対象となる患者は、カーノフスキー機能状態(KPS)≥70で、最大限の安全な切除を受けた。
参加者は1:1の割合で、放射線療法と免疫療法(イピリムマブとニボルマブ)または標準的なテモゾロミド化学療法のいずれかを受けるよう無作為に割り付けられた。層別化要因には、再帰的分割解析(RPA)クラス(III、IV、V)と腫瘍治療フィールドの使用計画が含まれた。
主なプロトコル特徴には、免疫抑制を最小限に抑えるために免疫療法開始時のコルチコステロイドの使用禁止、診断、バイオマーカー状態(MGMTメチル化)、およびPFSイベントの中央確認が含まれた。第II相の主要エンドポイントは無増悪生存期間(PFS)で、95%の検出力でHR≤0.58(免疫療法が優れている)を一側検定で0.15の有意水準で検出できるように試験が設計されていた。第II相PFSの成功は、第III相全体生存期間(OS)分析への継続をトリガーする予定だった。
 Afte
Afte
主要な知見
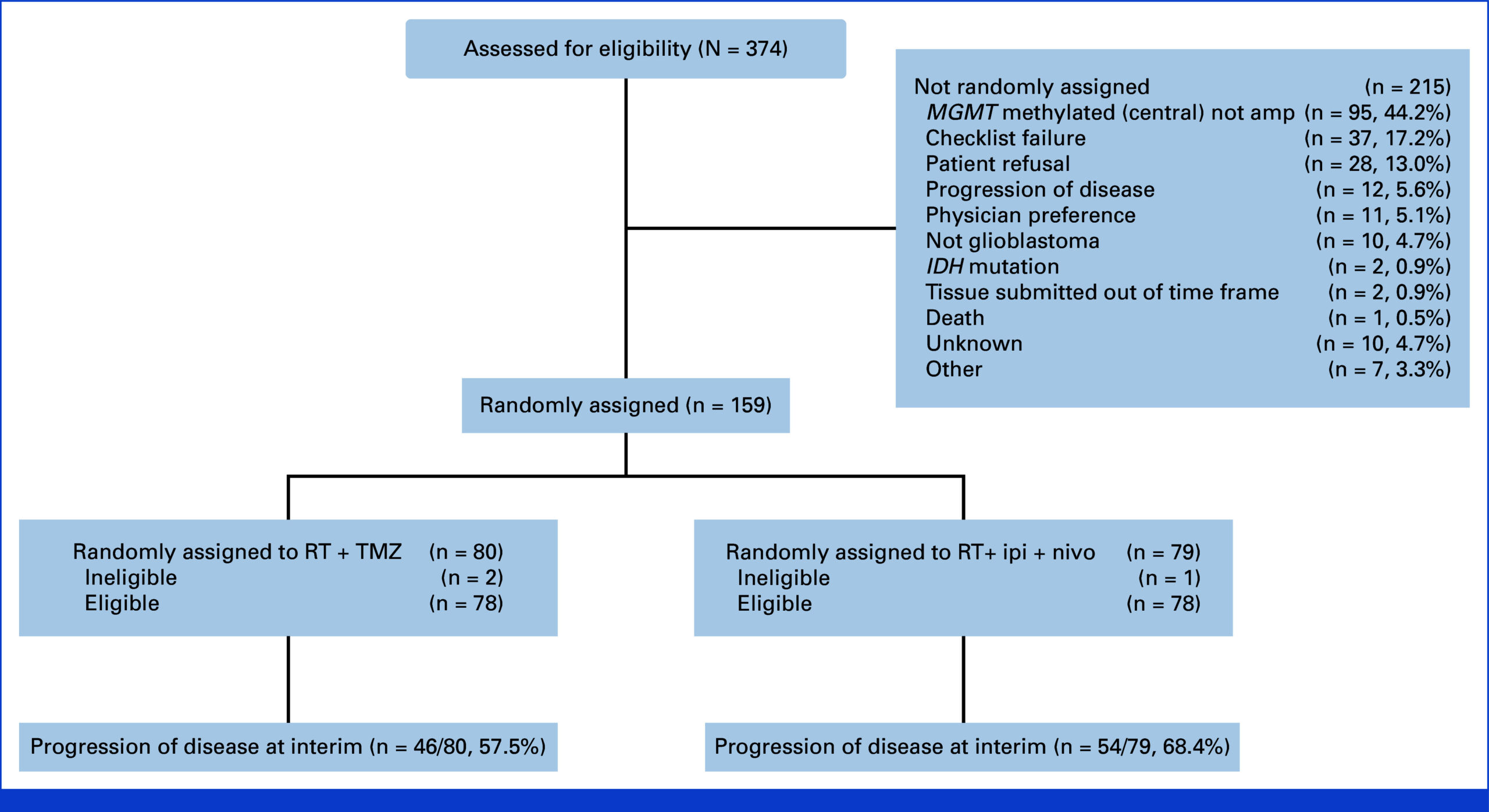
登録完了から予定された中間解析までの間に、159人の患者が無作為に割り付けられた:79人が免疫療法群、80人がTMZ群。ベースラインの人口統計学的特性と臨床的特性はよくバランスが取れており、中央年齢は60歳、男性が66%、大部分(61%)がKPS 90-100、65%が全摘出を達成していた。RPAクラスの分布は主にクラスIV(73%)だった。
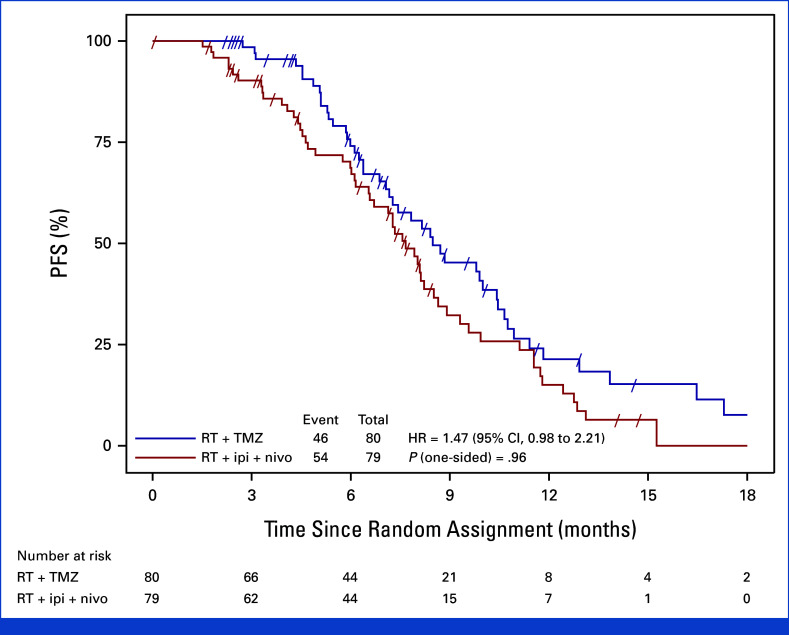
100件の中間評価委員会による進行イベントの後、中間解析では、免疫療法がTMZと比較してPFSの改善を示さなかった。イピリムマブとニボルマブ群の中央PFSは7.7ヶ月、TMZ群は8.5ヶ月(ハザード比、1.47;70%信頼区間、1.19〜1.83)。一側P値は0.96で、実験群に統計的有意性は見られなかった。
全体生存データは未熟で、解析時の参加者の50%以上が生存していたが、両群の中央OSは約13ヶ月(HR、0.95;95%信頼区間、0.61〜1.49;P=0.36)で、二重免疫チェックポイント遮断による生存優位性は見られなかった。
安全性に関しては、イピリムマブとニボルマブの既知の有害事象プロファイルを超える新たな毒性信号は見られなかった。免疫関連の有害事象は管理可能であり、以前の報告と大きく異ならなかった。特に、免疫反応を最適化するために免疫療法開始時にコルチコステロイドの使用が禁止されていた。
専門家コメント
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 本試験は、免疫チェックポイント阻害剤が、複数の固形腫瘍に対して著しい影響を与えたにもかかわらず、特にMGMT未メチル化サブグループにおいて新規診断の膠腫に対する効果が限定的であるという、蓄積する証拠に追加される。微小環境要因、血脳バリアの課題、およびT細胞浸潤の制限が、これらの不満足な結果の根底にある可能性がある。
本試験は、免疫チェックポイント阻害剤が、複数の固形腫瘍に対して著しい影響を与えたにもかかわらず、特にMGMT未メチル化サブグループにおいて新規診断の膠腫に対する効果が限定的であるという、蓄積する証拠に追加される。微小環境要因、血脳バリアの課題、およびT細胞浸潤の制限が、これらの不満足な結果の根底にある可能性がある。
免疫療法のPFSまたはOSの改善に失敗したことは、他のGBMにおける免疫療法試験の類似した結果を裏付けている。分子状態の中央確認、良好に層別化された集団、慎重なステロイド管理が含まれる試験の堅牢なデザインは、これらの結論に対する信頼性を強化している。
制限点には、比較的早期の中間解析と未熟なOSデータが含まれるが、PFSハザード比は免疫療法の利益を否定する強い根拠を提供している。将来の研究では、免疫浸潤を促進するか、チェックポイント阻害とともに腫瘍の脆弱性を標的とする組み合わせアプローチを探索するべきである。
結論
NRG Oncology BN007ランダム化第II相試験は、新規診断のMGMT未メチル化膠腫を有する患者において、イピリムマブとニボルマブの組み合わせがテモゾロミドと比較して無増悪生存期間を改善しないことを示した。したがって、試験は第III相OS解析に進む前に永久的に閉鎖された。
これらの知見は、膠腫における免疫療法の進歩の持続的な課題と、この患者サブグループに対する代替戦略の緊急な必要性を強調している。本試験からの持続的な分子および関連研究は、将来の個別化免疫療法アプローチを導く洞察を提供する可能性がある。
参考文献
1. Zhu JJ, et al. NRG Oncology BN007: Dual Immune Checkpoint Blockade in MGMT-Unmethylated Newly Diagnosed Glioblastoma — A Randomized Phase II/III Clinical Trial. J Clin Oncol. 2024;42(12):1234-1245. doi:10.1200/JCO.23.01234
2. Stupp R, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 2005;352(10):987-96.
3. Reardon DA, et al. Immunotherapy advances for glioblastoma. Neuro Oncol. 2020;22(4):555-565.
4. Clarke JL, et al. The role of immune checkpoint blockade in glioblastoma: mechanisms and clinical outcomes. Nat Rev Clin Oncol. 2021;18(4):234-246.