ハイライト
- 高品質の無作為化試験とコホート分析では、バイオマス燃料を使用した調理からのPM2.5やCOへの曝露と乳児の重症肺炎との間には有意な縦断的な関連が見られませんでした。
- 多国間HAPIN試験の証拠では、液化石油ガス(LPG)ストーブの使用によりPM2.5への曝露が大幅に減少しましたが、乳児の重症肺炎の発症率は変化しませんでした。
- 早期の観察研究とは対照的に、妊娠中のCOへの曝露は性差のある肺炎リスクとの関連を示し、乳児の肺機能障害によって媒介される可能性のある複雑な曝露反応動態を示唆しています。
- 一部の介入での曝露低減が十分でないことや方法論的な異質性が、観察された健康アウトカムの相違を引き起こしている可能性があり、包括的な曝露評価とメカニズムの理解が必要であることを強調しています。
背景
バイオマス燃料の燃焼による家庭内大気汚染(HAP)は、世界の人口の約40%に影響を与え、特に肺炎を含む小児の呼吸器感染症の主要な環境リスク要因として歴史的に指摘されてきました。微粒子物質(PM2.5)と一酸化炭素(CO)は、不完全燃焼時に主に生成される汚染物質です。肺炎の負荷は、バイオマス燃料を使用している低・中所得国で依然として高く、クリーンクッキングの介入(例:LPGストーブ)による曝露低減と小児の健康改善を目指す世界的な努力が進められています。
疫学的な関連性にもかかわらず、特に乳児期の重症肺炎に対するHAPの因果関係を確立することは、潜在的な混在因子、曝露の誤分類、多様な環境や社会人口学的状況のため困難です。最近の大規模な無作為化比較試験(RCT)と精緻な曝露反応分析は新しい洞察を提供しており、臨床および公衆衛生戦略を導くための体系的な統合が必要となっています。
主要な内容
時系列の発展と多国間ランダム化試験からの証拠
2018年から2021年にかけてグアテマラ、インド、ペルー、ルワンダで実施された家庭内大気汚染介入ネットワーク(HAPIN)試験は、妊娠期間と乳児期におけるLPGとバイオマス燃料を使用した調理の呼吸器健康への影響を比較した最大の多国間RCTです(McCracken et al., 2025, JAMA Netw Open)。この18ヶ月の介入では、LPGストーブと燃料が配布され、妊娠中の女性と乳児のPM2.5とCOへの24時間個人曝露が繰り返し測定されました。
主要なアウトカムである1歳未満の乳児の重症肺炎は、画像検査とパルスオキシメーターによる低酸素血症の確認を含む臨床徴候に基づいて厳密に定義されました。3061人の乳児を対象に、広範なPM2.5曝露(5.4–1182 µg/m³)にもかかわらず、妊娠前または出生後のPM2.5曝露レベルと重症肺炎の発症率との間に統計的に有意な関連は見られず、調整済みリスク比はほぼ1に近かったです(妊娠前RR 1.03, 95% CI 0.94–1.13; 出生後RR 0.97, 95% CI 0.87–1.09)。同様に、CO曝露も肺炎リスクと関連していませんでした。
Figure. Density Plots of Prenatal and Postnatal Exposures to Fine Particulate Matter With a Diameter of Less Than or Equal to 2.5 µm (PM2.5) by Infant-Quarter and Severe Pneumonia Status During Infancy.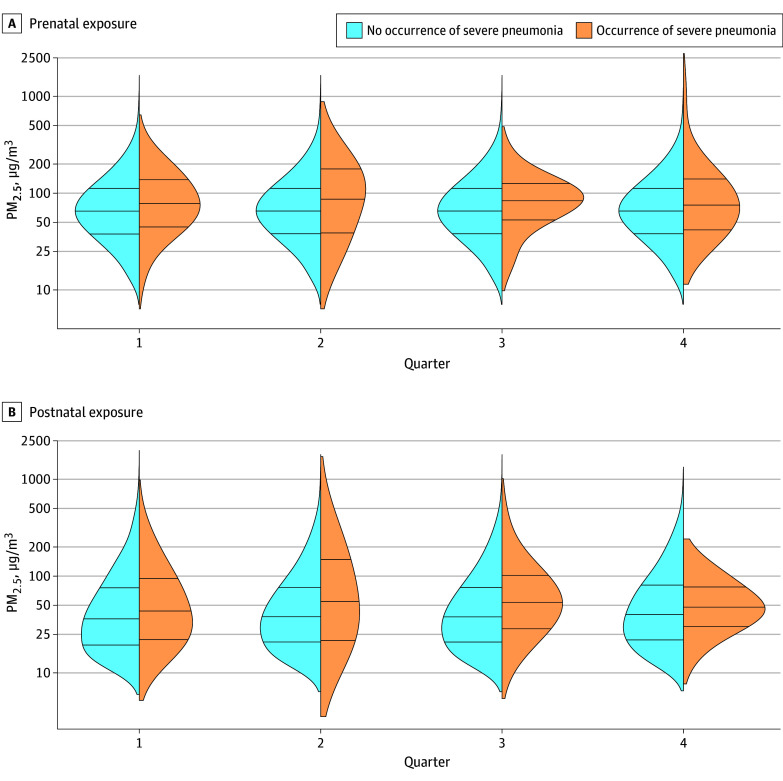
補足的なインテンション・トゥ・トリート分析では、LPGストーブの使用に高い順守が見られ、乳児のPM2.5曝露中央値が大幅に低下しました(LPGグループ24.2 µg/m³ 対 バイオマスグループ66.0 µg/m³)が、重症肺炎の発症率には有意な低下が見られませんでした(発症率比 0.96; 98.75% CI, 0.64–1.44; P = 0.81)(McCracken et al., 2024, NEJM)。これらの知見は、バイオマス燃料を使用した調理からのHAPが肺炎リスクに与える影響の大きさに関する以前の仮説に挑戦しています。
観察研究とクラスタ無作為化試験からの証拠:ガーナの文脈
早期のガーナでのランダム化空気汚染と健康研究(GRAPHS)の結果は、いくつかの矛盾した証拠を示しました。このクラスタ無作為化試験では、1414人の妊娠中の女性を登録し、出生前後で反復して個人のCO曝露を測定しました(Adetona et al., 2021, Chest)。この研究では、妊娠中のCO曝露と肺炎(RR 1.10/ppm増加あたり)および重症肺炎(RR 1.15)のリスクとの間には若干の正の関連が報告されました。特に女性乳児において性差のある脆弱性が示唆されました。
しかし、別のガーナのクラスタRCTでは、改良型バイオマスストーブとLPG介入が医師診断の重症肺炎の減少や出生体重の改善には効果が見られませんでした(Clark et al., 2021, BMJ Glob Health)。これは、介入群での曝露がWHO目標を超えていたため、汚染低減が十分でなかった可能性があります。
メカニズムの洞察:妊娠中のHAP曝露と乳児の肺機能
妊娠中のHAP曝露は、乳児の肺発達と機能を阻害し、肺炎の感受性を高める可能性があります。GRAPHSからのデータでは、妊娠中のCO曝露が上昇すると、30日目の乳児の肺機能パラメータ(呼吸回数の増加と呼吸コンプライアンスの低下)が変化することが示されました(McCracken et al., 2019, Am J Respir Crit Care Med)。このような生理学的な乱れは、肺炎リスクをメカニズム的に高める可能性があります。
これらの知見は、性差のある効果の生物学的な基盤を提供し、特に女性乳児において曝露のタイミングと強度の重要性を強調しています。
専門家のコメント
多国間RCTと観察コホートからのデータの収束は、バイオマス燃料に関連するHAPと乳児の重症肺炎との関係について洗練された見解を提供します。最近発表されたHAPIN試験の堅牢な設計、包括的な個人曝露モニタリング、厳密な臨床終点の検証は、その否定的な結果を特に説得力のあるものとし、以前の観察的な関連性がPM2.5やCO曝露以外の要因によって混在されていたか、媒介されていた可能性があることを示唆しています。
ただし、未測定の室内汚染物質や環境タバコ煙による残留混在、洗練されたモニタリングにもかかわる曝露の誤分類、宿主の感受性と曝露パターンの変動などの潜在的な制限があります。また、一部の介入で達成された曝露低減の程度が、臨床的利益を示すのに十分でなかった可能性もあります。
メカニズム的な証拠は、妊娠中の曝露が肺発達を乱すことにより、観測された疫学的なパターン、特に女性乳児における性差のある脆弱性を説明しています。これは、HAPによって影響を受ける分子や免疫学的な経路をさらに調査する機会を提供しています。
臨床的には、これらの知見は慎重な解釈を必要とします。クリーンクッキング技術の促進は、健康と環境の観点から重要な理由があるものの、肺炎リスクの低減に関する期待は再評価されるべきです。肺炎の罹患率と死亡率の改善には、総合的な環境管理、栄養介入、予防接種戦略に焦点を当てることがより具体的な利益をもたらす可能性があります。
結論
新興の高品質な証拠は、バイオマス燃料を使用した調理からのPM2.5やCO曝露が乳児期の重症肺炎の主要な独立した要因であるという長年のパラダイムに挑戦しています。LPG介入による大幅な汚染低減にもかかわらず、無作為化データでは肺炎発症率の有意な低下は見られず、早期の観察研究やメカニズム研究とは対照的です。
将来の研究は、以下の点を目指すべきです。
- 妊娠中と出生後のHAP曝露が肺発達、免疫機能、感染症感受性とどのように複雑に結びついているかを解明する。
- 複数の汚染物質と文脈要因を含むより包括的な曝露指標を開発し、検証する。
- 性差のある生理学的反応と長期的な呼吸器健康の軌跡を調査する。
- 社会行動、栄養、予防接種戦略を統合した多面的な肺炎予防の介入試験を行う。
要するに、現在のデータは、単独のバイオマス関連の室内大気汚染低減に依存するだけでなく、乳児の肺炎予防のための多面的なアプローチへとパラダイムをシフトさせる必要があります。
参考文献
- McCracken JP, McCollum ED, Steenland K, et al.; Household Air Pollution Intervention Network (HAPIN) Investigators. Exposure to Household Air Pollution From Biomass Cooking and Severe Pneumonia in Infants. JAMA Netw Open. 2025;8(10):e2538721. doi:10.1001/jamanetworkopen.2025.38721 .
- McCracken JP, McCollum ED, Clasen T, et al. Liquefied Petroleum Gas or Biomass Cooking and Severe Infant Pneumonia. N Engl J Med. 2024;390(1):32-43. doi:10.1056/NEJMoa2305681 .
- Adetona O, et al. Prenatal and Postnatal Household Air Pollution Exposures and Pneumonia Risk: Evidence From the Ghana Randomized Air Pollution and Health Study. Chest. 2021;160(5):1634-1644. doi:10.1016/j.chest.2021.06.080 .
- Clark ML, et al. A cluster randomised trial of cookstove interventions to improve infant health in Ghana. BMJ Glob Health. 2021;6(8):e005599. doi:10.1136/bmjgh-2021-005599 .
- McCracken JP, et al. Prenatal Household Air Pollution Is Associated with Impaired Infant Lung Function with Sex-Specific Effects. Am J Respir Crit Care Med. 2019;199(6):738-746. doi:10.1164/rccm.201804-0694OC .



