序論
難治性慢性咳嗽(RCC)は、既知の原因に対する検査や治療を経ても8週間以上続く持続的な咳を特徴とする重要な臨床的課題です。成人の一定の割合に影響を与え、患者の身体的、心理的、社会的幸福感を損なうことがあります。現在、RCCに対して広く利用可能で承認された治療法はなく、神経調節剤などの利用可能な治療法は、効果性の懸念や副作用により制限されています。最近の進歩は、ATPゲートイオンチャネルであるP2X3受容体に焦点を当てています。この受容体は、感覚ニューロンの活性化と咳反射の過敏性に関与すると考えられています。Camlipixantは、RCC管理のための有効性と安全性を評価するために使用される選択的P2X3アンタゴニストです。本稿では、RCC患者と基線時の咳頻度が高い成人を対象としたSOOTHE第2b相無作為化試験を批判的にレビューします。
研究デザインと方法
SOOTHEは、18〜80歳のRCC期間が1年以上かつ覚醒時の咳頻度が25回/時間以上の成人を対象とした多施設共同、二重盲検、プラセボ対照、第2b相用量探索試験でした。16日の単盲検プラセボ導入期間により、咳頻度を安定させ、プラセボ効果を軽減することを目指しました。導入期間後、310人の患者が無作為に12.5 mg、50 mg、または200 mgを1日2回投与するCamlipixant群またはプラセボ群に1:1:1:1で割り付けられました。患者は、覚醒時の咳頻度(<45または≥45回/時間)に基づいて無作為化時に層別化され、各グループ間の基線時重症度のバランスを保つようにしました。
主要評価項目は、VitaloJAK自動咳モニターを使用して測定した基線から第28日の24時間咳頻度の変化(自然対数スケールで解析)。副次評価項目には、第15日の変化、覚醒時および夜間の咳頻度、異なる咳減少閾値(≥30%、≥50%、≥70%)での反応者分析、患者報告アウトカム(咳の重症度(CS-VAS)、咳関連生活の質(レスター咳質問票;LCQ))、安全性評価が含まれました。
基線時の覚醒咳頻度が10〜25回/時間未満の探索的コホートが含まれ、200 mgのCamlipixantまたはプラセボに無作為に割り付けられましたが、有効性比較のための検出力はありませんでした。
主な知見
310人の無作為化患者のうち、249人が主要集団(覚醒咳頻度≥25回/時間)を構成しました。基線特性は均衡しており、大多数が女性(約78%)で、平均咳持続期間は10年以上でした。
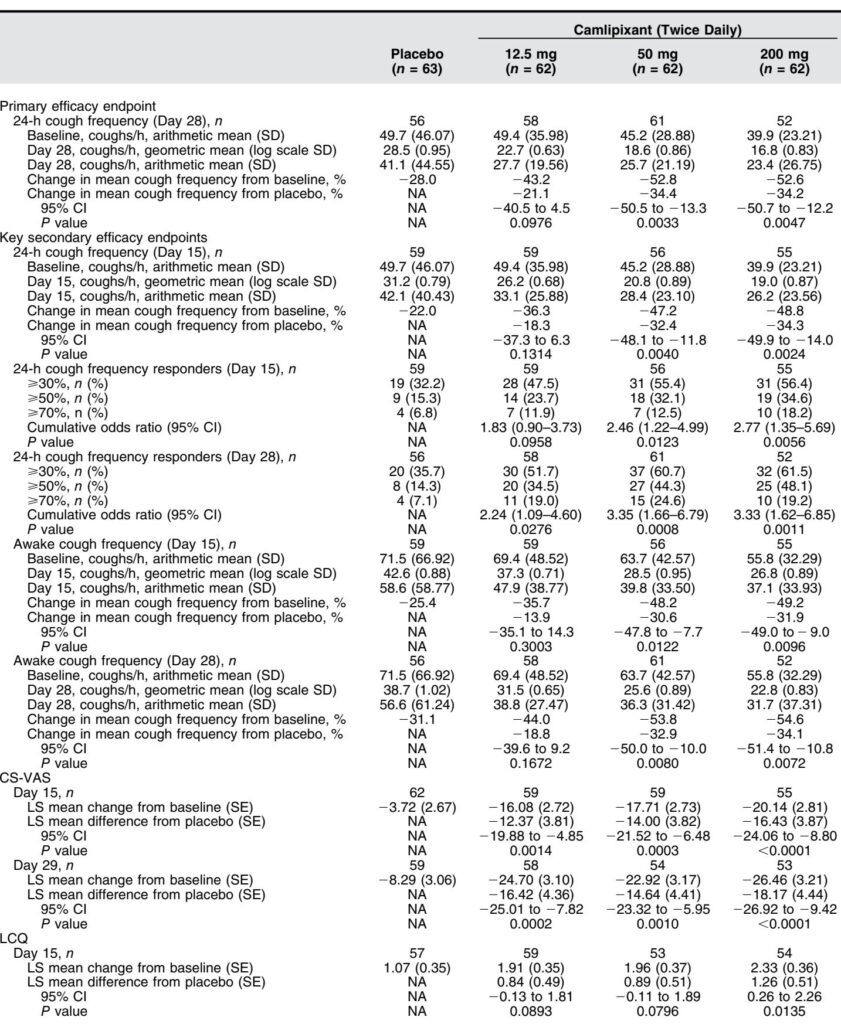
主要評価項目: 50 mgと200 mgを1日2回投与したCamlipixantは、第28日にプラセボと比較して24時間咳頻度を有意に減少させました。それぞれ34.4%(95% CI, -50.5 to -13.3; P=0.0033)と34.2%(95% CI, -50.7 to -12.2; P=0.0047)でした。12.5 mgの用量では、有意な21.1%の減少が見られませんでした。
副次評価項目:
– 50 mgと200 mgの群では、第15日時点で24時間咳頻度の有意な減少が観察されました。
– これらの用量群では、第15日と第28日時点で覚醒時の咳頻度が有意に減少しました。
– 反応者分析では、Camlipixant群の方がプラセボ群よりも臨床的に意味のある咳減少(≥30%、≥50%、≥70%)を達成した患者の割合が高いことが示されました。
– 夜間の咳頻度の減少は傾向として好ましかったが、統計学的有意性には至りませんでした。
– 患者報告アウトカムは一貫して改善しました。CS-VASスコアは、Camlipixant用量群で第15日と第29日時点で著しく低下し、LCQスコアも改善し、特に200 mg用量では生活の質の向上が示されました。
安全性と忍容性:治療関連有害事象(AEs)は、Camlipixant群とプラセボ群で類似していました。最も一般的なAEには、悪心と味覚障害(dysgeusia)があり、Camlipixant投与患者の≤6.5%とプラセボ群のいずれにも報告されました。すべての味覚関連AEは軽度から中等度であり、味覚問題による治療中止はありませんでした。深刻な治療関連AEは報告されていません。
専門家コメント
SOOTHE試験は、基線時咳頻度が高いRCC患者において、Camlipixantが咳頻度を減少させ、患者報告アウトカムを改善することを強力に示しています。プラセボ導入期間の設定と覚醒時咳頻度に基づく基線層別化は、患者選択と結果の信頼性を向上させました。
これらの知見は、gefafixantやeliafixantなどのP2X3アンタゴニストの先行研究と一致しており、同様の有効性の大きさを示していますが、味覚障害に関する忍容性プロファイルが改善している可能性があります。Camlipixantの味覚障害の発生率が低いことは、選択性P2X3アンタゴニストであるため、味覚知覚を変えるP2X2/3受容体ブロックを最小限に抑えている可能性があります。
興味深いことに、効果は基線時咳頻度と関連しているようです。これは、より重度の咳を持つ患者に焦点を当てた層別化アプローチを支持しています。この現象は、さらなるメカニズム的な調査が必要です。試験の比較的短い期間は、RCCの慢性性を考えると、長期的な有効性と安全性の評価を妨げています。
結論
50 mgと200 mgを1日2回投与するCamlipixantは、基線時咳頻度が高い難治性慢性咳嗽患者において、客観的な咳頻度を有意に減少させ、生活の質指標を改善します。特に味覚障害に関する良好な安全性と忍容性プロファイルは、RCCに対する新しい標的療法としての可能性を支持しています。
進行中の第3相試験(CALM-1とCALM-2)は、Camlipixantの治療プロファイルをさらに解明し、この未充足の患者集団における臨床的有用性を確立するでしょう。
参考文献
Smith JA, Birring SS, Blaiss MS, McGarvey L, Morice AH, Sher M, Carroll KJ, Garin M, Lanouette S, Shaw J, Yang R, Bonuccelli CM. Camlipixant in Refractory Chronic Cough: A Phase 2b, Randomized, Placebo-controlled Trial (SOOTHE). Am J Respir Crit Care Med. 2025 Jun;211(6):1038-1048. doi: 10.1164/rccm.202409-1752OC. PMID: 40043302; PMCID: PMC12180140.