序論
アルツハイマー病(AD)は、進行性の認知機能低下と世界的な大きな疾患負担を特徴とする主要な神経変性疾患であり続けている。遺伝的要因はADの感受性に大きく影響し、その中でもミエロイド細胞に発現されるトリガーリセプター2(TREM2)とアポリポタンパク質E(ApoE)の変異体が最も強力なリスク決定因子として注目されています。TREM2は、ミクログリア上のレセプターで、免疫応答とファゴサイトーシスを調節します。一方、脂質輸送体であるApoEには3つの一般的なアイソフォーム(ApoE2、ApoE3、ApoE4)があり、アミロイドβ代謝と神経炎症に影響を与えます。特に、ApoE4キャリアーはADのリスクが高まり、異なる病理学的軌道を示すことが知られています。
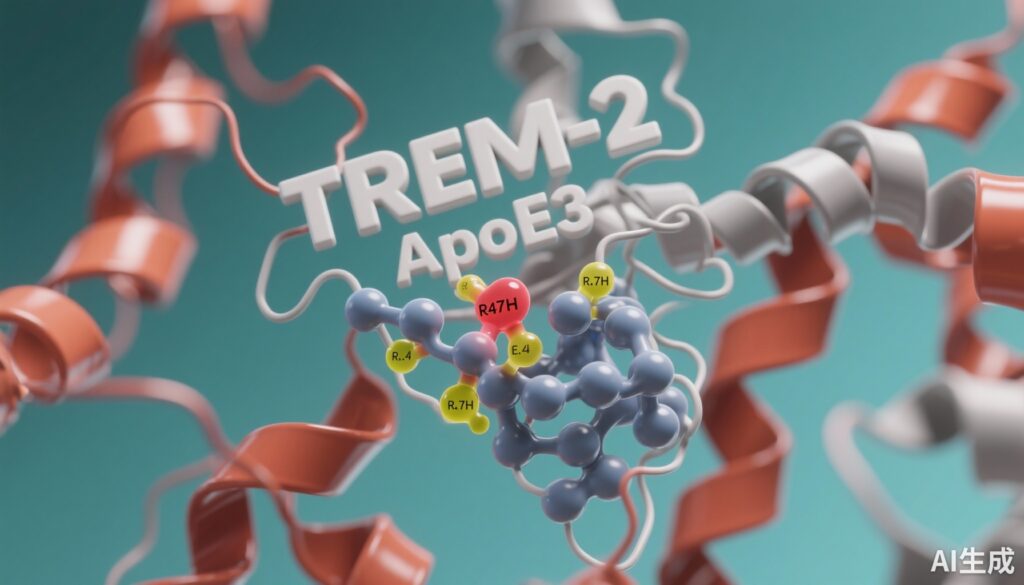
TREM2とApoE3の相互作用は実験的に示されており、これらのタンパク質の分子相互作用がミクログリアの機能とADの進行に影響を与えることを示唆しています。しかし、TREM2-apoE3結合の正確な構造的詳細と、AD関連変異体、具体的にはTREM2 R47HとApoE4がこの分子相互作用をどのように変化させるかはまだ完全には理解されていません。これらの洞察は、病態メカニズムの理解と、ADにおけるTREM2-ApoE相互作用を調整するための標的治療の開発に不可欠です。
研究デザインと方法
本研究では、コンセンサスプロテイン-プロテインドッキングと分子動力学(MD)シミュレーションを組み合わせた計算手法を用いました。これらの手法は、TREM2とApoE3が結合した複合体の実験的に一貫した三次元構造を生成し、AD関連変異体であるTREM2 R47HとApoE4の影響を検討することを目指しました。ドッキングは、実験データから導かれた制約条件に基づいて潜在的なインターフェースと結合モードを同定し、MDシミュレーションはこれらの複合体の安定性と動的挙動を評価しました。
本研究では、野生型TREM2-ApoE3複合体の構造的風景と相互作用ネットワークを、TREM2のR47H突然変異を含むものやApoE3の代わりにApoE4アイソフォームを含むものと比較しました。構造的摂動、結合親和性、多量体化傾向を分析することで、これらの突然変異がAD病態に影響を与えるメカニズムの詳細を解明しました。
主要な見なし
得られたTREM2-ApoE3複合体は、以前に報告された接触点を超えた新たな相互作用部位を明らかにしました。これらの新しいインターフェースは、より複雑な分子認識機構をサポートし、タンパク質の立体構造に影響を与えることを示唆しています。ApoE3の結合は、TREM2とApoE3の両方の立体構造に変化をもたらし、効果的な相互作用と機能的なミクログリアシグナル伝達に重要な相互適応を示しています。
AD関連のTREM2 R47H変異体は、典型的なApoE3結合モードを変更することが示されました。具体的には、R47H置換はApoE3の結合を、受容体オリゴメル化に関与するTREM2領域に向けることになり、TREM2の多量体化と下流のシグナル伝達に干渉する可能性があります。この空間的なシフトは、R47Hに伴う機能喪失の表型とその増加したADリスクを説明するのに役立つかもしれません。
ApoE3の代わりにApoE4を使用すると、複合体の両方のパートナーの立体構造の整合性が不安定になることが示されました。ApoE4は結合安定性が低く、TREM2の立体構造の変動を促進し、受容体機能とリガンド相互作用に障害を与える可能性があります。この不安定化は、ApoE4キャリアーで観察される増加したADリスクと疾患進行の加速と一致しています。
専門家のコメントとメカニズムの洞察
本研究の構造的および動的解析の統合は、遺伝的変異体がTREM2-ApoE相互作用にどのように影響を与えるかについて重要なメカニズム的理解を提供します。TREM2が神経細胞損傷とアミロイド病態に対するミクログリア反応に関与していることを考えると、TREM2-ApoE結合の障害は、ADにおけるミクログリア活性化状態と神経炎症を調節する可能性があります。
R47H突然変異が多量体化インターフェースに向かってApoE3の結合位置を再配置することから、この変異体がTREM2の集団化とシグナル伝達の強度を低下させるメカニズムが示唆されます。同様に、ApoE4による不安定化はリガンド認識とクリアランス機能を障害する可能性があります。これらの構造的摂動は、これらの変異体がAD病態に結びつく生物学的に説明可能な基盤を提供します。
これらの見なしは魅力的ですが、in silicoモデルから派生しており、生物理的および細胞実験による実験的確認が必要です。さらに、TREM2とApoEの体内での機能の複雑さは他の共因子と下流経路を含んでおり、さらなる調査が必要です。
結論と臨床的意義
本研究は、AD関連変異体TREM2 R47HとApoE4が結合動態と立体構造の安定性をどのように変更するかを分子レベルで理解することに貢献し、新たな相互作用インターフェースと立体効果を特定しました。これらの発見は、これらの高リスクアレルを有する患者におけるTREM2-ApoE相互作用の回復または調整を目的とした合理的な治療設計の基礎を提供します。
これらの特定の分子的欠陥を対象とした治療法は、ミクログリア機能の改善、神経炎症の減少、疾患進行の遅延を可能にする個人化されたAD介入の有望な手段となります。今後の多分野的研究は、構造生物学、機能実験、臨床研究を統合して、これらの洞察を効果的なAD治療に翻訳するために不可欠です。
参考文献
Greer RA, Tuckey RA, Dean HB, Brett TJ, Roberson ED, Song Y. TREM2-apoE3 interactions and Alzheimer’s disease: Molecular and structural insights and effects of TREM2 R47H and apoE4 variants. Alzheimers Dement. 2025 Oct;21(10):e70729. doi: 10.1002/alz.70729. PMID: 41085188; PMCID: PMC12519512.