ハイライト
前例のない無増悪生存率
標準的なレナリドミドとリツキシマブ(R2)療法にエポリタマブを追加した結果、R2単独と比較して病気の進行または死亡リスクが79%減少しました(ハザード比 0.21)。
優れた奏効率
この組み合わせ療法の全奏応率(ORR)は95%で、R2コントロール群で観察された79%よりも有意に高かったため、難治性の患者集団において高い有効性を示しました。
管理可能な安全性プロファイル
エポリタマブ群ではグレード3以上の有害事象の発生率が高かったものの、サイトカイン放出症候群(CRS)イベントは主に低グレード(グレード1-2)であり、すべて成功裏に解決されました。これにより、外来または地域での使用が可能であることが確認されました。
濾胞性リンパ腫の進化する治療環境
濾胞性リンパ腫(FL)は最も一般的な低悪性度非ホジキンリンパ腫です。この疾患は、化学免疫療法への高い初期反応を特徴としますが、繰り返し再発するパターンがあり、各々の治療ラインでしばしばより短い寛解期間が得られる傾向があります。初期治療から24か月以内に病気が進行する患者(POD24)や複数の治療ラインに対して難治性の患者の場合、臨床予後は歴史的に不良でした。
近年、化学療法フリーの治療法への移行が大きな勢いを得ています。免疫調整剤のレナリドミドと抗CD20モノクローナル抗体のリツキシマブ(R2療法)は、AUGMENT試験の結果に基づいて、再発または難治性(R/R)FLの標準治療として確立されました。しかし、より深い持続的な反応を誘導し、従来の細胞毒性化学療法に関連する蓄積毒性を回避できるより強力な組み合わせに対する需要は依然として大きいです。
生物学的根拠:エポリタマブとT細胞活性化
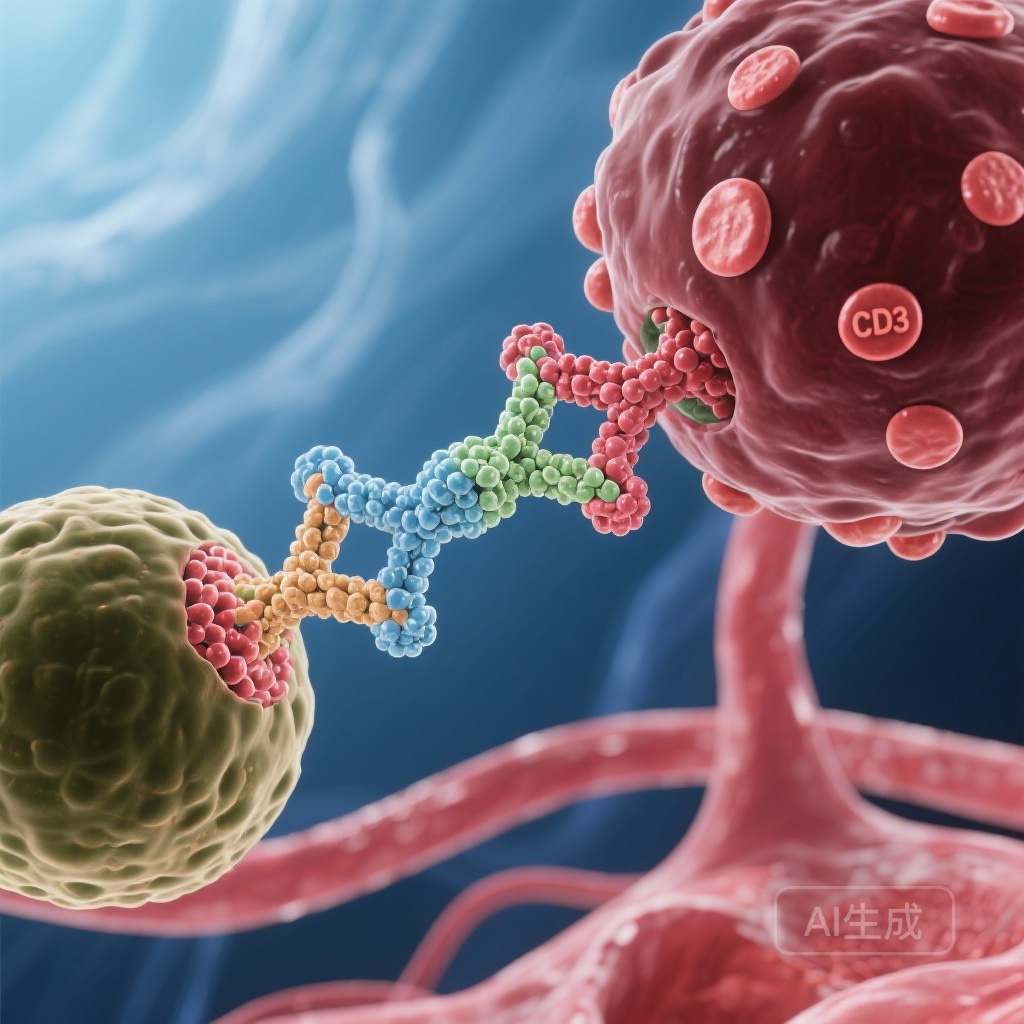
エポリタマブは、T細胞上のCD3とB細胞上のCD20を標的とする初の皮下投与型バイスペシフィック抗体です。その作用機序は、自己の細胞毒性T細胞をCD20陽性の悪性B細胞の特異的な除去に誘導することです。CAR-T細胞療法とは異なり、エポリタマブは複雑な製造と患者固有のエンジニアリングを必要としない「オフ・ザ・シェルフ」免疫療法であり、さまざまな臨床設定でより容易に投与できます。
エポリタマブとR2を組み合わせる根拠は相乗的です。レナリドミドはT細胞と自然キラー(NK)細胞の活性を高め、エポリタマブによって誘導されるT細胞介在性細胞毒性を潜在的に強化します。リツキシマブは、抗体依存性細胞毒性(ADCC)と補体依存性細胞毒性(CDC)を通じて追加的なB細胞除去を提供します。これら3つの組み合わせアプローチは、免疫系がリンパ腫細胞を排除する能力を最大限に引き出すことを目指しています。
EPCORE FL-1:試験デザインと参加者の特性
EPCORE FL-1試験は、30か国189施設で実施された世界的、オープンラベル、無作為化第3相試験です。この試験には、少なくとも1回の化学免疫療法を受けたR/R濾胞性リンパ腫患者488人が登録されました。参加者は1:1の比率で、エポリタマブとR2の組み合わせまたはR2単独を最大12サイクル受けました。
エポリタマブの投与スケジュールは、サイトカイン放出症候群のリスクを軽減するために設計され、最初のサイクルではステップアップ投与を行い、サイクル1-3では週1回、サイクル4-12では4週間に1回の投与が行われました。レナリドミドは毎日(各28日サイクルの1-21日)、リツキシマブはサイクル1では週1回、サイクル2-5では月1回投与されました。主要評価項目は、独立審査委員会(IRC)による全奏応率(ORR)と無増悪生存率(PFS)でした。
効果評価:PFSにおけるパラダイムシフト
この試験は、統計学的および臨床的に著しい意義を持つ主要評価項目を達成しました。中央値14.8か月の追跡調査で、エポリタマブとR2の組み合わせ群のORRは95%(95%信頼区間 92-97)で、R2コントロール群は79%(95%信頼区間 74-84)(p<0.0001)でした。この高い反応率は、エポリタマブの追加がR/R濾胞性リンパ腫に見られる抵抗メカニズムを克服できることを示唆しています。
より重要なのは、無増悪生存データに明显的な利点があったことです。進行または死亡のハザード比(HR)は0.21(95%信頼区間 0.14-0.31、p<0.0001)で、エポリタマブ組み合わせが病気の進行リスクをほぼ80%低下させました。16か月の推定PFS率は、エポリタマブ-R2群で85.5%、R2群で40.2%でした。コントロール群(R2)が歴史的な基準と一貫していたことから、これらの結果は実験的な三剤療法の効力が際立っていることを示しています。
安全性分析:免疫療法プロファイルの管理
既存の治療法に強力な免疫療法を追加したことで予想されたように、エポリタマブとR2の組み合わせ群では有害事象(AE)の発生率が高くなりました。グレード3以上のAEは、三剤組み合わせを受けた参加者の90%で、R2群では68%で観察されました。最も多い高グレードAEは血液学的であり、これはレナリドミドの既知の安全性プロファイルと一致していました。
バイスペシフィック抗体の主要な焦点は、サイトカイン放出症候群(CRS)の発生頻度と重症度です。EPCORE FL-1試験では、エポリタマブ-R2群の26%の患者でCRSが観察されました。重要なことに、すべてのCRSイベントは低グレード(21%がグレード1、5%がグレード2)であり、グレード3以上のCRSイベントは報告されていません。すべての症例は、必要に応じてトシリズマブや副腎皮質ホルモンを使用した標準的なプロトコルで管理可能で、解決されました。重度のCRSの低い発生率と皮下投与ルートは、主要な学術移植センター以外での広範な臨床利用が可能であることを示唆しています。
臨床的意味と専門家のコメント
EPCORE FL-1試験の結果は、濾胞性リンパ腫の治療における重要なマイルストーンを代表しています。第3相試験でハザード比0.21を達成したことにより、エポリタマブとR2の組み合わせ療法は、二次治療以降の新しい効力ベンチマークを設定しました。これらの知見は、早期にT細胞活性化療法を統合することで、強度の高い化学療法や自家末梢血幹細胞移植なしで深く持続的な寛解を達成できる可能性があることを示唆しています。
分野の専門家は、この試験で観察された高い奏応率とPFSの利益が、現在の治療順序に挑戦する可能性があると指摘しています。CAR-T細胞療法は高い効力を提供しますが、論理的な複雑さや毒性の懸念から、通常は後方ラインの治療に留められます。エポリタマブ-R2は、早期に病態経過で投与できる、効果的で「オフ・ザ・シェルフ」の代替治療法を提供します。これは、POD24などの高リスク特徴を持つ患者の長期予後に寄与する可能性があります。
ただし、医師は、蓄積毒性の管理と持続的なB細胞欠損に関連する感染症リスクの増加に注意を払う必要があります。この試験で使用された12サイクルの固定期間アプローチは、最大の治療効果と治療間隔や免疫回復の必要性とのバランスを取る重要な設計要素です。
結論
EPCORE FL-1試験は、エポリタマブとR2の組み合わせが、再発または難治性濾胞性リンパ腫の患者において、R2単独よりも優れていることを明確に示しています。この組み合わせ療法は、無増悪生存期間を大幅に延長しながら、管理可能な安全性プロファイルを維持する、極めて効果的な化学療法フリーの選択肢を提供します。これらの知見は、エポリタマブとR2の組み合わせが、二次治療またはその後の濾胞性リンパ腫の治療における新しい標準となり、この慢性かつ再発性の悪性腫瘍の管理を変革する可能性があることを示しています。
資金提供と臨床試験情報
EPCORE FL-1試験は、AbbVieとGenmabによって資金提供されました。この試験はClinicalTrials.gov(NCT05409066)とEudraCT(2021-000169-34)に登録されています。試験は現在進行中ですが、募集は終了しています。
参考文献
Falchi L, Nijland M, Huang H, et al. Epcoritamab, lenalidomide, and rituximab versus lenalidomide and rituximab for relapsed or refractory follicular lymphoma (EPCORE FL-1): a global, open-label, randomised, phase 3 trial. Lancet. 2026;407(10524):161-173. doi:10.1016/S0140-6736(25)02360-8.
Leonard JP, Trneny M, Izutsu K, et al. AUGMENT: A Phase III Study of Lenalidomide Plus Rituximab Versus Placebo Plus Rituximab in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol. 2019;37(14):1188-1199.