Nền tảng
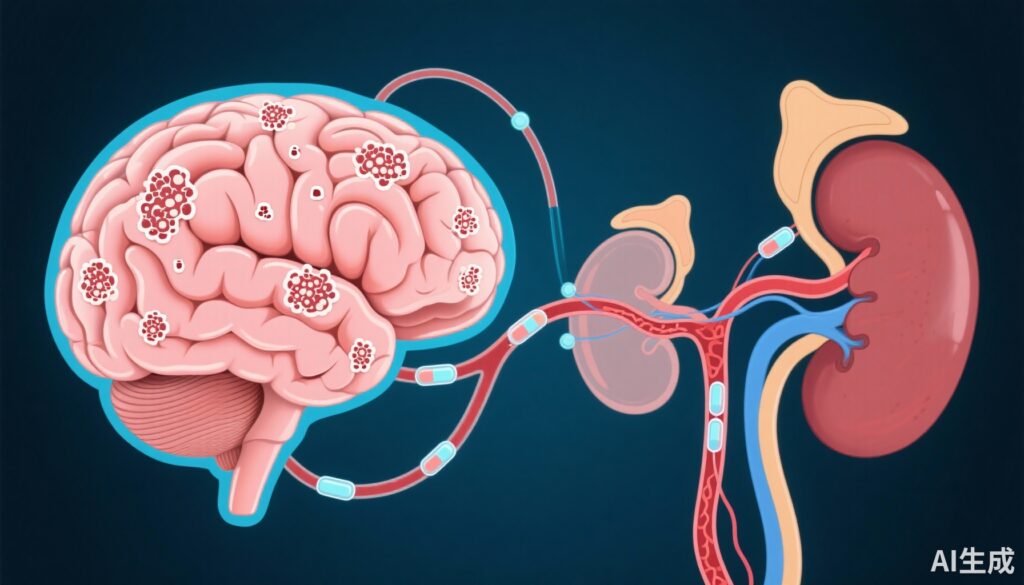
Bệnh Alzheimer (AD) vẫn là nguyên nhân hàng đầu gây ra sa sút trí tuệ trên toàn thế giới, với việc chẩn đoán ngày càng được hỗ trợ bởi các dấu sinh học chính xác dựa trên máu phản ánh bệnh lý thần kinh tiềm ẩn. Các dấu sinh học này bao gồm các peptit amyloid-β (Aβ42, Aβ40), các isoform tau phosphorylated, và các dấu hiệu thoái hóa thần kinh như chuỗi nhẹ neurofilament (NfL) và protein axit sợi glial (GFAP). Tuy nhiên, các bệnh lý hệ thống đồng mắc, đặc biệt là suy thận, có thể làm nhiễu loạn mức độ dấu sinh học máu do sự thay đổi trong chuyển hóa và thanh thải. Cho thấy việc sử dụng rộng rãi các dấu sinh học máu trong quy trình chẩn đoán AD lâm sàng, việc hiểu tác động của chức năng thận đối với mức độ dấu sinh học và giá trị dự đoán của chúng cho bệnh lý amyloid là quan trọng đối với y học chính xác.
Thiết kế nghiên cứu
Cuộc điều tra này đã phân tích 242 người tham gia từ nhóm Translational Biomarkers in Aging and Dementia (TRIAD), bao gồm các đối chứng không rối loạn nhận thức (n=124), rối loạn nhận thức nhẹ (MCI, n=58), sa sút trí tuệ do Alzheimer (n=34), và các trường hợp sa sút trí tuệ không phải AD (n=26). Tất cả người tham gia đã trải qua chụp hình PET amyloid với [18F] AZD-4694 để xác định tình trạng amyloid-β não. Máu được phân tích bằng các bài kiểm tra Simoa siêu nhạy để định lượng Aβ42, Aβ40, các isoform tau phosphorylated p-tau181, p-tau217, p-tau231, các đoạn N-terminal tau (NTA-tau), GFAP, và NfL.
Chức năng thận được đánh giá bằng tốc độ lọc cầu thận ước tính (eGFR, mL/phút/1.73 m2), tính toán thông qua creatinin huyết thanh cùng với tuổi và giới tính. Người tham gia được phân loại theo các giai đoạn bệnh thận mạn tính (CKD) 1 đến 3 dựa trên ngưỡng eGFR. Các mô hình hồi quy tuyến tính đã đánh giá mối liên hệ giữa eGFR và mỗi dấu sinh học máu. Các mô hình hồi quy logistic đã đánh giá việc kết hợp eGFR có cải thiện khả năng dự đoán tính dương tính của amyloid-β ngoài mức độ dấu sinh học và các biến số nhân khẩu học hay không.
Kết quả chính
Nồng độ của các dấu sinh học máu thường cao hơn ở những người tham gia có CKD giai đoạn 3, sau đó là những người có giai đoạn 2 và 1. Sự khác biệt thống kê đáng kể giữa các giai đoạn CKD đã được quan sát đối với NfL huyết tương, Aβ42, và Aβ40, nhưng không đối với tỷ lệ Aβ42/Aβ40. Phân tích tuyến tính tiết lộ mối liên hệ nghịch đảo đáng kể của eGFR với hầu hết các dấu sinh học ngoại trừ NTA-tau, cho thấy rằng chức năng thận thấp hơn tương quan với nồng độ dấu sinh học cao hơn, đặc biệt là đối với Aβ40 và NfL.
Điều chỉnh cho tuổi, giới tính, hoặc tỷ lệ hấp thu chuẩn hóa của PET amyloid (SUVr) làm giảm đáng kể mối liên hệ, với các mối liên hệ đáng kể chỉ còn tồn tại đối với Aβ40, Aβ42, NfL, và GFAP. Điều này cho thấy các yếu tố nhân khẩu học và gánh nặng amyloid não部分地混淆了肾功能与生物标志物之间的联系。
至关重要的是,将eGFR纳入预测模型以预测amyloid-β阳性,并没有在包括血浆生物标志物、年龄和性别的基础上改善模型拟合度或区分准确性。尽管年龄和性别显著提高了预测能力,但加入肾功能参数并没有带来有意义的临床益处,这通过Akaike信息标准和受试者工作特征曲线下面积进行评估。
专家评论
本研究提供了关于肾功能对AD血液生物标志物影响的细致见解。观察到肾功能受损个体中蛋白质生物标志物浓度升高可能反映了系统清除率降低,而不是神经退行性变本身增加。然而,在关键协变量调整后显著性的丧失强化了肾功能的混杂效应在大多数生物标志物解释中是适度的。
重要的是,诊断准确度最高的AD病理生物标志物,如p-tau217,不受eGFR的影响,突显了其稳健性。这些发现与某些低分子量蛋白在肾功能下降时可能在血浆中积累的生物学合理性一致。当临床表型不明确时,应考虑肾功能障碍可能导致一般神经退行性标志物(如NfL)水平升高。
局限性包括队列中相对保留的肾功能范围,限制了对中度至重度肾病结论的推广。未来的研究需要包括更广泛的CKD严重程度。此外,纵向评估生物标志物动态变化与进展性肾功能障碍的关系可以更好地阐明因果机制。
结论
这项严格评估表明,轻度至中度肾功能下降与选择性AD生物标志物的血浆浓度升高有关,特别是Aβ40、Aβ42、NfL和GFAP。然而,在控制人口统计因素和淀粉样蛋白负担后,这些关联减弱,并且重要的是,考虑肾功能并不能改善临床预测amyloid-β阳性的能力。
因此,在正常至轻度受损范围内,肾功能不会实质性地损害血浆AD生物标志物的临床实用性,尤其是那些具有高特异性的生物标志物,如p-tau217。这支持了在记忆诊所中应用基于血液的生物标志物检测而不必常规调整肾功能的实用性,尽管在解释定量值时仍需注意肾功能。