Những điểm nổi bật
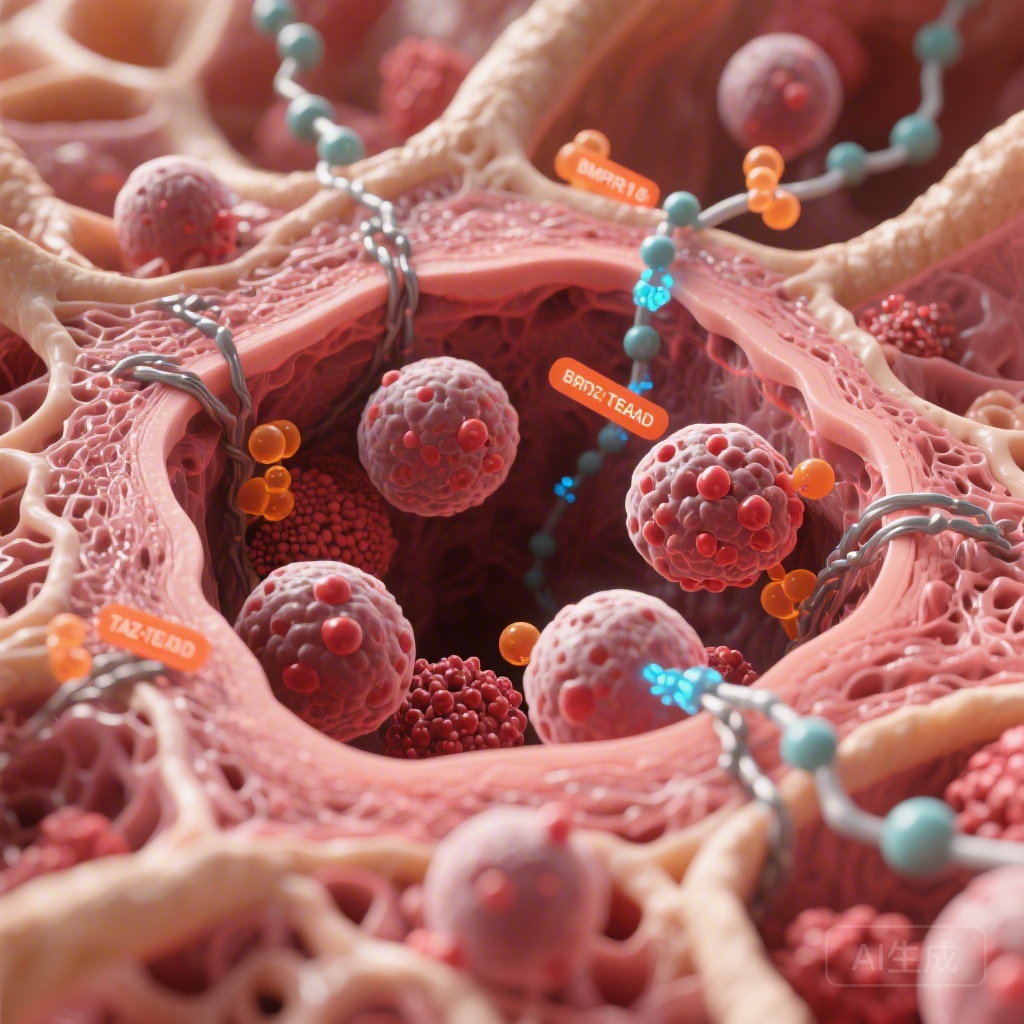
- Mức độ biểu hiện của BMPR1B và TAZ/TEAD tăng đáng kể ở bệnh nhân và tế bào AML tái phát kháng lại cytarabine hoặc venetoclax.
- Các thay đổi vật lý của tủy xương, bao gồm sự cứng lên của ma trận ngoại tế bào và tăng áp lực nội tủy, thúc đẩy sự tồn tại của tế bào bạch cầu.
- Tế bào gốc mô sợi (MSCs) dưới điều kiện chật hẹp tiết ra BMP4, kích hoạt đặc hiệu tế bào AML kháng hóa trị.
- Ức chế kết hợp BMPR1B hoặc TAZ/TEAD với cytarabine hiệu quả làm sạch tế bào AML nguyên phát trong mô hình tủy xương người 3D.
Giới thiệu: Cảnh quan Sinh học cơ học của AML
Trong nhiều thập kỷ, việc quản lý bệnh bạch cầu cấp tính (AML) tập trung chủ yếu vào cảnh quan di truyền và epigenetic của các tế bào bạch cầu. Dù đã giới thiệu các liệu pháp nhắm mục tiêu như ức chế FLT3 và venetoclax, tỷ lệ sống sót sau 5 năm vẫn chỉ khoảng 20%. Sự bế tắc lâm sàng này cho thấy hiểu biết của chúng ta về kháng hóa trị chưa đầy đủ. Một lượng lớn bằng chứng hiện nay chỉ ra rằng môi trường vi mô tủy xương (BM) không chỉ là nơi dự trữ thụ động cho tế bào, mà còn là một thành phần vật lý chủ động trong tiến trình bệnh.
Khi các tế bào bạch cầu phát triển theo kiểu clonal, chúng thay đổi cơ bản các tính chất vật lý của tủy xương. “Sự tái cấu trúc sinh học cơ học” này bao gồm sự cứng lên của ma trận ngoại tế bào (ECM), tăng áp lực nội tủy, và giảm đáng kể không gian vật lý cho các tế bào cư trú. Mặc dù những thay đổi này đã được quan sát trong các khối u rắn trong nhiều năm, vai trò của chúng trong sự sống còn của các bệnh ác tính huyết học chỉ mới được làm rõ. Nghiên cứu của Barral et al. (2026) cung cấp một bước đột phá quan trọng, xác định quá trình chuyển đổi cơ học—quá trình tế bào chuyển đổi kích thích cơ học thành tín hiệu hóa học—là động lực chính của kháng hóa trị trong AML.
Thiết kế nghiên cứu và Khung phương pháp luận
Các nhà nghiên cứu sử dụng một cách tiếp cận đa chiều để điều tra vai trò của stress cơ học trong AML. Nghiên cứu sử dụng các mẫu AML nguyên phát thu thập tại thời điểm chẩn đoán và tái phát, cũng như các dòng tế bào được thiết kế đặc biệt để kháng lại các chất điều trị chuẩn, cytarabine (Ara-C) và venetoclax.
Để mô phỏng các ràng buộc vật lý của tủy xương bạch cầu, nhóm nghiên cứu đã phát triển một mô hình tủy xương người 3D. Nền tảng này cho phép thao tác chính xác độ cứng của ma trận và sự hạn chế của tế bào, cung cấp môi trường sinh lý liên quan hơn so với các nền văn hóa 2D truyền thống. Nghiên cứu tập trung vào hai con đường chuyển đổi cơ học chính: con đường Bone Morphogenetic Protein (BMP) và các tác nhân của con đường Hippo, TAZ và YAP. Qua phân tích transcriptomic và định lượng protein, các tác giả tìm hiểu cách các con đường này phản ứng với áp lực cơ học của ngách bạch cầu.
Kết quả chính: Trục BMPR1B và TAZ/TEAD
Sự gia tăng của BMPR1B và TAZ trong kháng thuốc
Phân tích cho thấy mối tương quan đáng chú ý giữa tín hiệu chuyển đổi cơ học và kết quả lâm sàng. Các bệnh nhân tái phát sau hóa trị cho thấy mức độ BMPR1B (một receptor BMP) và TAZ, cùng với đối tác chuyển bản TEAD, cao hơn đáng kể so với tình trạng lúc chẩn đoán ban đầu. Thú vị là, mặc dù TAZ được tăng cường, paralog của nó là YAP—thường được coi là cảm biến cơ học trung tâm trong các mô khác—không cho thấy sự tăng cường tương tự. Điều này gợi ý một vai trò cụ thể, không trùng lặp, của TAZ trong ngữ cảnh của tủy xương bạch cầu.
Mô hình này được phản ánh trong các thí nghiệm in vitro. Các dòng tế bào AML kháng lại cytarabine và venetoclax thể hiện sự kích hoạt liên tục của phức hợp TAZ/TEAD. Những tế bào kháng này không chỉ khác biệt về mặt di truyền; chúng còn khác biệt về mặt cơ học. Chúng thể hiện khả năng bám dính tốt hơn vào các thành phần môi trường như fibronectin và laminin, và tăng tính biến dạng nội tại, cho phép chúng di chuyển và sống sót trong các không gian chật hẹp, áp lực cao của tủy xương chật chội.
Tín hiệu Paracrine: Liên kết MSC
Nghiên cứu cũng nhấn mạnh một cuộc giao tiếp quan trọng giữa các tế bào bạch cầu và tế bào gốc mô sợi cư trú (MSCs). Trong điều kiện chật hẹp vật lý—mô phỏng sự chật chội của tủy xương chứa đầy bạch cầu—MSCs được tìm thấy có mức độ biểu hiện BMP4 cao hơn. BMP4 do MSCs tiết ra hoạt động như một tín hiệu paracrine đặc hiệu kích hoạt BMPR1B trên bề mặt của tế bào AML kháng hóa trị. Sự tương tác này dường như tạo ra một “hiệu ứng ngách” bảo vệ, nơi stress vật lý của bệnh kích hoạt một tín hiệu sống sót bảo vệ các bạch cầu khỏi apoptosis do hóa trị gây ra.
Nhắm vào Cơ học để Làm nhạy cảm các tế bào bạch cầu
Có lẽ phát hiện lâm sàng quan trọng nhất là hiệu quả của ức chế dược lý. Sử dụng mô hình tủy xương người 3D, các nhà nghiên cứu đã chứng minh rằng nhắm vào BMPR1B hoặc phức hợp TAZ/TEAD có thể phá vỡ chu kỳ kháng thuốc. Khi các ức chế chuyển đổi cơ học này được kết hợp với cytarabine, có sự suy yếu đồng thời của sự tồn tại của tế bào AML nguyên phát. Bằng cách chặn khả năng cảm nhận và phản ứng của tế bào với môi trường cứng, áp lực cao, điều trị hiệu quả “bộc lộ” các tế bào bạch cầu, khiến chúng dễ bị tổn thương bởi liệu pháp hóa trị thông thường một lần nữa.
Bình luận Chuyên gia: Hiểu biết Cơ học và Ý nghĩa Lâm sàng
Các phát hiện của Barral et al. đại diện cho một sự thay đổi mô hình trong cách chúng ta tiếp cận AML kháng thuốc. Truyền thống, chúng ta coi tủy xương là một khoang lỏng, nhưng nghiên cứu này buộc chúng ta phải coi nó giống như môi trường vi mô của khối u rắn, nơi các lực vật lý quyết định số phận tế bào.
Việc tham gia cụ thể của TAZ thay vì YAP là một điểm sinh học thú vị. Trong nhiều ung thư biểu mô, YAP và TAZ thường được kích hoạt cùng nhau, nhưng ngách bạch cầu có thể đặt các yêu cầu cơ học độc đáo lên tế bào, ưu tiên chương trình chuyển bản TAZ-TEAD. Sự cụ thể này cung cấp một cửa sổ điều trị hẹp hơn, và có thể hiệu quả hơn, cho việc phát triển thuốc.
Tuy nhiên, có những hạn chế cần xem xét. Mặc dù mô hình tủy xương 3D là một bước tiến đáng kể, nó không thể tái tạo hoàn toàn độ phức tạp hệ thống của một bệnh nhân người, bao gồm vai trò của hệ miễn dịch trong ngách. Hơn nữa, áp lực nội tủy trong AML là động; hiểu cách các con đường này dao động trong các giai đoạn khác nhau của điều trị cảm ứng và cố định sẽ rất quan trọng cho việc xác định thời điểm của các can thiệp nhắm mục tiêu chuyển đổi cơ học.
Từ góc độ chính sách y tế và thử nghiệm lâm sàng, các kết quả này cho thấy chúng ta nên bắt đầu kết hợp các dấu hiệu sinh học cơ học—có thể thông qua hình ảnh hóa nâng cao hoặc phân tích sinh thiết chuyên biệt—vào việc phân loại rủi ro cho AML. Nếu một bệnh nhân có tủy xương đặc biệt cứng hoặc áp lực cao, họ có thể là ứng cử viên tiềm năng cho can thiệp sớm với ức chế BMPR1B hoặc TAZ.
Kết luận: Một trụ cột mới trong Điều trị AML
Việc xác định BMPR1B và TAZ/TEAD là các trung gian của kháng hóa trị mở ra một lĩnh vực mới trong hematologie-oncologie. Bằng cách giải quyết thực tế vật lý của tủy xương bạch cầu, chúng ta có thể cuối cùng vượt qua sự kháng thuốc do môi trường gây ra, điều đã làm phiền AML trong thời gian dài. Các chiến lược điều trị tương lai kết hợp các chất ức chế chuyển hóa cơ học với các chất ức chế truyền thống hứa hẹn mang lại sự thuyên giảm sâu hơn và tỷ lệ tái phát thấp hơn cho bệnh nhân hiện có ít lựa chọn. Khi chúng ta tiến tới năm 2026 và xa hơn, việc tích hợp sinh học cơ học vào điều trị lâm sàng sẽ có thể trở thành một trụ cột của y học chính xác.
Tham khảo
- Barral L, Lespinasse N, Martin Cardozo C, et al. Targeting BMP and TAZ/TEAD mechanotransduction pathways impairs acute myeloid leukemia chemoresistance. Leukemia. 2026-03-18. PMID: 41851473.
- Lampi MC, Reinhart-King CA. Targeting extracellular matrix stiffness to attenuate disease progression. Sci Transl Med. 2018;10(422).
- Passaro D, et al. Increased Bone Marrow Pressure Drives Hematopoietic Stem Cell Loss and Myeloid Neoplasia. Cell Stem Cell. 2021.
- Dupont S, et al. Role of YAP/TAZ in mechanotransduction. Nature. 2011;474(7350):179-183.