Giới thiệu và Bối cảnh
Ung thư dạ dày vẫn là nguyên nhân hàng đầu gây tử vong do ung thư trên toàn thế giới, tập trung ở Đông Á, một số khu vực Nam Mỹ và Trung Á. Năm 2025, Bản đồng thuận toàn cầu Taipei II (Gut 2025; Liou et al.) đã xem xét lại liệu và làm thế nào sàng lọc và diệt trừ Helicobacter pylori nên được sử dụng như một chiến lược phòng ngừa chính. Cập nhật này phản hồi các bằng chứng mới quan trọng kể từ bản đồng thuận đầu tiên của Taipei (2020), bao gồm hai thử nghiệm cộng đồng rất lớn (JAMA 2024; Nat Med 2024), tiến bộ trong các phương pháp điều trị diệt trừ (thuốc chống axit bismuth quadruple therapy, và các phác đồ dựa trên chất ức chế cạnh tranh axit kali [PCAB]), và dữ liệu mới về an toàn dài hạn (vi khuẩn, kháng thuốc và kết quả thực quản).
Bài viết này tổng hợp các khuyến nghị và bằng chứng cốt lõi từ Bản đồng thuận toàn cầu Taipei II, nhấn mạnh những gì đã thay đổi so với hướng dẫn trước đây, và chuyển đổi sự đồng thuận thành các cách tiếp cận thực tế cho bác sĩ, nhà quy hoạch y tế công cộng và nhà nghiên cứu.
Những điểm nổi bật của hướng dẫn mới
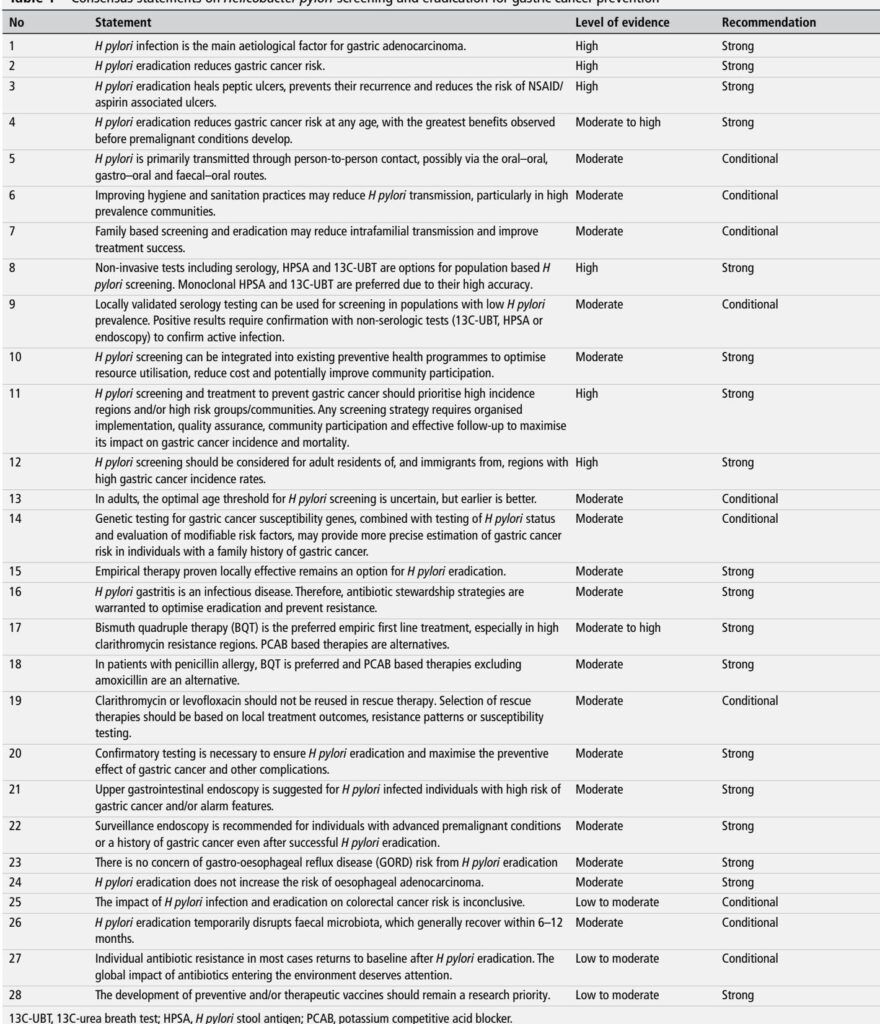
– Phạm vi đồng thuận: 32 chuyên gia từ 12 quốc gia; quá trình Delphi đã tạo ra 28 tuyên bố đồng thuận sử dụng GRADE. (Liou JM et al., Gut 2025).
– Kết luận chung: Diệt trừ H. pylori giảm nguy cơ ung thư dạ dày và nên được đề xuất cho tất cả người lớn bị nhiễm, với lợi ích lớn nhất khi đạt được trước khi có thay đổi tiền ung thư (khuyến nghị mạnh mẽ, bằng chứng cao–trung bình).
– Tập trung vào sàng lọc: ưu tiên các khu vực có tỷ lệ mắc cao và nhóm nguy cơ cao (cư dân và người nhập cư từ các khu vực có tỷ lệ mắc ung thư dạ dày cao).
– Chẩn đoán: Ưu tiên các xét nghiệm không xâm lấn cho sàng lọc cộng đồng—xét nghiệm hơi thở urea 13C (13C-UBT) và kháng nguyên phân lập đơn clonal trong phân (HPSA) là các xét nghiệm ưa thích; huyết thanh học được xác nhận địa phương có thể được sử dụng trong các khu vực tỷ lệ mắc thấp, miễn là kết quả dương tính được xác nhận bằng các xét nghiệm không phải huyết thanh.
– Điều trị: Điều trị kinh nghiệm vẫn được chấp nhận khi được chứng minh hiệu quả tại địa phương. Thuốc chống axit bismuth quadruple therapy (BQT) là phác đồ kinh nghiệm ưu tiên đầu tiên, đặc biệt trong các khu vực có kháng clarithromycin vừa phải–cao; các phác đồ dựa trên PCAB (ví dụ, vonoprazan)–dual therapy (đặc biệt là vonoprazan–amoxicillin) được công nhận là lựa chọn thay thế.
– Quản lý và an toàn: Kiểm tra xác nhận sau điều trị được khuyến nghị mạnh mẽ; áp dụng nguyên tắc quản lý kháng sinh; diệt trừ không tăng nguy cơ ung thư biểu mô thực quản và sự rối loạn vi khuẩn thường tự phục hồi trong vòng 6–12 tháng.
– Triển khai chương trình: tích hợp sàng lọc H. pylori vào các chương trình phòng ngừa sức khỏe hiện có nếu có thể; tổ chức với đảm bảo chất lượng, tham gia cộng đồng và hệ thống theo dõi.
Những điểm cần lưu ý cho bác sĩ:
– Đề xuất kiểm tra và điều trị cho người lớn bị nhiễm H. pylori ở các môi trường nguy cơ cao; xác nhận diệt trừ khách quan (13C-UBT hoặc HPSA).
– Đối với điều trị kinh nghiệm, ưu tiên BQT ở các khu vực có kháng macrolide cao; sử dụng PCAB–amoxicillin dual therapy ở các môi trường phù hợp.
– Không tái sử dụng clarithromycin hoặc levofloxacin cho điều trị cứu chữa mà không có hướng dẫn nhạy cảm.
Các khuyến nghị cập nhật và những thay đổi quan trọng (so với Taipei 2020 và các hướng dẫn trước đó)
Các cập nhật chính và lý do:
– Ủng hộ mạnh mẽ hơn cho các chương trình sàng lọc cộng đồng. Tại sao: hai thử nghiệm cộng đồng/pragmatic lớn (JAMA 2024; Nat Med 2024) cung cấp bằng chứng cấp độ dân số rằng sàng lọc và điều trị giảm tỷ lệ mắc ung thư dạ dày—mặc dù hiệu ứng nhỏ và bị ảnh hưởng bởi tuân thủ và thiết kế thử nghiệm.
– Cập nhật thứ tự ưu tiên của các phác đồ điều trị: BQT vẫn là lựa chọn kinh nghiệm hàng đầu ở các khu vực có kháng macrolide phổ biến; các phác đồ dựa trên PCAB dual/triple (ví dụ, vonoprazan–amoxicillin) hiện có sự hỗ trợ mạnh mẽ hơn từ các thử nghiệm ngẫu nhiên đối chứng (RCT) và phân tích tổng hợp gần đây cho thấy tỷ lệ diệt trừ cao và khả năng dung nạp tốt (Gut 2024–2025; Gastroenterology 2022).
– Nhấn mạnh kiểm tra xác nhận: khuyến nghị mạnh mẽ hơn rằng kiểm tra xác nhận nên được thực hiện thường xuyên sau điều trị (4–6 tuần sau khi điều trị sử dụng UBT hoặc HPSA) để xác nhận diệt trừ và hạn chế điều trị lại không cần thiết.
– Tiếp cận dựa trên gia đình: khuyến nghị rõ ràng hơn và hỗ trợ từ mô hình kinh tế cho việc sàng lọc/diệt trừ dựa trên gia đình hoặc hộ gia đình trong các cộng đồng tỷ lệ mắc cao để giảm tái nhiễm.
– Xem xét an toàn: đánh giá hệ thống về tác động dài hạn đến vi khuẩn và kháng thuốc, và khẳng định rằng diệt trừ không liên quan đến tăng nguy cơ ung thư biểu mô thực quản ở cấp độ dân số.
Bảng tóm tắt (gọn):
– Ai cần sàng lọc: người lớn sống ở hoặc nhập cư từ các khu vực tỷ lệ mắc cao, và các nhóm nguy cơ khác (mạnh).
– Các xét nghiệm sàng lọc ưu tiên: 13C-UBT hoặc kháng nguyên phân lập đơn clonal (mạnh).
– Huyết thanh học: được chấp nhận trong các khu vực tỷ lệ mắc thấp nếu được xác nhận địa phương và theo sau bằng kiểm tra xác nhận cho kết quả dương tính (điều kiện).
– Điều trị kinh nghiệm đầu tiên: BQT ưu tiên ở các khu vực có kháng clarithromycin vừa phải–cao; các phác đồ dựa trên PCAB là lựa chọn thay thế (mạnh).
– Xác nhận diệt trừ: bắt buộc ở bệnh nhân nguy cơ cao và được khuyến nghị mạnh mẽ nói chung (mạnh).
– Nội soi: chỉ định cho người bị nhiễm có dấu hiệu báo động hoặc các dấu hiệu nguy cơ cao khác; giám sát dành cho các thay đổi tiền ung thư tiến triển hoặc tiền sử ung thư dạ dày (mạnh).
Các khuyến nghị theo từng chủ đề
(Mỗi mục ghi mức độ bằng chứng và sức mạnh khuyến nghị như được trình bày bởi sự đồng thuận)
1) Nguyên nhân và tác động của việc diệt trừ
– Tuyên bố: H. pylori là nguyên nhân chính của ung thư biểu mô dạ dày (Bằng chứng cao; Khuyến nghị mạnh).
– Diệt trừ giảm nguy cơ ung thư dạ dày (Bằng chứng cao; Mạnh). Các phân tích tổng hợp và nhiều RCT, các nghiên cứu nhóm lớn cho thấy giảm tỷ lệ nguy cơ tương đối; cũng đề xuất lợi ích về tỷ lệ tử vong.
2) Ai nên ưu tiên sàng lọc
– Mục tiêu chính: Người lớn cư trú ở các khu vực tỷ lệ mắc ung thư dạ dày cao và người nhập cư từ những khu vực đó (Bằng chứng cao; Mạnh).
– Lý do: gánh nặng tập trung theo địa lý; các mô hình hiệu quả chi phí ủng hộ việc nhắm mục tiêu vào các dân số có nguy cơ cao hơn.
– Cách tiếp cận thực tế được đề xuất: bản đồ tỷ lệ mắc ung thư dạ dày địa phương, xác định các nhóm dân số tỷ lệ mắc cao (ví dụ, một số nhóm sắc tộc, cộng đồng bản địa), và triển khai các chương trình có tổ chức với lời mời, kiểm tra, điều trị và các con đường theo dõi.
3) Độ tuổi và thời điểm tối ưu
– Tuyên bố: Độ tuổi tối ưu chưa chắc chắn nhưng sớm hơn là tốt hơn; diệt trừ sớm (trước khi có thay đổi tiền ung thư) mang lại lợi ích lớn nhất (Bằng chứng trung bình; Khuyến nghị điều kiện).
– Lưu ý thực tế: Mô hình và khả thi lập luận cho việc sàng lọc ở độ tuổi thường được đề xuất giữa cuối 30 và giữa 40 ở các khu vực nguy cơ cao; tích hợp với các sàng lọc khác (ví dụ, FIT đại tràng ở tuổi 45) có thể là thực tế.
4) Các xét nghiệm sàng lọc và chẩn đoán
– Các xét nghiệm ưa thích: 13C-UBT và kháng nguyên phân lập đơn clonal HPSA (Bằng chứng cao; Mạnh).
– Huyết thanh học: được chấp nhận trong các khu vực tỷ lệ mắc thấp nếu các xét nghiệm được xác nhận địa phương; kết quả dương tính huyết thanh phải được xác nhận bằng các xét nghiệm không phải huyết thanh trước khi điều trị (Bằng chứng trung bình; Điều kiện).
– Thời điểm xét nghiệm: tránh xét nghiệm trong hoặc ngay sau khi sử dụng PPIs/PCABs (ngừng PPIs/PCABs 2 tuần, kháng sinh/bismuth 4 tuần trước khi xét nghiệm) để tránh kết quả âm tính giả.
5) Chiến lược điều trị
– Điều trị kinh nghiệm: được phép nếu hiệu quả tại địa phương (Bằng chứng trung bình; Mạnh).
– Đầu tiên: Thuốc chống axit bismuth quadruple therapy (BQT: PPI/PCAB + bismuth + tetracycline + metronidazole) ưa thích trong các khu vực có kháng clarithromycin; các phác đồ 10–14 ngày được khuyến nghị tùy thuộc vào dữ liệu địa phương. PCAB–amoxicillin dual therapy (ví dụ, vonoprazan–amoxicillin) là lựa chọn thay thế hiệu quả được hỗ trợ bởi RCT (Bằng chứng trung bình–cao; Mạnh).
– Dị ứng penicillin: BQT ưa thích; các phác đồ PCAB không có amoxicillin được chấp nhận (Bằng chứng trung bình; Mạnh).
– Điều trị cứu chữa/kháng trị: tránh tái sử dụng clarithromycin hoặc levofloxacin mà không có xác nhận nhạy cảm; chọn các phác đồ cứu chữa dựa trên kháng thuốc địa phương hoặc AST (Điều kiện).
6) Quản lý kháng sinh
– Nguyên tắc cốt lõi: Diệt trừ H. pylori là điều trị bệnh nhiễm trùng và phải được hướng dẫn bởi các nguyên tắc quản lý (Bằng chứng trung bình; Mạnh).
– Biện pháp thực tế: chọn các phác đồ ít bị ảnh hưởng bởi kháng thuốc phổ biến, sử dụng điều trị dựa trên nhạy cảm khi có sẵn (phân tử hoặc nuôi cấy), xác nhận khỏi, theo dõi các kết quả diệt trừ địa phương và xu hướng kháng thuốc, và ưu tiên hỗ trợ tuân thủ.
7) Kiểm tra xác nhận và nội soi
– Xác nhận diệt trừ: được khuyến nghị 4–6 tuần sau khi hoàn thành điều trị bằng 13C-UBT hoặc HPSA (Bằng chứng trung bình; Mạnh).
– Nội soi trên: được đề xuất cho người bị nhiễm có triệu chứng báo động, tiền sử ung thư dạ dày, pepsinogen bất thường, hoặc các dấu hiệu nguy cơ cao khác (Bằng chứng trung bình; Mạnh).
– Giám sát: được khuyến nghị cho những người có các tình trạng tiền ung thư tiến triển (OLGA/OLGIM III–IV, atrophy loại mở) hoặc tiền sử ung thư dạ dày ngay cả sau khi diệt trừ thành công (Bằng chứng trung bình; Mạnh).
8) Nguy cơ và an toàn dài hạn
– GERD và ung thư biểu mô thực quản: diệt trừ không tăng nguy cơ ung thư biểu mô thực quản dài hạn (Bằng chứng trung bình; Mạnh).
– Vi khuẩn: diệt trừ gây rối loạn tạm thời vi khuẩn phân, thường phục hồi trong vòng 6–12 tháng; ý nghĩa lâm sàng vẫn chưa rõ (Bằng chứng trung bình; Điều kiện).
– Kháng thuốc: Tăng kháng thuốc cá nhân thường tạm thời và trở lại mức cơ bản, nhưng tác động dân số và môi trường đòi hỏi giám sát cẩn thận và quản lý (Bằng chứng thấp–trung bình; Điều kiện).
9) Tiếp cận dựa trên gia đình và cộng đồng
– Sàng lọc và điều trị dựa trên gia đình có thể giảm truyền nhiễm trong gia đình và cải thiện thành công diệt trừ trong các cộng đồng tỷ lệ mắc cao (Bằng chứng trung bình; Điều kiện).
– Ví dụ chương trình: Chương trình Matsu của Đài Loan, các sáng kiến cộng đồng bản địa khác và phương pháp chỉ số gia đình minh họa khả thi và tác động.
Bình luận và nhận xét của chuyên gia
Quan điểm của ban đồng thuận (tóm tắt):
– “Diệt trừ H. pylori hiện là công cụ phòng ngừa chính dựa trên bằng chứng cho ung thư dạ dày ở nhiều môi trường.” (quan điểm cốt lõi)
– Các chuyên gia nhấn mạnh rằng kích thước lợi ích thay đổi theo nguy cơ cơ bản, tuân thủ và thời điểm; lợi ích dân số lớn nhất đạt được khi các chương trình ưu tiên các khu vực tỷ lệ mắc cao và đạt được tỷ lệ tham gia cao và diệt trừ được xác nhận.
– Ủy ban tranh luận về sàng lọc phổ quát hay nhắm mục tiêu; sự nhất trí ủng hộ ưu tiên các khu vực và nhóm nguy cơ cao trong khi đề xuất các chương trình thí điểm và đánh giá địa phương ở nơi khác.
– Vẫn còn tranh cãi: Độ tuổi tối ưu để bắt đầu sàng lọc; cân nhắc giữa việc diệt trừ rộng rãi và quản lý kháng sinh; hậu quả dài hạn đối với vi khuẩn và kháng thuốc dân số; và cách kết hợp tốt nhất các chương trình H. pylori với các dịch vụ sàng lọc ung thư hiện có.
Những thông điệp thực tế từ chuyên gia:
– Triển khai sàng lọc và điều trị như một chương trình có tổ chức với các chỉ số chất lượng: tỷ lệ mời/tham gia, tỷ lệ sử dụng xét nghiệm, tỷ lệ hoàn thành điều trị, tỷ lệ xác nhận khỏi và tỷ lệ thành công diệt trừ địa phương.
– Sử dụng giám sát kháng thuốc địa phương để hướng dẫn các lựa chọn kinh nghiệm; ở nơi có kiểm tra nhạy cảm, sử dụng AST phân tử để điều chỉnh phác đồ.
– Đảm bảo giáo dục bệnh nhân vững chắc và hỗ trợ tuân thủ; xem xét các phác đồ liều cố định hoặc đơn giản hóa để cải thiện tỷ lệ hoàn thành.
Suy luận thực tế: Chuyển đổi sự đồng thuận thành thực hành
Các xem xét cấp hệ thống:
– Tích hợp sàng lọc H. pylori vào các dịch vụ phòng ngừa hiện có (ví dụ, kết hợp lấy mẫu kháng nguyên phân trong phân với FIT đại tràng nếu có thể) để tiết kiệm chi phí và tận dụng cơ sở hạ tầng mời gọi đã được thiết lập (bằng chứng và ví dụ do thử nghiệm thực tế JAMA và nền tảng quốc gia của Đài Loan cung cấp).
– Triển khai thí điểm: bắt đầu với các khu vực địa lý tỷ lệ mắc cao hoặc các nhóm dân số nguy cơ cao để chứng minh khả thi, điều chỉnh các con đường giới thiệu và tinh chỉnh hiệu quả chi phí địa phương.
Luồng công việc thực hành lâm sàng (đề xuất):
1. Xác định ứng cử viên cho sàng lọc (người lớn từ khu vực tỷ lệ mắc cao hoặc các tiêu chí nguy cơ cao khác).
2. Đề xuất xét nghiệm không xâm lấn—ưu tiên 13C-UBT hoặc kháng nguyên phân lập đơn clonal.
3. Nếu dương tính, tư vấn về lợi ích/rủi ro và đề xuất điều trị diệt trừ với phác đồ ưa thích được hướng dẫn bởi kháng thuốc địa phương.
4. Sau điều trị, thực hiện kiểm tra xác nhận (13C-UBT hoặc HPSA) ít nhất 4–6 tuần sau khi hoàn thành điều trị và sau khi ngừng PPIs/PCABs.
5. Nếu nhiễm trùng kéo dài, chọn các phác đồ cứu chữa dựa trên kiểm tra nhạy cảm nếu có; tránh sử dụng lại macrolides/fluoroquinolones kinh nghiệm.
6. Đối với bệnh nhân có triệu chứng báo động, pepsinogen bất thường hoặc tiền sử gia đình, giới thiệu cho nội soi và phân loại nguy cơ (OLGA/OLGIM).
Vignette bệnh nhân (minh họa):
John, một người đàn ông Mỹ gốc Hàn 48 tuổi, không có triệu chứng báo động nhưng có tiền sử gia đình mắc ung thư dạ dày (bố được chẩn đoán ở tuổi 62), đến khám sức khỏe sơ cấp. Dựa trên nền tảng của anh, anh được đề xuất kiểm tra H. pylori; 13C-UBT dương tính. Sau khi tư vấn, anh nhận được 14 ngày BQT (kháng clarithromycin địa phương >15%). Anh hoàn thành điều trị với buồn nôn nhẹ. 6 tuần sau khi điều trị, 13C-UBT âm tính—thành công điều trị được ghi nhận. Do có tiền sử gia đình, giới thiệu cho nội soi trên và lập bản đồ dạ dày cơ bản để phân loại và lập kế hoạch giám sát theo OLGA/OLGIM.
Các ưu tiên nghiên cứu trong tương lai (được xếp hạng bởi sự đồng thuận)
Hướng dẫn liệt kê chín lĩnh vực nghiên cứu ưu tiên. Trong số đó:
– Xác định độ tuổi tối ưu để sàng lọc nhằm tối đa hóa lợi ích suốt đời và hiệu quả chi phí.
– Định rõ các khoảng thời gian giám sát và chiến lược cho bệnh nhân có các tổn thương tiền ung thư (OLGA/OLGIM phân loại).
– Nghiên cứu dài hạn về vi khuẩn, trao đổi chất và hệ miễn dịch của việc diệt trừ cấp dân số.
– Phát triển và thử nghiệm lâm sàng vắc-xin H. pylori (phòng ngừa và điều trị) và các phương pháp không dùng kháng sinh (ức chế urease, chất chống bám dính).
– Các nghiên cứu triển khai lớn, đa quốc gia đánh giá các kết quả dân số, sinh thái kháng thuốc và tác động môi trường của việc sử dụng kháng sinh hàng loạt.
Cái gì không thay đổi—Nguyên tắc bền vững
– H. pylori vẫn là chất gây ung thư nhóm 1 và là mục tiêu có thể hành động để phòng ngừa ung thư dạ dày.
– Ở nơi có năng lực nội soi và gánh nặng bệnh tật rất cao, kết hợp diệt trừ với sàng lọc nội soi vẫn là chiến lược hợp lý.
– Kiểm tra xác nhận khỏi vẫn là trụ cột của thực hành lâm sàng tốt để xác nhận diệt trừ và hạn chế điều trị lại không cần thiết.
Lời kết: Cân bằng lợi ích, rủi ro và khả thi
Bản đồng thuận toàn cầu Taipei II (2025) đưa lĩnh vực từ sự ủng hộ khái niệm của sàng lọc và điều trị sang các khuyến nghị thực tế, dựa trên bằng chứng cho việc triển khai. Hướng dẫn nhấn mạnh rằng diệt trừ giảm nguy cơ ung thư dạ dày và ngăn ngừa bệnh loét dạ dày tá tràng, nhưng hiệu ứng ở cấp dân số phụ thuộc vào thiết kế chương trình: ai được mời, xét nghiệm nào được sử dụng, phác đồ nào được chọn, và liệu có cơ sở hạ tầng xác nhận khỏi và giám sát hay không. Quản lý kháng sinh và theo dõi liên tục kháng thuốc là cần thiết, cũng như đầu tư vào nghiên cứu—đặc biệt là phát triển vắc-xin và các phương pháp không dùng kháng sinh—sẽ giảm sự phụ thuộc vào kháng sinh toàn thân.
Đối với các bác sĩ và nhà lãnh đạo y tế công cộng, thông điệp là rõ ràng: ở các môi trường có nguy cơ ung thư dạ dày cao, các chương trình sàng lọc và điều trị H. pylori có tổ chức—xây dựng với đảm bảo chất lượng, tham gia cộng đồng và các biện pháp bảo vệ quản lý—are now supported by stronger evidence and pragmatic recommendations.
Tài liệu tham khảo
(Các tài liệu tham khảo chính được trích dẫn trong bài viết này; bản đồng thuận đầy đủ chứa danh sách tham khảo toàn diện.)
1. Liou JM, Malfertheiner P, Hong TC, et al. Screening and eradication of Helicobacter pylori for gastric cancer prevention: Taipei Global Consensus II. Gut. 2025;74:1767–1791. doi:10.1136/gutjnl-2025-336027.
2. Lee Y‑C, Chiang T‑H, Chiu H‑M, et al. Screening for Helicobacter pylori to Prevent Gastric Cancer: A Pragmatic Randomized Clinical Trial. JAMA. 2024;332:1642–1651.
3. Pan K‑F, Li W‑Q, Zhang L, et al. Gastric cancer prevention by community eradication of Helicobacter pylori: a cluster‑randomized controlled trial. Nat Med. 2024;30:3250–3260.
4. Malfertheiner P, Megraud F, Rokkas T, et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus. Gut. 2022;71:1724–1762.
5. Chey WD, Howden CW, Moss SF, et al. ACG Clinical Guideline: Treatment of Helicobacter pylori Infection. Am J Gastroenterol. 2024;119:1730–1753.
6. Best LM, Takwoingi Y, Siddique S, et al. Non‑invasive diagnostic tests for Helicobacter pylori infection. Cochrane Database Syst Rev. 2018;CD012080.
7. Liou JM, Jiang X‑T, Chen C‑C, et al. Second‑line levofloxacin‑based quadruple therapy versus bismuth‑based quadruple therapy and long‑term microbiota/resistome outcomes: Lancet Gastroenterol Hepatol. 2023;8:228–241.
8. Lee Y‑C, Chiang T‑H, Chou C‑K, et al. Association Between Helicobacter pylori Eradication and Gastric Cancer Incidence: A Systematic Review and Meta‑analysis. Gastroenterology. 2016;150:1113–1124.
9. Fukase K, Kato M, Kikuchi S, et al. Effect of eradication of Helicobacter pylori on incidence of metachronous gastric carcinoma after endoscopic resection: Lancet 2008;372:392–397.
10. WHO. Antimicrobial stewardship programmes in healthcare facilities (toolkit). Geneva: WHO; 2019.
(Để biết danh sách toàn diện, xem bài đồng thuận đầy đủ: Liou et al., Gut 2025.)