Nhấn Mạnh
Thời Gian Sống Không Tiến Trình Chưa Từng Có
Việc thêm epcoritamab vào liệu pháp tiêu chuẩn lenalidomide và rituximab (R2) đã giảm 79% nguy cơ tiến triển bệnh hoặc tử vong so với nhóm R2 đơn thuần (Tỷ lệ Nguy cơ 0.21).
Tỷ Lệ Đáp Ứng Tốt Hơn
Kết hợp này đạt tỷ lệ đáp ứng tổng thể (ORR) là 95%, cao hơn đáng kể so với 79% được quan sát ở nhóm đối chứng R2, cho thấy hiệu quả cao trong dân số khó điều trị.
Hồ Sơ An Toàn Có Thể Quản Lý Được
Mặc dù tỷ lệ xảy ra sự cố bất lợi cấp độ 3 hoặc cao hơn cao hơn ở nhóm epcoritamab, các sự cố hội chứng giải phóng cytokine (CRS) chủ yếu là nhẹ (cấp độ 1-2) và tất cả đều được giải quyết thành công, hỗ trợ việc sử dụng liệu pháp này trong môi trường ngoại trú hoặc cộng đồng.
Bối Cảnh Biến Động của Bệnh Bạch Cầu Tế Bào Phôi
Bệnh bạch cầu tế bào phôi (FL) vẫn là bệnh bạch cầu không Hodgkin ủ mạn phổ biến nhất. Mặc dù bệnh này đặc trưng bởi phản ứng ban đầu cao đối với hóa miễn dịch, nhưng nó cũng được định nghĩa bằng mẫu lặp lại các đợt tái phát, với mỗi lần điều trị tiếp theo thường mang lại thời gian thuyên giảm ngắn hơn. Đối với những bệnh nhân có tiến triển bệnh trong vòng 24 tháng sau điều trị ban đầu (POD24) hoặc kháng nhiều loại điều trị, tiên lượng lâm sàng trước đây thường kém.
Trong những năm gần đây, xu hướng chuyển sang các liệu pháp không sử dụng hóa chất đã tăng cường đáng kể. Sự kết hợp của lenalidomide, một chất điều hòa miễn dịch, và rituximab, một kháng thể đơn dòng chống CD20 (liệu pháp R2), đã trở thành chuẩn mực điều trị cho bệnh bạch cầu tế bào phôi phục hồi hoặc kháng thuốc (R/R) sau kết quả của thử nghiệm AUGMENT. Tuy nhiên, vẫn còn nhu cầu cấp thiết về các sự kết hợp mạnh mẽ hơn có thể gây ra những đáp ứng sâu và bền vững hơn mà không có các độc tính tích lũy liên quan đến hóa chất độc hại truyền thống.
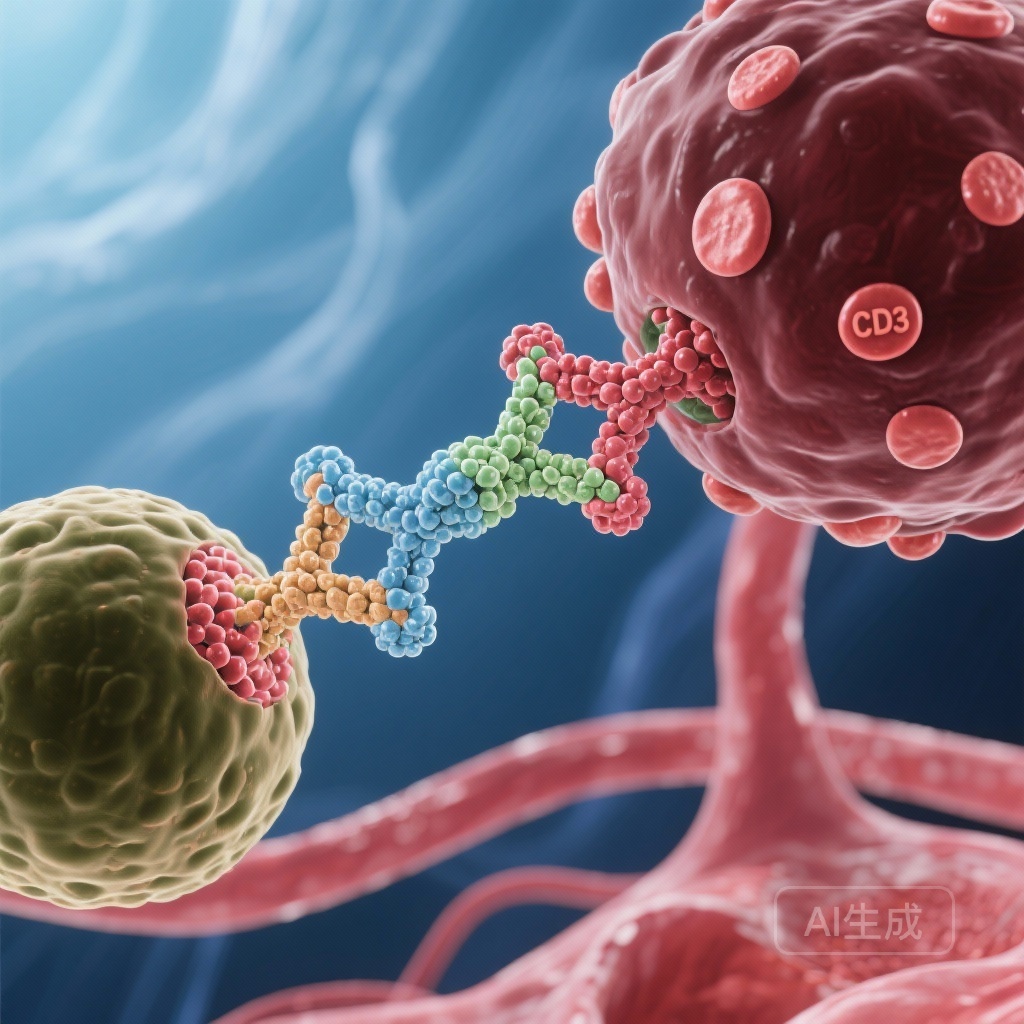
Lý Luận Sinh Học: Epcoritamab và Sự Tham Gia của T-Cells
Epcoritamab là một kháng thể song đặc hiệu tiêm dưới da đầu tiên, nhắm mục tiêu CD3 trên T-cells và CD20 trên B-cells. Cơ chế tác động của nó liên quan đến việc định hướng các T-cells độc tính nội sinh để tiêu diệt cụ thể các B-cells ác tính dương tính với CD20. Khác với các liệu pháp CAR-T, cần sản xuất phức tạp và kỹ thuật riêng biệt cho từng bệnh nhân, epcoritamab là một liệu pháp miễn dịch “sẵn sàng sử dụng” có thể được quản lý dễ dàng hơn trong các bối cảnh lâm sàng khác nhau.
Lý do kết hợp epcoritamab với R2 là cùng tác dụng. Lenalidomide tăng cường hoạt động của T-cells và các tế bào sát thủ tự nhiên (NK), có thể tăng cường độc tính T-cell do epcoritamab gây ra. Rituximab cung cấp thêm sự tiêu diệt B-cells thông qua độc tính tế bào phụ thuộc kháng thể (ADCC) và độc tính phụ thuộc bổ thể (CDC). Cùng nhau, cách tiếp cận kết hợp ba thuốc này nhằm tối đa hóa khả năng của hệ thống miễn dịch trong việc tiêu diệt các tế bào bạch cầu.
EPCORE FL-1: Thiết Kế Nghiên Cứu và Đặc Điểm Người Tham Gia
Thử nghiệm EPCORE FL-1 là một thử nghiệm toàn cầu, mở, ngẫu nhiên, giai đoạn 3 được thực hiện tại 189 trung tâm ở 30 quốc gia. Nghiên cứu đã tuyển chọn 488 người tham gia mắc bệnh bạch cầu tế bào phôi phục hồi hoặc kháng thuốc đã nhận ít nhất một liệu pháp hóa miễn dịch trước đó. Người tham gia được phân ngẫu nhiên theo tỷ lệ 1:1 để nhận epcoritamab cộng với R2 hoặc R2 đơn thuần trong tối đa 12 chu kỳ.
Lịch dùng epcoritamab được thiết kế để giảm thiểu nguy cơ hội chứng giải phóng cytokine, sử dụng cách tiếp cận tăng liều dần dần trong chu kỳ đầu tiên, sau đó là quản lý hàng tuần trong các chu kỳ 1-3 và mỗi bốn tuần trong các chu kỳ 4-12. Lenalidomide được quản lý hàng ngày (ngày 1-21 của mỗi chu kỳ 28 ngày), và rituximab được quản lý hàng tuần trong chu kỳ 1 và hàng tháng trong các chu kỳ 2-5. Hai điểm cuối chính là tỷ lệ đáp ứng tổng thể (ORR) và thời gian sống không tiến triển (PFS) do ủy ban đánh giá độc lập (IRC) xác định.
Kết Quả Hiệu Quả: Một Sự Thay Đổi Mô Hình trong PFS
Thử nghiệm đã đạt được các điểm cuối chính với ý nghĩa thống kê và lâm sàng đáng kể. Tại thời điểm theo dõi trung bình 14.8 tháng, tỷ lệ đáp ứng tổng thể (ORR) là 95% (95% CI 92-97) cho nhóm epcoritamab cộng với R2 so với 79% (95% CI 74-84) cho nhóm đối chứng R2 (p<0.0001). Tỷ lệ đáp ứng cao này cho thấy việc thêm epcoritamab có thể vượt qua các cơ chế kháng thuốc phổ biến trong bệnh bạch cầu tế bào phôi phục hồi hoặc kháng thuốc.
Quan trọng hơn, dữ liệu thời gian sống không tiến triển tiết lộ lợi ích đáng kể. Tỷ lệ nguy cơ (HR) cho tiến triển hoặc tử vong là 0.21 (95% CI 0.14-0.31, p<0.0001), cho thấy sự kết hợp epcoritamab giảm nguy cơ tiến triển bệnh gần 80%. Tỷ lệ PFS dự kiến sau 16 tháng là 85.5% trong nhóm epcoritamab-R2 so với chỉ 40.2% trong nhóm R2. Những kết quả này đặc biệt đáng chú ý khi nhóm đối chứng (R2) hoạt động nhất quán với các chuẩn mực lịch sử, làm nổi bật hiệu quả của liệu pháp ba thuốc thử nghiệm.
Phân Tích An Toàn: Quản Lý Hồ Sơ Miễn Dịch
Như mong đợi khi thêm một liệu pháp miễn dịch mạnh vào một liệu pháp hiện có, tỷ lệ xảy ra sự cố bất lợi (AEs) cao hơn ở nhóm epcoritamab cộng với R2. Các sự cố bất lợi cấp độ 3 hoặc cao hơn xảy ra ở 90% người tham gia nhận sự kết hợp ba thuốc, so với 68% ở nhóm R2. Các sự cố bất lợi cấp độ cao phổ biến nhất là huyết học, bao gồm trung bạch cầu giảm, phù hợp với hồ sơ an toàn đã biết của lenalidomide.
Một điểm tập trung chính đối với các kháng thể song đặc hiệu là tỷ lệ và mức độ nghiêm trọng của hội chứng giải phóng cytokine (CRS). Trong thử nghiệm EPCORE FL-1, CRS xảy ra ở 26% bệnh nhân trong nhóm epcoritamab-R2. Quan trọng nhất, tất cả các sự cố CRS đều là nhẹ (21% cấp độ 1 và 5% cấp độ 2), và không có sự cố CRS cấp độ 3 hoặc cao hơn được báo cáo. Tất cả các trường hợp đều có thể quản lý và được giải quyết bằng các quy trình tiêu chuẩn, bao gồm việc sử dụng tocilizumab và corticosteroids khi cần thiết. Tỷ lệ thấp của CRS nghiêm trọng và cách quản lý dưới da cho thấy liệu pháp này có thể khả thi cho sử dụng lâm sàng rộng rãi bên ngoài các trung tâm ghép tủy lớn.
Nhận Định Lâm Sàng và Ý Kiến Chuyên Gia
Kết quả của EPCORE FL-1 đại diện cho một cột mốc quan trọng trong điều trị bệnh bạch cầu tế bào phôi. Bằng cách đạt được tỷ lệ nguy cơ 0.21 trong một thử nghiệm giai đoạn 3, sự kết hợp epcoritamab cộng với R2 đã đặt ra một chuẩn mực hiệu quả mới cho liệu pháp thứ hai và sau đó. Kết quả cho thấy việc tích hợp sớm các liệu pháp tham gia T-cells có thể cung cấp những đợt thuyên giảm sâu và bền vững mà trước đây khó đạt được mà không cần hóa chất cường độ cao hoặc ghép tế bào gốc tự thân.
Các chuyên gia trong lĩnh vực này lưu ý rằng tỷ lệ đáp ứng cao và lợi ích PFS được quan sát trong thử nghiệm này có thể thách thức trình tự điều trị hiện tại. Mặc dù liệu pháp CAR-T cung cấp hiệu quả cao, chúng thường được dự trữ cho các đợt điều trị sau do các vấn đề về hậu cần và độc tính. Epcoritamab-R2 cung cấp một lựa chọn thay thế hiệu quả, sẵn sàng sử dụng có thể được quản lý sớm hơn trong quá trình bệnh, có thể cải thiện triển vọng dài hạn cho bệnh nhân có các đặc điểm rủi ro cao như POD24.
Tuy nhiên, các bác sĩ phải luôn cảnh giác trong việc quản lý các độc tính tích lũy và tăng nguy cơ nhiễm trùng liên quan đến sự suy giảm B-cells kéo dài. Cách tiếp cận 12 chu kỳ cố định được sử dụng trong thử nghiệm này là một yếu tố thiết kế quan trọng, vì nó cố gắng cân bằng lợi ích điều trị tối đa với nhu cầu về các khoảng thời gian không điều trị và phục hồi miễn dịch.
Kết Luận
Thử nghiệm EPCORE FL-1 cung cấp bằng chứng vững chắc rằng sự kết hợp epcoritamab cộng với R2 vượt trội hơn R2 đơn thuần ở bệnh nhân mắc bệnh bạch cầu tế bào phôi phục hồi hoặc kháng thuốc. Sự kết hợp này cung cấp một lựa chọn hiệu quả, không sử dụng hóa chất, kéo dài đáng kể thời gian sống không tiến triển trong khi duy trì hồ sơ an toàn có thể quản lý. Những kết quả này đặt vị trí epcoritamab cộng với R2 là chuẩn mực điều trị mới cho liệu pháp thứ hai hoặc sau đó của bệnh bạch cầu tế bào phôi, có thể biến đổi việc quản lý bệnh ác tính mãn tính và tái phát này.
Quỹ Tài Trợ và Thông Tin Thử Nghiệm Lâm Sàng
Thử nghiệm EPCORE FL-1 được tài trợ bởi AbbVie và Genmab. Nghiên cứu đã đăng ký với ClinicalTrials.gov (NCT05409066) và EudraCT (2021-000169-34). Thử nghiệm đang diễn ra, mặc dù đã đóng cửa tuyển chọn.
Tài Liệu Tham Khảo
Falchi L, Nijland M, Huang H, et al. Epcoritamab, lenalidomide, and rituximab versus lenalidomide and rituximab for relapsed or refractory follicular lymphoma (EPCORE FL-1): a global, open-label, randomised, phase 3 trial. Lancet. 2026;407(10524):161-173. doi:10.1016/S0140-6736(25)02360-8.
Leonard JP, Trneny M, Izutsu K, et al. AUGMENT: A Phase III Study of Lenalidomide Plus Rituximab Versus Placebo Plus Rituximab in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol. 2019;37(14):1188-1199.