Những Điểm Chính
– Một nghiên cứu phụ CT với 100 bệnh nhân của thử nghiệm giai đoạn 3 ASPEN đã phát hiện ra rằng brensocatib uống (25 mg) đã giảm điểm số phụ tắc nghẽn đờm và tăng tỷ lệ mô phổi khỏe mạnh sau 52 tuần so với giả dược (giá trị P danh nghĩa là .0084 và .0154).
– Trên các đo lường đường hô hấp định lượng được hỗ trợ bởi AI (LungQ-BA), liều 25 mg liên quan đến ít cặp động mạch-đường thở hơn (P = .0499); liều 10 mg cho thấy đường kính ngoại vi của đường thở nhỏ hơn đáng kể so với giả dược.
– Kết quả này mang tính gợi ý: kích thước mẫu nhỏ, nhiều so sánh và chấm điểm bán định lượng hạn chế việc đưa ra các tuyên bố quyết định rằng brensocatib có khả năng điều chỉnh bệnh, nhưng các tín hiệu hình ảnh bổ sung cho lợi ích lâm sàng được quan sát trong thử nghiệm chính ASPEN.
Nền Tảng và Yêu Cầu Chưa Đáp Ứng
Bệnh phế quản phì đại không phải xơ nang (NCFB) là một bệnh đường hô hấp mãn tính đặc trưng bởi viêm trung bạch cầu trung tính kéo dài, các đợt bùng phát nhiễm trùng tái phát, giãn đường thở, giữ đờm và tổn thương phổi tiến triển. Các đợt bùng phát gây ra bệnh tật, làm tăng tốc độ suy giảm chức năng phổi và tăng sử dụng dịch vụ y tế. Các lựa chọn điều trị để giảm tần suất bùng phát là hạn chế, và các phương pháp điều trị thực sự điều chỉnh bệnh để làm chậm tiến trình cấu trúc còn thiếu.
Brensocatib (Brinsupri), một chất ức chế DPP-1 uống, nhắm vào hoạt hóa thượng nguồn của các enzym protease trung bạch cầu serine (bao gồm elastase trung bạch cầu, proteinase 3 và cathepsin G) và được phát triển để giảm tổn thương đường thở do trung bạch cầu gây ra. Vào tháng 4 năm 2025, thử nghiệm giai đoạn 3 ASPEN đã báo cáo rằng brensocatib uống một lần mỗi ngày đã giảm nguy cơ bùng phát, kéo dài thời gian đến đợt bùng phát đầu tiên và tăng khả năng duy trì không bùng phát trong một năm. Vào tháng 8 năm 2025, FDA đã phê duyệt brensocatib (liều uống 10 mg và 25 mg) cho người lớn và thanh thiếu niên từ 12 tuổi trở lên mắc NCFB đáp ứng các tiêu chí dựa trên nhãn.
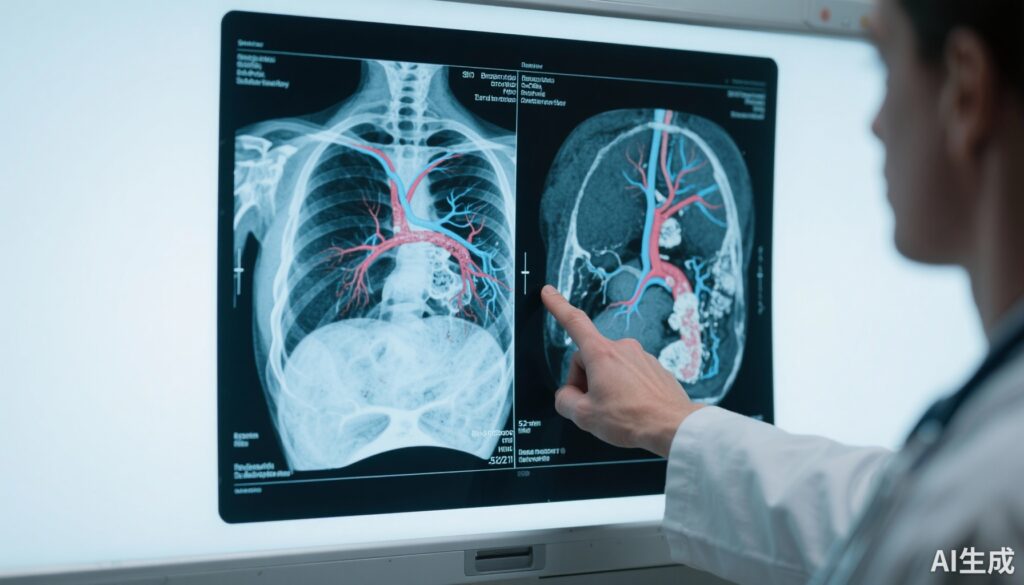
Thiết Kế Nghiên Cứu: Nghiên Cứu Phụ CT của Thử Nghiệm ASPEN
Các nhà nghiên cứu đã thực hiện một nghiên cứu phụ hình ảnh trong chương trình lớn hơn ASPEN giai đoạn 3 để đánh giá xem brensocatib có ảnh hưởng đến bệnh lý cấu trúc phổi trong 52 tuần hay không. Nghiên cứu phụ đã phân tích các bản quét CT ghép đôi từ 100 người tham gia thử nghiệm được random hóa trong ASPEN: 37 người nhận brensocatib 10 mg hàng ngày, 24 người nhận 25 mg hàng ngày và 39 người nhận giả dược.
Các bản quét CT được chấm điểm ở thời điểm cơ sở và sau 52 tuần bằng hai cách tiếp cận bổ sung: kỹ thuật chấm điểm bệnh phế quản phì đại cho CT (BEST-CT), một công cụ chấm điểm trực quan bán định lượng được phát triển và xác minh trong các đăng ký bệnh phế quản phì đại, và LungQ-BA, một nền tảng định lượng được hỗ trợ bởi AI trích xuất các chỉ số đường thở (ví dụ, các cặp động mạch-đường thở và đường kính đường thở). Phân tích chính so sánh sự thay đổi trong nhóm tại 52 tuần và sự khác biệt giữa các nhóm so với giả dược. Nghiên cứu phụ đã được trình bày tại Hội nghị Hàng năm CHEST 2025 bởi James D. Chalmers et al.
Các Phát Hiện Chính
Tổng thể, các phân tích đã chứng minh sự khác biệt hình ảnh vừa phải nhưng có ý nghĩa thống kê thuận lợi cho brensocatib—đặc biệt nhất là liều 25 mg—trong các chỉ số liên quan đến đờm và một số chỉ số đường thở sau 52 tuần.
Tắc Nghẽn Đờm và Thay Đổi Mô Phổi (BEST-CT)
– Nhóm 25 mg đã cho thấy sự giảm đáng kể điểm số phụ BEST-CT cho bệnh phế quản phì đại với tắc nghẽn đờm và tắc nghẽn đờm tổng thể so với giả dược (P = .0084 và P = .0154, tương ứng).
– Bệnh nhân nhận 25 mg cũng có sự tăng tỷ lệ mô phổi “khỏe mạnh” lớn hơn sau 52 tuần so với giả dược.
Các Chỉ Số Đường Hô Hấp (LungQ-BA)
– Trên LungQ-BA, bệnh nhân được random hóa vào liều 25 mg đã có ít cặp động mạch-đường thở hơn đáng kể sau 52 tuần so với giả dược (P = .0499). Ít cặp động mạch-đường thở có thể phản ánh sự giảm dày thành đường thở hoặc các đặc điểm tái tạo đường thở khác được bắt bởi nền tảng.
– Nhóm 10 mg cho thấy các biện pháp đường kính ngoại vi của đường thở nhỏ hơn đáng kể so với giả dược sau 52 tuần, cho thấy tín hiệu độc lập về liều cho một số thay đổi đường kính đường thở.
Mối Liên Quan Lâm Sàng
Các kết quả hình ảnh này phù hợp với các kết quả lâm sàng được báo cáo trong chương trình chính ASPEN: ít bùng phát hơn, thời gian đến đợt bùng phát đầu tiên bị kéo dài và suy giảm chức năng phổi chậm hơn với brensocatib—đặc biệt là liều 25 mg. Các nhà nghiên cứu và các chuyên gia độc lập đã giải thích các tín hiệu hình ảnh là phù hợp với tác động sinh học có thể giải thích được của việc ức chế DPP-1 đối với việc loại bỏ đờm và viêm đường thở.
An Toàn và Cân Nhắc Liều Dùng
Chương trình ASPEN đã xác lập hồ sơ an toàn tổng thể hỗ trợ việc phê duyệt brensocatib 10 mg và 25 mg của FDA. Trong nghiên cứu phụ hình ảnh, không có tín hiệu an toàn mới được báo cáo liên quan đến các phát hiện CT. Dựa trên dữ liệu lâm sàng và hình ảnh kết hợp, một số nhà nghiên cứu ưu tiên liều 25 mg làm liều đầu tiên cho bệnh nhân có nguy cơ tiến triển cao hơn hoặc những người có tắc nghẽn đờm rõ rệt, trong khi công nhận rằng nhãn cho phép cả hai liều.
Lý Do Cơ Chế
Việc ức chế DPP-1 giảm quá trình trưởng thành của các enzym protease trung bạch cầu serine trong tủy xương, do đó giảm gánh nặng của các enzym protease hoạt hóa được chuyển đến đường thở trong quá trình viêm trung bạch cầu. Elastase trung bạch cầu và các enzym liên quan đóng góp vào tăng tiết đờm, giảm khả năng loại bỏ đờm niêm mạc, tổn thương thành đường thở và giãn đường thở tiến triển. Sự giảm tắc nghẽn đờm được quan sát cung cấp một cây cầu cơ chế: giảm hoạt động của protease trung bạch cầu có thể giảm sản xuất/độ dai của đờm và viêm thành đường thở, cho phép cải thiện có thể phát hiện trên CT trong 12 tháng.
Bình Luận và Giải Thích của Chuyên Gia
Các chuyên gia độc lập tại CHEST và trong các cuộc phỏng vấn sau đó đã nhấn mạnh rằng sự thay đổi cấu trúc trên CT trong một năm là không phổ biến trong bệnh phế quản phì đại vì bệnh thường tiến triển chậm. Việc nghiên cứu phụ phát hiện sự giảm tắc nghẽn đờm và thay đổi nhỏ đường thở là đáng chú ý, nhưng có một số điểm cần thận trọng:
- Nghiên cứu phụ đã tuyển 100 bệnh nhân, một phần nhỏ của nhóm ASPEN (>1,700 tổng cộng), hạn chế sức mạnh và khả năng áp dụng rộng rãi.
- Nhiều điểm cuối và so sánh đã được kiểm tra, và các giá trị P được báo cáo là danh nghĩa (không điều chỉnh cho nhiều so sánh), tăng nguy cơ lỗi loại I.
- BEST-CT là bán định lượng và phụ thuộc vào người đọc; mặc dù đã được xác minh trong công việc đăng ký, chấm điểm trực quan giới thiệu sự biến đổi. Việc thêm LungQ-BA (các chỉ số dựa trên AI) giảm thiểu nhưng không loại bỏ sự không chắc chắn trong đo lường.
Vì vậy, các chuyên gia mô tả các phát hiện là mang tính gợi ý thay vì bằng chứng quyết định về việc điều chỉnh bệnh. Họ vẫn coi kết quả này có ý nghĩa lâm sàng trong bối cảnh các lợi ích triệu chứng và bùng phát được quan sát trong ASPEN, và khẳng định rằng lợi ích mong đợi mạnh nhất sẽ là ở bệnh nhân có bệnh viêm trung bạch cầu chiếm ưu thế và bùng phát thường xuyên bất chấp các chiến lược làm sạch đường thở và kháng sinh theo chuẩn.
Hạn Chế
Các hạn chế chính bao gồm: kích thước mẫu nhỏ của nghiên cứu phụ so với thử nghiệm chính; giá trị P danh nghĩa không điều chỉnh cho nhiều so sánh; khả năng biến đổi của người đọc trong chấm điểm bán định lượng; và khoảng theo dõi 52 tuần, có thể ngắn để phát hiện thay đổi cấu trúc ở nhiều bệnh nhân. Việc tài trợ và đóng góp của nhà sản xuất, Insmed, đã được tiết lộ và một số nhà nghiên cứu đã báo cáo mối quan hệ tư vấn hoặc cấp vốn với Insmed, nên xem xét khi diễn giải.
Sự Ảnh Hưởng Lâm Sàng và Hướng Dẫn Thực Tế
Đối với các bác sĩ điều trị NCFB, tổng thể dữ liệu ASPEN cộng với nghiên cứu phụ CT này hỗ trợ việc xem xét brensocatib (đặc biệt là liều 25 mg) cho người lớn và thanh thiếu niên có bùng phát thường xuyên hoặc suy giảm chức năng phổi tiến triển bất chấp các chiến lược làm sạch đường thở và kháng sinh theo chuẩn. Bệnh nhân có tắc nghẽn đờm rõ rệt trên CT hoặc có nguy cơ tiến triển cao có thể được ưu tiên. Các cân nhắc thực tế bao gồm chi phí, bảo hiểm thanh toán và tuân thủ lâu dài sẽ ảnh hưởng đến việc sử dụng. Quyết định chung nên cân nhắc lịch sử bùng phát cá nhân, biểu hiện (viêm trung bạch cầu), bệnh kèm theo và sở thích của bệnh nhân.
Hướng Nghiên Cứu và Chính Sách
Để xác nhận và lượng hóa các lợi ích cấu trúc, lĩnh vực cần các nhóm hình ảnh lớn hơn, được lập kế hoạch trước hoặc bao gồm các điểm cuối hình ảnh trên toàn bộ dân số thử nghiệm với các điểm cuối được xác định trước và kiểm soát đa dạng. Theo dõi lâu hơn (>1 năm), phân tích nhóm dựa trên biểu hiện và các sổ đăng ký thực tế đánh giá an toàn, tuân thủ, hiệu quả chi phí và các kết quả cấu trúc dài hạn sẽ quan trọng. Chuẩn hóa thu thập và chấm điểm CT—hoặc sử dụng rộng rãi các nền tảng phân tích được xác minh dựa trên AI—sẽ cải thiện tính lặp lại giữa các nghiên cứu.
Kết Luận
Nghiên cứu phụ CT từ chương trình ASPEN cung cấp bằng chứng hình ảnh đầu tiên cho thấy brensocatib có thể giảm tắc nghẽn đờm và tạo ra cải thiện vừa phải trong các chỉ số đường thở và mô phổi khỏe mạnh trong 52 tuần, với liều 25 mg cho thấy tín hiệu nhất quán nhất. Dữ liệu này bổ sung cho việc giảm bùng phát lâm sàng và suy giảm chức năng phổi chậm hơn được báo cáo trong thử nghiệm chính và cung cấp hỗ trợ sinh học có thể giải thích được rằng việc ức chế DPP-1 có thể ảnh hưởng đến sinh học bệnh lý của NCFB. Với tính chất khám phá của nghiên cứu và các hạn chế, kết quả hình ảnh nên được xem xét là mang tính gợi ý. Các nghiên cứu hình ảnh lớn hơn, được xác định trước và theo dõi lâu hơn là cần thiết để xác định xem brensocatib có thực sự điều chỉnh bệnh hay không và xác định nhóm bệnh nhân nào có lợi ích cấu trúc lớn nhất.
Tài Trợ và clinicaltrials.gov
Nghiên cứu phụ và thử nghiệm chính ASPEN được hỗ trợ bởi Insmed. Các nhà nghiên cứu đã tiết lộ mối quan hệ tư vấn và cấp vốn với Insmed khi có liên quan. Thử nghiệm giai đoạn 3 ASPEN được tham chiếu trong bài công bố chính: Chalmers JD et al., N Engl J Med. 2025;392(16):1569–1581 (DOI: 10.1056/NEJMoa2411664).
Tham Khảo
1. Chalmers JD, Burgel PR, Daley CL, De Soyza A, Haworth CS, Mauger D, Loebinger MR, McShane PJ, Ringshausen FC, Blasi F, Shteinberg M, Mange K, Teper A, Fernandez C, Zambrano M, Fan C, Zhang X, Metersky ML; ASPEN Investigators. Phase 3 Trial of the DPP-1 Inhibitor Brensocatib in Bronchiectasis. N Engl J Med. 2025 Apr 24;392(16):1569–1581. doi: 10.1056/NEJMoa2411664. PMID: 40267423.
2. Thông cáo báo chí của nhà sản xuất: Insmed thông báo FDA phê duyệt brensocatib (Brinsupri) cho bệnh phế quản phì đại không phải xơ nang, tháng 8 năm 2025.
3. Bài trình bày: Chalmers JD. Hiệu ứng của Brensocatib trên cấu trúc phổi: Nghiên cứu phụ CT của ASPEN. Hội nghị Hàng năm American College of Chest Physicians (CHEST) 2025.