Tổng Quan
- Bexotegrast, một chất ức chế kép bằng đường uống của integrin β1 và β6, đã được dung nạp tốt ở bệnh nhân IPF trong 12 tuần.
- So với giả dược, việc điều trị bằng bexotegrast liên quan đến việc giảm sự suy giảm dung tích sống cưỡng bức (FVC), cho thấy hiệu quả chống xơ hóa tiềm năng.
- Hình ảnh xơ phổi định lượng (QLF) và các dấu sinh học lưu thông ITGB6 và PRO-C3 cho thấy cải thiện phụ thuộc liều với bexotegrast.
- Đặc điểm an toàn của thuốc hỗ trợ các thử nghiệm dài hạn tiếp theo để xác lập tính bền vững của lợi ích.
Nền Tảng
Xơ phổi tự phát (IPF) là một rối loạn phổi tiến triển, gây tử vong, đặc trưng bởi xơ hóa quá mức làm suy giảm chức năng hô hấp, biểu hiện bằng ho và khó thở ngày càng nặng. Thời gian sống trung bình không điều trị là 3 đến 4 năm. Các liệu pháp được chấp thuận hiện tại—pirfenidone và nintedanib—chậm nhưng không ngăn chặn sự tiến triển của bệnh và thường gặp các vấn đề về dung nạp như tác dụng phụ tiêu hóa. Do đó, vẫn còn một nhu cầu cấp bách chưa được đáp ứng đối với các liệu pháp an toàn và hiệu quả hơn.
Kích hoạt yếu tố tăng trưởng biến đổi beta (TGF-β), một động lực chính của xơ hóa, xảy ra thông qua integrin β1 và β6, được tăng cường trong phổi IPF. Nhắm mục tiêu vào các integrin này để chặn kích hoạt TGF-β tại chỗ đại diện cho một chiến lược chống xơ hóa mới. Bexotegrast (PLN-74809) là một phân tử nhỏ, dùng hàng ngày bằng đường uống, ức chế chọn lọc các integrin này, ngăn chặn chuỗi phản ứng xơ hóa do TGF-β khởi xướng.
Thiết Kế Nghiên Cứu
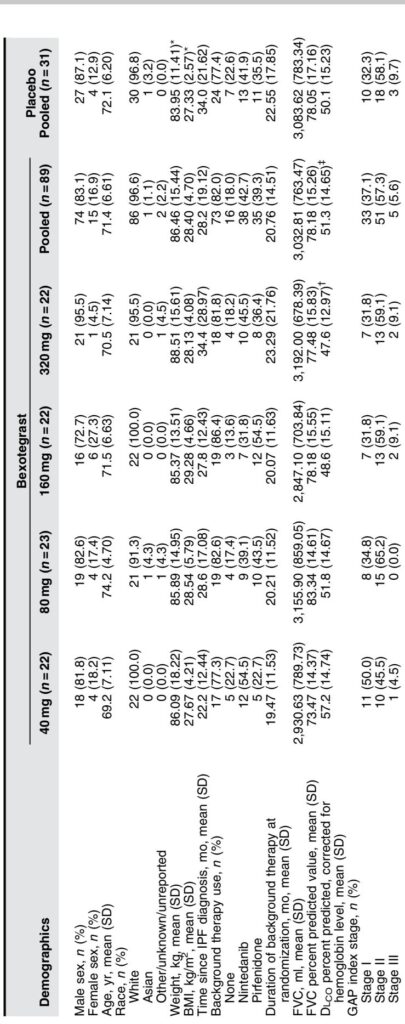
Thử nghiệm INTEGRIS-IPF (NCT04396756) là một nghiên cứu giai đoạn 2a, ngẫu nhiên, mù đôi, kiểm soát bằng giả dược, đánh giá liều lượng, được thực hiện tại 39 địa điểm quốc tế. Tổng cộng 119 người tham gia, chủ yếu ở độ tuổi 70, có IPF được xác nhận, được phân ngẫu nhiên 3:1 để nhận bexotegrast đường uống hàng ngày với liều 40 mg, 80 mg, 160 mg hoặc 320 mg hoặc giả dược trong ít nhất 12 tuần. Các liệu pháp nền IPF (pirfenidone hoặc nintedanib) được phép nếu ổn định trong hơn 3 tháng trước khi đăng ký; khoảng 80% người tham gia đang sử dụng liệu pháp nền.
Điểm cuối chính tập trung vào an toàn, cụ thể là tần suất các sự cố bất lợi xuất hiện do điều trị (TEAEs). Các điểm cuối hiệu quả试探 bao gồm sự thay đổi từ cơ bản đến tuần 12 trong dung tích sống cưỡng bức (FVC), mức độ xơ phổi định lượng được đánh giá bằng chụp cắt lớp vi tính độ phân giải cao (HRCT), và các dấu sinh học liên quan đến xơ hóa bao gồm integrin beta-6 (ITGB6) và neopeptide tổng hợp collagen loại III (PRO-C3).
Kết Quả Chính
An Toàn và Dung Nạp: Bexotegrast được dung nạp tốt ở tất cả các liều, không có sự tăng TEAEs phụ thuộc liều. Tần suất tổng thể của TEAEs giữa nhóm bexotegrast (69.7%) và nhóm giả dược (67.7%) tương đương. Sự cố bất lợi phổ biến nhất là tiêu chảy, chủ yếu xảy ra ở những người tham gia cũng đang sử dụng nintedanib, phù hợp với tác dụng đã biết của thuốc đó. Không có sự cố bất lợi nghiêm trọng hoặc tử vong liên quan đến điều trị được báo cáo. Đánh giá phòng thí nghiệm, dấu hiệu sống và ECG không cho thấy tín hiệu an toàn.
Dược động học: Tiếp xúc với bexotegrast tăng tỷ lệ gần đúng với liều, hỗ trợ dược động học dự đoán được.
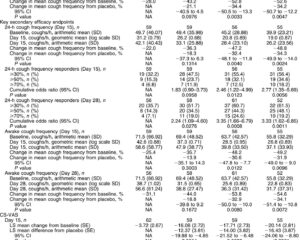
Hiệu Quả: Trong dân số điều trị theo ý định đã sửa đổi (với hơn 80% đang sử dụng liệu pháp nền), bexotegrast đã giảm đáng kể sự suy giảm FVC so với giả dược ở liều 80 mg và 320 mg sau 12 tuần. Nhóm giả dược trải qua sự suy giảm FVC trung bình là -110.5 ml, trong khi các nhóm bexotegrast cho thấy sự suy giảm nhỏ hơn hoặc cải thiện nhẹ (ví dụ, +29.4 ml với liều 320 mg). Sự giảm này trong mất chức năng phổi đã được quan sát bất kể việc sử dụng liệu pháp nền.
Sự giảm phụ thuộc liều cũng được thấy trong tỷ lệ người tham gia trải qua sự suy giảm tương đối hoặc tuyệt đối 10% FVC dự kiến. HRCT dựa trên mức độ xơ phổi định lượng cho thấy sự ổn định hoặc tiến triển hạn chế ở liều 160 mg và 320 mg so với giả dược. Phân tích dấu sinh học cho thấy sự giảm phụ thuộc liều trong mức ITGB6 và PRO-C3 trong huyết tương, cả hai đều liên quan đến quá trình xơ hóa và dự đoán sự tiến triển của bệnh.
Trong nhóm mở rộng, đa số (88.9%) bệnh nhân dùng liều 320 mg có cải thiện FVC sau 12 tuần duy trì nó sau 24 tuần, không giống như những người nhận giả dược.
Bình Luận Chuyên Gia
Thử nghiệm INTEGRIS-IPF cung cấp bằng chứng lâm sàng hứa hẹn sớm cho thấy bexotegrast có thể ức chế an toàn kích hoạt TGF-β do integrin và giảm sự tiến triển xơ hóa trong IPF. Khác với các kháng thể chặn integrin trước đây gây lo ngại về tăng nguy cơ bùng phát cấp tính, bexotegrast không liên quan đến các tín hiệu an toàn như vậy, có thể phản ánh sự khác biệt về dạng thuốc và dược động học.
Việc bao gồm người tham gia đang sử dụng liệu pháp chống xơ hóa nền ổn định trong nghiên cứu phản ánh thực hành lâm sàng thực tế, và kết quả cho thấy bexotegrast có thể mang lại lợi ích bổ sung mà không có thêm độc tính. Tuy nhiên, thời gian ngắn (12 tuần) và quy mô mẫu vừa phải của nghiên cứu hạn chế kết luận chắc chắn về hiệu quả lâu dài và tác động đến sự sống còn. Sự thay đổi FVC biến đổi được quan sát nhấn mạnh sự biến thiên đo lường cố hữu trong thử nghiệm chức năng phổi ngắn hạn.
Dữ liệu dấu sinh học và hình ảnh củng cố khả năng sinh học của hành động chống xơ hóa của bexotegrast. Sự giảm ITGB6 phù hợp với việc chặn các integrin nhắm mục tiêu, và sự thay đổi PRO-C3 phản ánh sự điều chỉnh chu trình collagen.
Các thử nghiệm lớn hơn và dài hơn trong tương lai, chẳng hạn như thử nghiệm BEACON-IPF kéo dài 52 tuần đang diễn ra, là cần thiết để xác nhận lợi ích bền vững và xác định các điểm cuối lâm sàng bao gồm tỷ lệ tử vong, chất lượng cuộc sống và tần suất bùng phát. Việc tuyển dụng nên cố gắng đa dạng hóa dân tộc để tăng cường khả năng tổng quát.
Kết Luận
Bexotegrast cho thấy đặc điểm an toàn thuận lợi và những dấu hiệu khích lệ về hiệu quả trong việc giảm sự suy giảm chức năng phổi và sự tiến triển xơ hóa ở bệnh nhân xơ phổi tự phát. Bằng cách nhắm mục tiêu vào các integrin quan trọng để ức chế kích hoạt TGF-β, bexotegrast cung cấp một cơ chế mới có thể bổ sung cho các liệu pháp chống xơ hóa hiện có. Các nghiên cứu giai đoạn 3 đang diễn ra và trong tương lai sẽ là then chốt để xác định vai trò của nó trong thực hành lâm sàng và tiềm năng cải thiện kết quả trong bệnh này.
Tham Khảo
Lancaster L, Cottin V, Ramaswamy M, Wuyts WA, Jenkins RG, Scholand MB, Kreuter M, Valenzuela C, Ryerson CJ, Goldin J, Kim GHJ, Jurek M, Decaris M, Clark A, Turner S, Barnes CN, Achneck HE, Cosgrove GP, Lefebvre c9A, Flaherty KR; PLN-74809-IPF-202 Trial Investigators. Bexotegrast in Patients with Idiopathic Pulmonary Fibrosis: The INTEGRIS-IPF Clinical Trial. Am J Respir Crit Care Med. 2024 Aug 15;210(4):424-434. doi: 10.1164/rccm.202403-0636OC.