Những Điểm Chính
– Trong HFrEF, sự giảm nhanh chóng của tốc độ lọc cầu thận ước tính (eGFR) có thể được phát hiện lên đến 12 tháng trước khi nhập viện hoặc tử vong do suy tim (HF).
– Bệnh nhân gặp sự kiện HF có xu hướng eGFR trước sự kiện khoảng -4 đến -6 mL/phút/1.73 m²/năm so với khoảng -1 đến -1.4 mL/phút/1.73 m²/năm ở những bệnh nhân không gặp sự kiện trong các nhóm thử nghiệm và thực tế.
– eGFR tiếp tục giảm trong năm sau sự kiện HF nhưng với tốc độ chậm hơn, liên kết sự suy giảm thận trước sự kiện với tình trạng tắc nghẽn triệu chứng và hậu quả bất lợi.
– Xu hướng eGFR theo thời gian (xu hướng) có thể xác định bệnh nhân có nguy cơ cao sớm hơn so với sự thay đổi dựa trên ngưỡng đơn lẻ và có thể hỗ trợ tăng cường điều trị giảm tắc nghẽn, theo dõi, và quyết định điều trị.
Nền Tảng: Tại Sao Xu Hướng Thận Quan Trọng Trong HFrEF
Suy tim với phân suất tống máu giảm (HFrEF) và bệnh thận mạn tính (CKD) thường cùng tồn tại. Sự suy giảm chức năng thận là một dấu hiệu tiên lượng đã được xác định trong HF: eGFR cơ bản thấp hơn và các đợt suy thận nặng hơn đều liên quan đến tỷ lệ mắc bệnh và tử vong cao hơn. Tuy nhiên, hầu hết các khuyến nghị lâm sàng và hướng dẫn tập trung vào các ngưỡng eGFR cắt ngang (ví dụ, khi nào nên điều chỉnh hoặc tránh sử dụng một số loại thuốc) thay vì hành vi eGFR theo thời gian. Hiểu rằng liệu sự suy giảm chức năng thận có tiền phong cho sự suy giảm lâm sàng của HF hay không có thể mở ra cơ hội can thiệp sớm.
Thiết Kế Nghiên Cứu và Đối Tượng
Nghiên cứu của Kobayashi et al. (Eur Heart J. 2025) đã xem xét các xu hướng eGFR cá nhân trước và sau các sự kiện liên quan đến HF bằng dữ liệu từ hai bộ dữ liệu thử nghiệm lâm sàng ngẫu nhiên (EPHESUS và EMPHASIS-HF) và một nhóm HF thực tế (BARCELONA).
– Các nhóm EPHESUS và EMPHASIS-HF (tổng số n=8,587) cung cấp các đo lường creatinin/eGFR lặp đi lặp lại trong khoảng thời gian theo dõi trung bình khoảng 17 tháng.
– Đăng ký BARCELONA (n=2,048) cung cấp theo dõi thực tế dài hạn hơn (trung bình 47 tháng).
Các sự kiện liên quan đến HF được định nghĩa là nhập viện do HF hoặc tử vong do HF. Các nhà nghiên cứu đã mô hình hóa sự thay đổi tuyến tính của eGFR (mL/phút/1.73 m² mỗi năm) trong 12 tháng trước và 12 tháng sau một sự kiện HF, và so sánh các xu hướng giữa những người có và không có sự kiện. Họ cũng khám phá các tương quan lâm sàng như lớp NYHA.
Kết Quả Chính
Tỷ Lệ Sự Kiện và Bối Cảnh Nhóm
Các sự kiện liên quan đến HF xảy ra ở 14.1% bệnh nhân trong các bộ dữ liệu thử nghiệm kết hợp (EPHESUS/EMPHASIS-HF; thời gian theo dõi trung bình 17.1 tháng) và 33.8% bệnh nhân trong BARCELONA (thời gian theo dõi trung bình 47.0 tháng). Những tỷ lệ này phản ánh thời gian theo dõi khác nhau và sự khác biệt giữa dân số thử nghiệm và thực tế.
Xu Hướng eGFR Trước Sự Kiện
Trong cả hai nhóm thử nghiệm và đăng ký, bệnh nhân sau đó gặp sự kiện HF có sự giảm eGFR nhanh hơn đáng kể trong năm trước sự kiện so với những người không gặp sự kiện:
- EPHESUS/EMPHASIS-HF: độ dốc trung bình trước sự kiện -4.83 mL/phút/1.73 m²/năm so với -1.18 mL/phút/1.73 m²/năm ở bệnh nhân không gặp sự kiện HF.
- BARCELONA: độ dốc trung bình trước sự kiện -5.77 mL/phút/1.73 m²/năm so với -1.35 mL/phút/1.73 m²/năm ở bệnh nhân không gặp sự kiện HF.
Những sự khác biệt này có ý nghĩa lâm sàng. Sự giảm khoảng 4–6 mL/phút/1.73 m² trong một năm lớn hơn nhiều so với sự giảm liên quan đến tuổi và có thể là dấu hiệu của các quá trình bệnh lý học liên quan đến sự mất ổn định của HF.

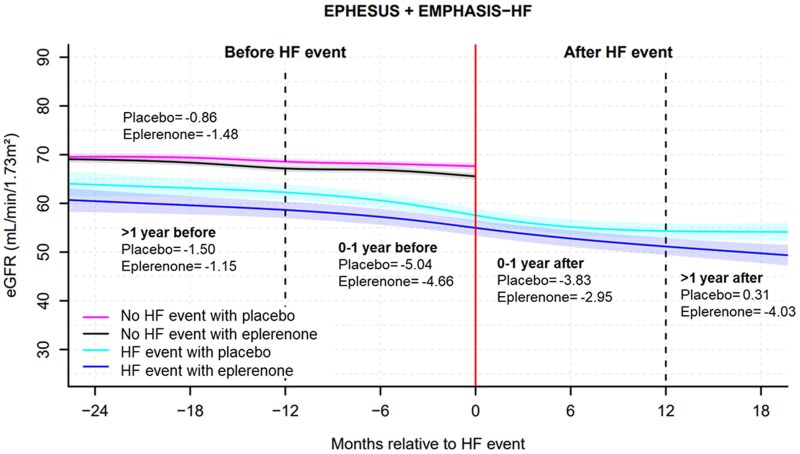
Fig.Estimated glomerular filtration rate trajectory before and after heart failure events from the EPHESUS and EMPHASIS-HF trials. HF, heart failure; eGFR, estimated glomerular filtration rate; CI, confidence interval. Number in the figure presents the estimated rate of eGFR decline per year
Xu Hướng eGFR Sau Sự Kiện
Trong năm sau khi nhập viện hoặc tử vong do HF (khi có thể đo được), eGFR tiếp tục giảm nhưng với tốc độ trung bình chậm hơn so với trước sự kiện: khoảng -3.04 đến -3.45 mL/phút/1.73 m²/năm trong các bộ dữ liệu. Mô hình này cho thấy các quá trình gây ra sự giảm thận trước sự kiện vẫn tiếp diễn sau khi xuất viện nhưng có thể bị giảm bớt phần nào bởi quản lý trong bệnh viện.

Fig.
Fig. New York Heart Association class trajectory before and after heart failure events from the EPHESUS and EMPHASIS-HF trials. HF, heart failure; NYHA, New York Heart Association; CI, confidence interval. Dotted lines indicate 1 year before and after HF events. Number in the figure presents the estimated rate of estimated glomerular filtration rate decline per year
Gánh Nặng Triệu Chứng và Độ Dốc Thận
Lớp NYHA xấu đi song song với sự giảm eGFR nhanh hơn trước sự kiện HF, hỗ trợ mối liên kết lâm sàng giữa tình trạng tắc nghẽn triệu chứng và suy giảm chức năng thận — nhất quán với các tương tác tim-thận do áp lực tĩnh mạch trung tâm và thận cao và lưu lượng máu thận giảm.
Fig. Estimated glomerular filtration rate trajectory before and after heart failure events between eplerenone and placebo groups from the EPHESUS and EMPHASIS-HF trials. HF, heart failure, Number in the figure presents the estimated rate of estimated glomerular filtration rate decline per year in the placebo/eplerenone groups
Giải Đáp và Khả Năng Cơ Chế
Sự phát hiện nhất quán trong các nhóm thử nghiệm ngẫu nhiên và thực tế rằng eGFR giảm đáng kể trong 12 tháng trước khi nhập viện hoặc tử vong do HF hỗ trợ một liên kết thời gian và có thể là cơ chế. Có nhiều giải thích bệnh lý học có thể:
- Tổn thương thận do tắc nghẽn: áp lực tĩnh mạch trung tâm và tĩnh mạch thận cao làm giảm lọc hiệu quả và có thể dẫn đến suy thận tiến triển trước khi mất ổn định rõ ràng.
- Lưu lượng tim thấp và thiếu máu thận: giảm lưu lượng tiến triển góp phần gây tổn thương thận tiến triển.
- Kích hoạt thần kinh nội tiết và viêm: kích hoạt mạn tính của hệ thống renin-angiotensin-aldosteron (RAAS), hệ thống thần kinh giao cảm và các con đường viêm có thể thúc đẩy cả sự suy giảm cấu trúc và chức năng tim và thận.
- Yếu tố điều trị và chẩn đoán: thay đổi liều lợi tiểu, khởi đầu hoặc ngừng sử dụng chất ức chế RAAS, độc tố thận hoặc các bệnh đồng thời có thể tăng tốc sự giảm eGFR và gây ra nhập viện.
Nghiên cứu này củng cố khái niệm về chuỗi tim-thận, nơi suy giảm thận không chỉ là một nhân chứng mà còn là một phần của quá trình tiến triển hướng đến các sự kiện HF.
Ý Nghĩa Lâm Sàng
Một số ý nghĩa thực tế phát sinh từ những phát hiện này:
- Theo dõi độ dốc eGFR, không chỉ các ngưỡng tuyệt đối. Các phép đo lặp đi lặp lại tiết lộ một độ dốc âm tăng tốc trong vài tháng có thể xác định bệnh nhân có nguy cơ cao nhập viện HF ngắn hạn.
- Tích hợp độ dốc eGFR vào các cảnh báo rủi ro và các con đường chăm sóc. Hồ sơ sức khỏe điện tử có thể đánh dấu các bệnh nhân có độ dốc eGFR giảm vượt quá mức giảm liên quan đến tuổi hoặc xu hướng cơ bản cá nhân, thúc đẩy xem xét của bác sĩ.
- Đánh giá tắc nghẽn khi phát hiện sự giảm thận. Vì tắc nghẽn có vẻ liên quan đến sự giảm thận trước sự kiện, các bác sĩ nên đánh giá tình trạng khối lượng và cân nhắc điều chỉnh lợi tiểu ngoại trú sớm hoặc xem xét tuân thủ và xu hướng cân nặng.
- Cẩn thận khi diễn giải sự tăng creatinin sau khi bắt đầu sử dụng chất ức chế RAAS hoặc SGLT2. Một số sự tăng creatinin sớm do thuốc không đòi hỏi ngừng ngay lập tức; bối cảnh lâm sàng và xu hướng quan trọng.
- Cân nhắc chăm sóc đa ngành. Sự hợp tác chặt chẽ hơn giữa các đội ngũ suy tim và thận có thể có lợi cho bệnh nhân có eGFR giảm nhanh.
Hạn Chế và Bất Định
Mặc dù thuyết phục, các phát hiện cần diễn giải cẩn thận:
- Phân tích xu hướng quan sát không thể thiết lập đầy đủ nguyên nhân; mặc dù eGFR giảm trước các sự kiện HF, nó có thể phản ánh bệnh lý học chung hơn là một động lực gây ra.
- Tần suất và thời điểm đo lường khác nhau giữa các thử nghiệm và đăng ký, và các kiểm tra creatinin ngoại trú ít thường xuyên có thể bỏ lỡ các biến động ngắn hạn.
- Các sự tăng creatinin cấp tính liên quan đến các yếu tố tạm thời (ví dụ, nhiễm trùng đồng thời, độc tố thận, mất nước) có thể gây nhiễu độ dốc nếu không được diễn giải lâm sàng.
- Tính tổng quát đối với dân số HFpEF hoặc không HFrEF chưa biết; các nhóm được nghiên cứu là dân số HFrEF.
- Ngưỡng tối ưu cho độ dốc eGFR bất thường (có thể kích hoạt hành động) chưa được xác định và cần xác minh triển vọng.
Các Khoảng Trống Nghiên Cứu và Thực Hành
Các bước tiếp theo quan trọng bao gồm:
- Nghiên cứu xác minh triển vọng để xác định ngưỡng độ dốc eGFR hành động, đánh giá độ nhạy và độ đặc hiệu cho các sự kiện HF sắp tới, và thử nghiệm các chiến lược can thiệp được kích hoạt bởi cảnh báo độ dốc.
- Thử nghiệm ngẫu nhiên về các can thiệp giảm tắc nghẽn sớm hoặc đa ngành được kích hoạt bởi sự giảm eGFR để xác định xem chiến lược này có ngăn ngừa nhập viện HF hay không.
- Tích hợp độ dốc eGFR với các dấu hiệu sinh học khác (peptide natriuretic, cân nặng, bioimpedance) và dữ liệu theo dõi từ xa để xây dựng các mô hình dự đoán mạnh mẽ.
Các Điểm Cần Nhớ Thực Tế cho Bác Sĩ
– Xem xét các giá trị eGFR lặp đi lặp lại trong vài tháng thay vì một kết quả phòng thí nghiệm đơn lẻ. Sự giảm tiến triển vài mL/phút/1.73 m²/năm nên thúc đẩy đánh giá lại tình trạng tắc nghẽn, tuân thủ, thay đổi thuốc, và các yếu tố đồng mắc.
– Khi eGFR giảm, hãy cân nhắc tăng cường xem xét lâm sàng (điện thoại, thăm khám) và đánh giá tắc nghẽn khách quan thay vì ngừng ngay lập tức điều trị HF theo hướng dẫn.
– Sử dụng đầu vào đa ngành sớm cho bệnh nhân có eGFR giảm nhanh, và cân nhắc tư vấn thận khi các xu hướng dốc hoặc khi nghi ngờ có các tổn thương thận thêm.
Kết Luận
Nghiên cứu của Kobayashi et al. cho thấy rằng trong HFrEF, sự suy giảm chức năng thận có ý nghĩa lâm sàng thường tiền phong cho nhập viện hoặc tử vong do HF liên quan đến HF lên đến một năm, và eGFR tiếp tục giảm sau các sự kiện này. Các xu hướng eGFR lặp đi lặp lại cung cấp thông tin tiên lượng có thể hành động bổ sung cho các đánh giá hiện có về triệu chứng và peptide natriuretic. Tích hợp theo dõi dựa trên độ dốc vào chăm sóc thường quy — được hỗ trợ bởi xác minh triển vọng và các con đường chăm sóc tích hợp — có thể cho phép xác định sớm hơn các bệnh nhân có nguy cơ mất ổn định và cho phép can thiệp kịp thời, mục tiêu.
Tài Trợ và clinicaltrials.gov
Tham khảo xuất bản gốc để biết nguồn tài trợ chi tiết và đăng ký thử nghiệm cho EPHESUS và EMPHASIS-HF.
Tham Khảo
1. Kobayashi M, Bayes-Genis A, Duarte K, McMurray JJV, Ferreira JP, Pocock SJ, Van Veldhuisen DJ, Lupón J, Pitt B, Zannad F, Girerd N. Kidney function trajectories before and after hospitalization for heart failure with reduced ejection fraction. Eur Heart J. 2025 Nov 14;46(43):4583-4593. doi: 10.1093/eurheartj/ehaf457 IF: 35.6 Q1 .
2. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599–3726.
3. McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2019;381:1995-2008.
4. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl. 2013;3(1):1–150.