Nổi bật
- Nghiên cứu ngẫu nhiên hoán vị BRADiNP đã đánh giá fulmetibant trong đau thần kinh do đái tháo đường (DNP), cho thấy không có lợi ích giảm đau đáng kể so với giả dược.
- Mặc dù hứa hẹn trong các mô hình tiền lâm sàng, liều 450 mg mỗi ngày một lần của fulmetibant không giảm đáng kể mức độ đau trung bình trong 24 giờ ở bệnh nhân bị đau thần kinh cảm giác vận động đối xứng xa.
- Các sự cố bất lợi chủ yếu là nhẹ hoặc vừa phải, xảy ra ở 41,8% bệnh nhân dùng fulmetibant so với 32,9% dùng giả dược, chỉ ra một hồ sơ an toàn có thể quản lý được.
- Nghiên cứu nhấn mạnh nhu cầu chưa đáp ứng về các liệu pháp hiệu quả trong việc điều trị DNP và những thách thức trong việc chuyển đổi các mục tiêu phân tử thành các liệu pháp lâm sàng.
Nền tảng nghiên cứu và gánh nặng bệnh tật
Đau thần kinh do đái tháo đường (DNP) là một biến chứng phổ biến và gây tàn phế, ảnh hưởng đến khoảng 50% bệnh nhân mắc đái tháo đường kéo dài, bao gồm cả đái tháo đường tuýp 1 và tuýp 2. DNP được đặc trưng bởi đau thần kinh cảm giác vận động đối xứng xa, gây đau rát, đau nhói và đau như điện giật chủ yếu ở chi dưới. Đau mãn tính này làm giảm đáng kể chất lượng cuộc sống, góp phần vào rối loạn giấc ngủ và thách thức việc quản lý hiệu quả. Các liệu pháp dược lý hiện tại—bao gồm chống co giật, chống trầm cảm và opioid—thường cung cấp sự giảm đau không đủ và thường đi kèm với tác dụng phụ đáng kể.
Bradykinin, một peptit gây viêm, có liên quan đến các con đường đau thần kinh thông qua tác động lên thụ thể bradykinin-1 (B1R), được tăng biểu hiện trong viêm mãn tính và tổn thương dây thần kinh. Các mô hình tiền lâm sàng đã chứng minh rằng việc đối kháng B1R có thể làm giảm đau thần kinh, định vị fulmetibant, một chất đối kháng B1R chọn lọc, là một ứng viên giảm đau mới đầy hứa hẹn cho DNP.
Thiết kế nghiên cứu
Nghiên cứu BRADiNP (ClinicalTrials.gov NCT05219812) là một thử nghiệm ngẫu nhiên, mù đôi, kiểm soát bằng giả dược, hoán vị hoàn chỉnh giai đoạn 2a. Nghiên cứu đã tuyển chọn người lớn mắc đái tháo đường tuýp 1 hoặc tuýp 2 có đau thần kinh cảm giác vận động đối xứng xa kéo dài hơn sáu tháng và có đau thần kinh đo được. Sau một thời gian rửa sạch mù, loại bỏ các liệu pháp DNP trước đó, các đối tượng được ngẫu nhiên hóa 1:1 để nhận fulmetibant 450 mg mỗi ngày một lần hoặc giả dược trong bốn tuần, sau đó hoán vị sang liệu pháp thay thế trong bốn tuần nữa.
Điểm kết thúc chính về hiệu quả là sự thay đổi từ cơ bản trong điểm số mức độ đau trung bình trong 24 giờ hàng tuần được đo ở tuần 4 của mỗi kỳ điều trị, sử dụng các thang đo đau được xác nhận. Các điểm kết thúc thứ cấp bao gồm đánh giá về an toàn và khả năng dung nạp dựa trên các sự cố bất lợi được báo cáo và các thông số phòng thí nghiệm.
Kết quả chính
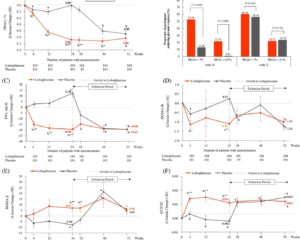
Tổng cộng 79 đối tượng bắt đầu điều trị với fulmetibant và 79 với giả dược; 75 hoàn thành cả hai kỳ điều trị. Tại điểm kết thúc chính (tuần 4), sự khác biệt trung bình về mức độ đau giữa fulmetibant và giả dược là 0,07 với khoảng tin cậy 95% từ -0,170 đến 0,314, cho thấy không có lợi ích giảm đau thống kê hay lâm sàng đáng kể của fulmetibant so với giả dược.
Sự vắng mặt của hiệu quả là nhất quán trong các nhóm con và các biện pháp thứ cấp. Về mặt an toàn, 41,8% đối tượng báo cáo các sự cố bất lợi khi dùng fulmetibant, so với 32,9% khi dùng giả dược. Hầu hết các sự cố bất lợi là nhẹ đến vừa phải, bao gồm mệt mỏi, chóng mặt và các triệu chứng tiêu hóa, không có sự cố bất lợi nghiêm trọng nào được gán cho fulmetibant.
Những kết quả này cho thấy rằng, mặc dù có lý thuyết hợp lý và bằng chứng tiền lâm sàng hỗ trợ việc đối kháng B1R cho đau thần kinh, fulmetibant ở liều và lịch điều trị được thử nghiệm không cung cấp lợi ích điều trị có ý nghĩa cho bệnh nhân mắc DNP.
Bình luận chuyên gia
Nghiên cứu BRADiNP cung cấp những hiểu biết quan trọng về những thách thức trong việc chuyển đổi các liệu pháp nhắm mục tiêu phân tử từ phòng thí nghiệm sang lâm sàng trong các tình trạng đau thần kinh phức tạp. Như đã lưu ý bởi các chuyên gia đau thần kinh, đái tháo đường thần kinh liên quan đến nhiều yếu tố bệnh sinh học bao gồm các thành phần chuyển hóa, mạch máu và thần kinh miễn dịch, có thể không được giải quyết đầy đủ bằng cách đối kháng B1R đơn thuần.
Các lý do tiềm năng cho kết quả tiêu cực bao gồm sự thâm nhập không đủ vào hệ thống thần kinh trung ương của fulmetibant, các con đường gây đau bù trừ và sự đa dạng của bệnh nhân về cơ chế đau. Thiết kế hoán vị của nghiên cứu tăng cường tính hợp lệ nội bộ bằng cách giảm biến động giữa cá nhân, nhưng thời gian điều trị bốn tuần có thể quá ngắn để quan sát được hiệu quả điều trị tối đa.
Nghiên cứu tương lai có thể khám phá các liệu pháp kết hợp, các mục tiêu thay thế trong hệ thống kinin-kallikrein hoặc lựa chọn bệnh nhân phân tầng dựa trên các hồ sơ sinh học. Hơn nữa, các nghiên cứu cơ chế kỹ lưỡng có thể giúp làm rõ tại sao việc ức chế B1R không tái tạo được hiệu quả giảm đau tiền lâm sàng trong DNP ở người.
Kết luận
Nghiên cứu giai đoạn 2a BRADiNP đã chứng minh rằng fulmetibant, một chất đối kháng thụ thể bradykinin-1, không giảm đáng kể mức độ đau thần kinh ở bệnh nhân mắc đau thần kinh do đái tháo đường so với giả dược. Mặc dù nói chung là an toàn, việc thiếu hiệu quả giảm đau làm nổi bật sự phức tạp của bệnh sinh DNP và những hạn chế của các phương pháp tiếp cận đơn mục tiêu.
Những kết quả này nhấn mạnh sự cần thiết cấp bách về việc tiếp tục đổi mới và hiểu sâu hơn về cơ chế để xác định các liệu pháp hiệu quả, an toàn cho DNP. Các bác sĩ nên tiếp tục hướng dẫn bằng các chiến lược quản lý đau thần kinh dựa trên bằng chứng hiện tại trong khi chú ý đến các tác nhân mới đang được đánh giá lâm sàng kỹ lưỡng.
Tài liệu tham khảo
1. Stemper B, Löwen S, Fritsch A, Hoffmann A, Sarkar A. The bradykinin-1 receptor antagonist fulmetibant in patients with diabetic neuropathic pain: the randomized, crossover, placebo-controlled, double-blind, phase 2a BRADiNP study. Pain. 2025 Oct 1;166(10):2421-2429. doi: 10.1097/j.pain.0000000000003642. Epub 2025 May 6. PMID: 40334047.
2. Ziegler D, Fonseca V. From guideline to patient: a review of recent recommendations for pharmacotherapy of painful diabetic neuropathy. J Diabetes Complications. 2015;29(1):146-156.
3. Fields HL. Mechanisms of neuropathic pain: therapeutic implications. Rev Neurol Dis. 2006;3(4):186-193.
4. Kemp TI, Kingsbury L, McNair K, Graham J, Helyes Z, Szabo A. Bradykinin and neuropathic pain: a novel pharmacological target? Eur J Pain. 2017;21(9):1431-1442.