Giới thiệu
Ung thư tiền liệt tuyến di căn kháng nút (mCRPC) vẫn là thách thức lâm sàng lớn và là nguyên nhân hàng đầu gây tử vong do ung thư ở nam giới trên toàn cầu. Mặc dù đã có những tiến bộ trong điều trị toàn thân như các chất ức chế đường dẫn truyền androgen (ARPIs) bao gồm Enzalutamide và Abiraterone, kết quả sống vẫn chưa tối ưu, đặc biệt khi có di căn xương. Radium-223 dichloride (Ra223), một dược phẩm phóng xạ phát ra hạt alpha chọn lọc nhắm vào di căn xương osteoblastic, đã chứng minh lợi ích sống khi sử dụng đơn độc trong bệnh nhân mCRPC có triệu chứng. Tuy nhiên, các chiến lược kết hợp với ARPIs đã gặp lo ngại về an toàn như đã ghi nhận trong thử nghiệm ERA 223 nơi Ra223 được kết hợp với Abiraterone, dẫn đến tỷ lệ gãy xương và tử vong tăng. Thử nghiệm EORTC 1333/PEACE-3 điều tra sự kết hợp của Enzalutamide với Ra223 làm liệu pháp đầu tiên trong mCRPC có di căn xương, với việc sử dụng bắt buộc các tác nhân bảo vệ xương (BPAs) để giảm thiểu các biến cố xương.
Thiết kế nghiên cứu
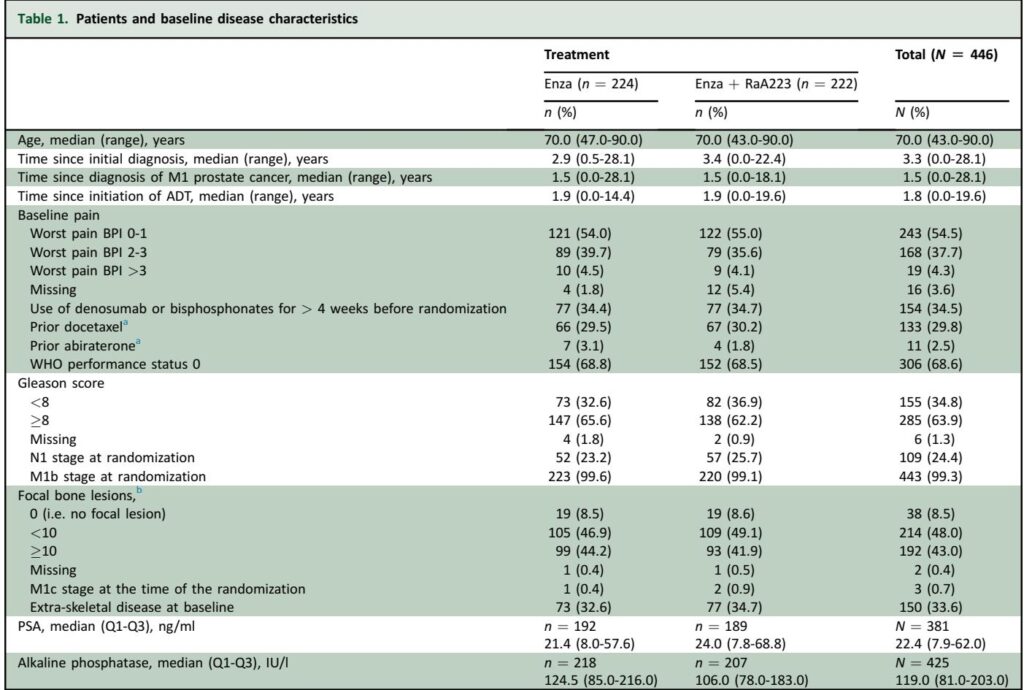
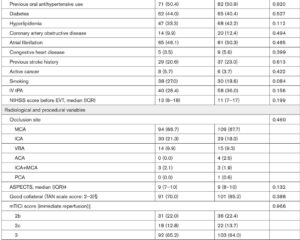
PEACE-3 là một thử nghiệm quốc tế, ngẫu nhiên, mở nhãn giai đoạn III tuyển chọn 446 bệnh nhân có mCRPC tiến triển và ít nhất hai di căn xương (tăng lên bốn ở châu Âu sau khi sửa đổi giao thức). Bệnh nhân không có di căn tạng và không triệu chứng hoặc đau nhẹ được phân ngẫu nhiên 1:1 để nhận Enzalutamide 160 mg mỗi ngày đơn độc hoặc Enzalutamide kết hợp với sáu liều tiêm tĩnh mạch hàng tháng của Ra223 ở liều 55 kBq/kg. Việc sử dụng bắt buộc BPAs (zoledronic acid hoặc denosumab) đã được thực hiện từ tháng 3 năm 2018 dựa trên tín hiệu an toàn trước đó. Các yếu tố phân tầng bao gồm quốc gia, điểm đau cơ bản, tiếp xúc docetaxel trước đó, sử dụng BPAs, và tiếp xúc abiraterone trước đó. Điểm cuối chính là thời gian sống không tiến triển theo hình ảnh (rPFS) được đánh giá bởi nhà nghiên cứu. Các điểm cuối phụ quan trọng bao gồm thời gian sống tổng thể (OS), thời gian đến lần điều trị hệ thống tiếp theo (TTNT), thời gian đến sự tiến triển đau (TTPP), và thời gian đến sự kiện xương có triệu chứng (TTSSE). Đánh giá an toàn bao gồm giám sát lâm sàng, phòng thí nghiệm và các sự cố bất lợi theo tiêu chuẩn CTCAE v4.03.
Kết quả chính
Với thời gian theo dõi trung bình vượt quá 41 tháng, thử nghiệm đã đạt được điểm cuối chính. Việc thêm Ra223 vào Enzalutamide cải thiện đáng kể rPFS: thời gian rPFS trung bình là 19.4 tháng (95% CI 17.1–25.3) trong nhóm kết hợp so với 16.4 tháng (95% CI 13.8–19.2) với Enzalutamide đơn độc (HR 0.69; 95% CI 0.54–0.87; P=0.0009). Hiệu ứng điều trị này nhất quán trong tất cả các nhóm phụ được chỉ định trước mà không có tương tác đáng kể.
Tại phân tích tạm thời OS tại 80% sự kiện, nhóm kết hợp cho thấy thời gian OS trung bình là 42.3 tháng (95% CI 36.8–49.1) so với 35.0 tháng (95% CI 28.8–38.9) trong nhóm đơn độc (HR 0.69; 95% CI 0.52–0.90; P=0.0031). Mặc dù giả định nguy cơ tỷ lệ không được thỏa mãn do các ca tử vong sớm trong nhóm kết hợp, việc theo dõi lâu hơn được lên kế hoạch để xác nhận lợi ích sống hứa hẹn này.
TTNT được kéo dài đáng kể với sự kết hợp (HR 0.57; P<0.0001), trong khi không có sự khác biệt đáng kể về TTPP hoặc TTSSE tại phân tích tạm thời.
Hồ sơ an toàn phù hợp với mong đợi: các sự cố bất lợi xuất hiện (TEAEs) cấp độ ≥3 xảy ra ở 55.8% bệnh nhân dùng Enzalutamide đơn độc và 65.6% nhận điều trị kết hợp. Đáng chú ý, sự kết hợp làm tăng tỷ lệ gãy xương (24.3% so với 13.4%) mặc dù có sử dụng bắt buộc BPAs, với tỷ lệ gãy xương giảm đáng kể sau khi thực hiện yêu cầu này. Huyết áp cao xuất hiện là một TEAE phổ biến cấp độ ≥3 (~34% trong cả hai nhóm), cao hơn so với những gì đã được báo cáo với Enzalutamide, có thể do tiêu chí bao gồm bệnh nhân rộng rãi hơn.
Bình luận chuyên gia
PEACE-3 đại diện cho nỗ lực học thuật nghiêm túc nhằm giải quyết nhu cầu chưa được đáp ứng quan trọng trong quản lý mCRPC: cải thiện kết quả cho bệnh nhân có di căn xương đồng thời duy trì an toàn. Sự cải thiện đáng kể trong rPFS và xu hướng OS hứa hẹn nhấn mạnh tiềm năng lợi ích cộng gộp hoặc cộng hưởng của Ra223 với Enzalutamide, có thể phản ánh khả năng của Ra223 phá vỡ môi trường di căn xương thông qua các cơ chế phức tạp ngoài độc tính trực tiếp.
Những nguy cơ không tỷ lệ quan sát được trong phân tích OS, với các ca tử vong sớm, đòi hỏi cách diễn giải thận trọng nhưng có thể phản ánh các hiệu ứng miễn dịch hoặc chậm như đã quan sát trong các thử nghiệm miễn dịch nơi lợi ích OS vượt quá cải thiện rPFS. Kết quả này biện minh cho phân tích OS cuối cùng được lên kế hoạch tại sự kiện đầy đủ để xác định chính xác lợi ích dài hạn.
Sử dụng bắt buộc BPAs là quan trọng để giảm các biến cố xương. PEACE-3 xác nhận các tín hiệu an toàn trước đây từ ERA 223 và nhấn mạnh sự cần thiết phải quản lý sức khỏe xương trong ngữ cảnh này. Sự cảnh giác liên tục đối với gãy xương và hoại tử xương hàm vẫn là điều cần thiết.
Các hạn chế bao gồm thời gian tuyển chọn kéo dài (>8.5 năm), phản ánh sự thay đổi trong thực hành lâm sàng và các thay đổi quy định sau ERA 223. Phần nhỏ bệnh nhân được điều trị trước bằng ARPIs trong tình trạng nhạy cảm với hormon có thể hạn chế khả năng tổng quát hóa cho các quần thể hiện đại ngày càng nhận ARPI therapy sớm hơn. Tuy nhiên, Enzalutamide cộng với Ra223 vẫn có liên quan, đặc biệt là cho bệnh nhân có ít tiếp xúc ARPIs trước đó hoặc chống chỉ định.
Kết luận
Thử nghiệm EORTC 1333/PEACE-3 xác định rằng việc thêm sáu chu kỳ Ra223 vào Enzalutamide và BPAs cải thiện đáng kể rPFS và gợi ý lợi ích OS trong bệnh nhân có mCRPC và di căn xương. Hồ sơ an toàn của sự kết hợp có thể kiểm soát được, với sự nhấn mạnh vào việc ngăn ngừa gãy xương thông qua các tác nhân nhắm mục tiêu xương. Chế độ điều trị này cung cấp một lựa chọn điều trị đầu tiên hấp dẫn, nhấn mạnh tầm quan trọng của việc tích hợp các dược phẩm phóng xạ với ARPIs trong trình tự điều trị mCRPC. Việc theo dõi tiếp theo sẽ làm rõ mức độ và độ bền của lợi ích sống.
Tài liệu tham khảo
Tombal B, Choudhury A, Saad F, et al. Enzalutamide plus radium-223 in metastatic castration-resistant prostate cancer: results of the EORTC 1333/PEACE-3 trial. Ann Oncol. 2025 Sep;36(9):1058-1067. doi:10.1016/j.annonc.2025.05.011. Epub 2025 May 30. PMID: 40450503.