亮点
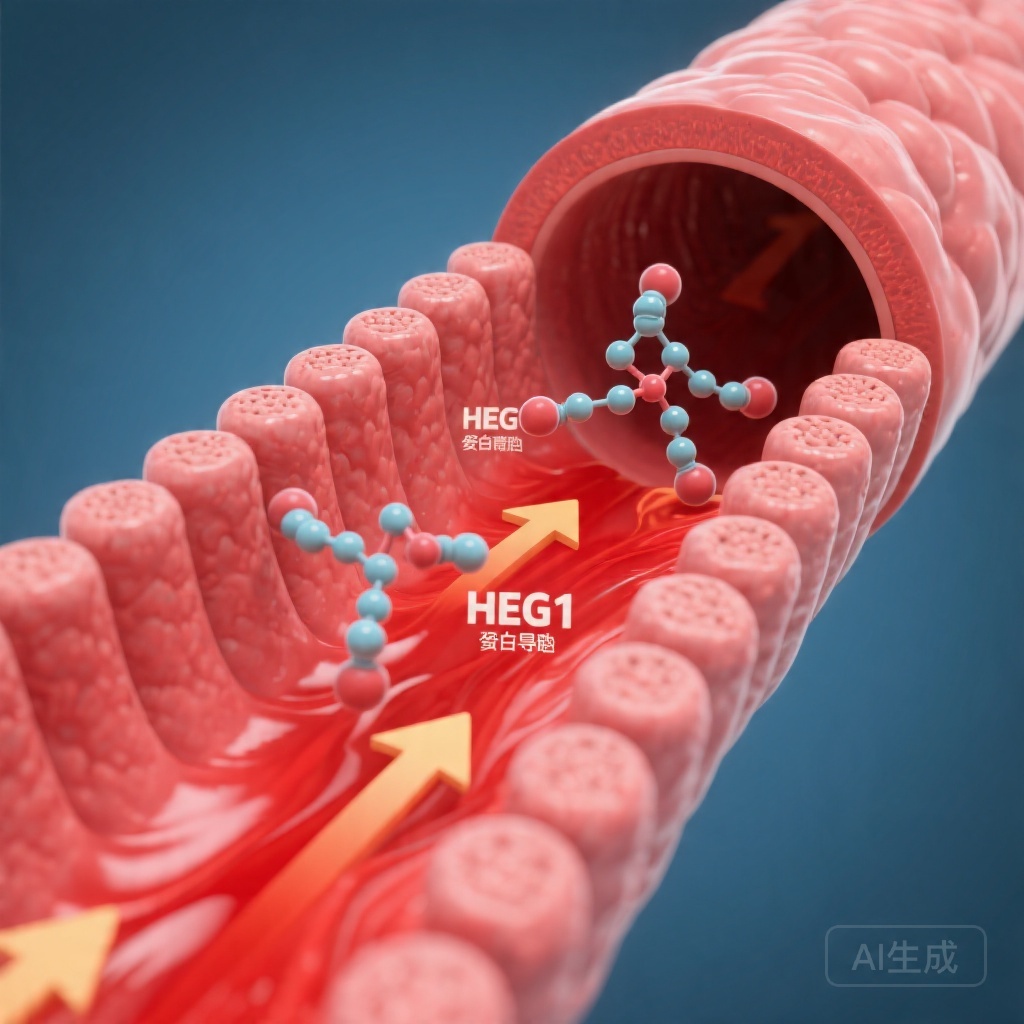
剪切应力诱导的内皮HEG1信号通路代表了一种新的调节机制,将血流动态与全身血压控制联系起来。高血压患者由于血管内皮壁剪切应力降低,血浆HEG1水平显著下降。小鼠中内皮特异性删除Heg1基因导致血压升高、内皮依赖性血管舒张受损和一氧化氮生成中断。该机制涉及HEG1介导的PHACTR1降解调控,控制SP1依赖性的eNOS转录。
背景
高血压仍然是全球心血管疾病、中风和肾功能障碍的主要可改变风险因素。尽管有多种抗高血压药物可用,但仍有相当比例的患者未能达到理想的血压控制,强调了寻找新型治疗靶点的必要性。内皮细胞覆盖整个血管系统,作为关键的机械感受器,将血液动力学力量(尤其是壁剪切应力)转化为生物化学信号,调控血管张力和血压稳态。
剪切应力是血流对内皮表面施加的摩擦力,通过尚未完全理解的机制刺激血管舒张。这种机械传导途径的损伤会导致内皮功能障碍,这是高血压和动脉粥样硬化性心血管疾病的标志。了解将剪切应力感知与一氧化氮(NO)生成连接起来的分子中介,可能揭示血压管理的可行目标。
心源性发育蛋白含EGF样结构域1(HEG1)是一种由内皮衍生的膜蛋白,先前已与流动力学和心血管表型相关联。流行病学数据表明HEG1表达与心血管危险因素呈负相关,但这种关联的机制基础尚未明确。本研究旨在阐明内皮HEG1在血压调节中的作用,并表征其下游信号级联。
研究设计
该研究采用多模态方法,整合人类流行病学、计算建模和实验小鼠遗传学,以确定HEG1信号传导与血压控制之间的因果关系。
人类研究包括多个队列的全表型关联分析、计算流体力学分析以表征主干动脉的剪切应力模式、动脉标本内皮细胞的单细胞RNA测序以及来自独立验证队列的高血压和正常血压受试者的血浆HEG1浓度测量。
实验研究使用通过Tie2启动子下的Cre-lox重组生成的内皮特异性Heg1敲除小鼠。使用遥测技术在清醒且不受限制的小鼠中进行血压监测。通过线性肌图评估内皮依赖性和内皮非依赖性血管舒张功能。研究在C57BL/6J和Apoe敲除(ApoeKO)背景下进行,以检查与血脂异常的相互作用。
机制研究采用蛋白质组学、转录组学、泛素化测定和核质分离,以鉴定HEG1相互作用蛋白和下游效应因子。使用CCG-1423药理抑制PHACTR1核转运测试治疗潜力。
主要发现
人类高血压中HEG1减少
在三个独立队列中,高血压患者的血浆HEG1浓度显著低于正常血压对照组(p < 0.001)。这种减少与通过计算流体力学分析颈动脉和肱动脉得出的壁剪切应力估计值降低相关。单细胞RNA测序确认HEG1表达主要在内皮细胞中,低剪切应力区域的血管中转录水平降低。
Heg1删除后的血压升高
内皮特异性Heg1敲除小鼠与同窝对照组相比,收缩压持续升高(平均差异:+12 mmHg,95% CI:8-16 mmHg,p < 0.001)。在ApoeKO背景下,Heg1缺乏的小鼠发展出相当于人类2期高血压的高血压。舒张压和平均动脉压也相应升高。
血管舒张能力受损
线性肌图显示,Heg1缺乏的主动脉和肠系膜阻力动脉内皮依赖性血管舒张严重受损。乙酰胆碱剂量反应曲线右移,最大反应减少约60%(p < 0.001)。内皮非依赖性血管舒张对硝普钠保持完整,证实了特定的内皮机制。这种损害在C57BL/6J小鼠中基线时观察到,并在高脂饮食的ApoeKO动物中加剧。
分子机制:HEG1-PHACTR1-eNOS轴
蛋白质组学分析鉴定PHACTR1(磷酸酶和肌动蛋白调节蛋白1)为结合伴侣,其水平由HEG1反向调控。HEG1与CUL3物理相互作用,CUL3是Cullin-RING E3泛素连接酶复合物的支架蛋白,促进CUL3介导的PHACTR1泛素化和蛋白酶体降解。在缺乏HEG1的情况下,PHACTR1积累并发生核转运。
在细胞核内,PHACTR1抑制SP1介导的eNOS(内皮一氧化氮合酶)转录,后者是一氧化氮生成的关键限速酶。染色质免疫沉淀证实Heg1缺乏的内皮细胞中SP1与eNOS启动子的结合减少。相应地,条件培养基和主动脉组织中的一氧化氮代谢物水平显著降低。
药理救援
用CCG-1423(一种小分子抑制剂,抑制PHACTR1核定位)治疗可防止Heg1缺乏小鼠的血压升高并恢复内皮依赖性血管舒张。通过饮用水给药四周后,核PHACTR1积累减少,eNOS表达恢复到野生型水平,血压恢复正常,不影响收缩功能或肾脏参数。
关键机制通路
正常剪切应力 → HEG1表达和释放 → CUL3介导的PHACTR1降解 → 核内PHACTR1低 → SP1活性不受抑制 → eNOS转录 → NO生成 → 血管舒张 → 正常血压。
高血压 ↓ 剪切应力 → HEG1下调 → PHACTR1积累 → 核转运 → SP1抑制 → eNOS抑制 → NO减少 → 血管舒张受损 → 血压升高。
专家评论
这些发现确立了HEG1作为关键的机械敏感调节因子,将血液动力学力量与内皮NO生成联系起来。HEG1介导的泛素化控制下剪切应力与PHACTR1核定位之间的逆向关系,提供了低或振荡剪切应力区域易患内皮功能障碍和高血压的有力分子解释。
观察到药理抑制PHACTR1核导入可在遗传性高血压模型中恢复正常血压,表明这一途径可能适合治疗靶向。虽然CCG-1423目前未获临床批准,但它代表了一类新型抗高血压药物的概念证明。
有几个局限性需要考虑。首先,人类研究具有相关性;尽管遗传小鼠模型支持其转化意义,但仍需要人类干预研究。其次,ApoeKO背景与动脉粥样硬化性疾病相关,引入了代谢混杂因素。第三,鉴于PHACTR1在其他组织(包括大脑和肾脏)中的作用,其抑制的长期安全性仍需确定。
HEG1作为支架将CUL3和PHACTR1聚集在一起的机制洞察扩展了我们对内皮机械传导的理解。HEG1基疗法是否可以补充现有的抗高血压策略,尤其是在耐药性高血压患者中,值得研究。
结论
本研究确定了一种新的剪切应力响应信号轴,中心为内皮HEG1,通过调控PHACTR1泛素化、核定位和下游eNOS表达来控制血压。高血压患者血浆HEG1减少反映了内皮机械感应减弱,可能作为血流介导的血管舒张受损的生物标志物。
从剪切应力到HEG1、CUL3、PHACTR1、SP1再到eNOS转录的机制级联代表了一个先前未被认识的途径,将血管生物学与全身血压控制联系起来。CCG-1423介导的PHACTR1核导入抑制为与内皮功能障碍相关的高血压提供了一种潜在的治疗策略。
未来方向包括开发HEG1模拟肽或小分子激活剂、验证血浆HEG1作为预后生物标志物,以及在有记录的内皮功能障碍的高血压人群中进行PHACTR1核导入抑制剂的临床试验。
资助
本研究得到国家自然科学基金、中国医学科学院和欧洲研究委员会的资助。作者声明无利益冲突。
参考文献
Wu W, Liu J, Chen X, Zhu P, Xu J, Yue J, Liu X, Fang J, Chen X, Pi J, Zheng L, Zhang Q, Zhang L, Schneider CV, Schneider KM, Trautwein C, Gao P, Reilly MP, Zhang Y, Zheng X, Liu J. Shear stress-induced endothelial HEG1 signalling regulates vascular tone and blood pressure. Eur Heart J. 2026;47(14):1721-1737. PMID: 40986512.