亮点
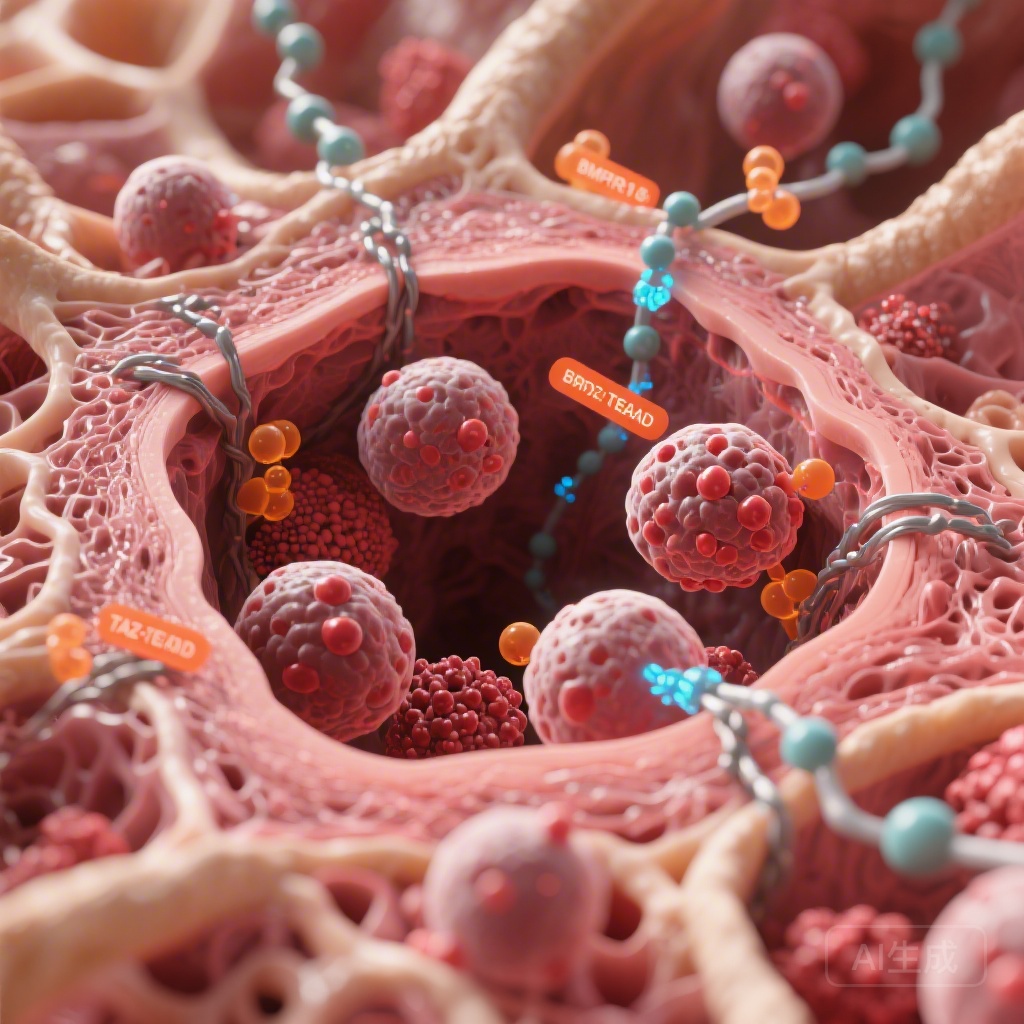
- BMPR1B和TAZ/TEAD在复发性AML患者及对阿糖胞苷或维奈托克耐药的细胞中的表达水平显著升高。
- 骨髓物理变化,包括细胞外基质硬化和髓内压增高,驱动白血病持续存在。
- 在高限制条件下,间充质干细胞(MSCs)分泌BMP4,特异性激活化疗耐药的AML细胞。
- 联合抑制BMPR1B或TAZ/TEAD与阿糖胞苷能有效清除3D人骨髓模型中的AML原代细胞。
引言:AML的生物力学景观
数十年来,急性髓系白血病(AML)的管理几乎完全集中在白血病母细胞的基因和表观遗传学特征上。尽管引入了FLT3抑制剂和维奈托克等靶向疗法,但5年总生存率仍仅为20%。这一临床停滞表明我们对化疗耐药性的理解是不完整的。越来越多的证据现在指向骨髓(BM)微环境——不仅作为细胞的被动储存库,而且作为疾病进展的积极参与者。
随着白血病母细胞的克隆扩增,它们从根本上改变了骨髓的物理特性。这种“生物力学重塑”包括细胞外基质(ECM)硬化、髓内压升高以及驻留细胞可用物理空间的显著减少。虽然这些变化在实体瘤中已经观察多年,但其在血液系统恶性肿瘤生存中的作用才刚刚被阐明。Barral等人(2026年)的研究提供了关键突破,确定机械转导——细胞将机械刺激转化为化学信号的过程——是AML化疗耐药性的主要驱动因素。
研究设计和方法框架
研究人员采用多方面的方法调查机械应激在AML中的作用。该研究使用了诊断时和复发时收集的原发性AML样本,以及特异性工程化为对标准治疗药物阿糖胞苷(Ara-C)和维奈托克耐药的细胞系。
为了模拟白血病骨髓的物理约束,研究团队开发了一个3D人骨髓样模型。该平台允许精确操控基质硬度和细胞限制,提供比传统2D培养更生理相关的环境。研究重点是两个关键的机械转导通路:骨形态发生蛋白(BMP)通路和Hippo通路效应器,TAZ和YAP。通过转录组分析和蛋白质定量,作者试图确定这些通路如何响应白血病生态位的机械压力。
关键发现:BMPR1B和TAZ/TEAD轴
BMPR1B和TAZ在耐药性中的上升
分析揭示了机械转导信号与临床结果之间的显著相关性。化疗后复发的患者显示BMPR1B(一种BMP受体)和TAZ及其转录伙伴TEAD的水平显著高于初次诊断时。有趣的是,尽管TAZ上调,其同源物YAP——通常被认为是其他组织中的中心机械传感器——并未显示出类似的增加。这表明TAZ在白血病骨髓环境中具有特定且不可替代的作用。
这一模式在体外也得到了反映。对阿糖胞苷和维奈托克耐药的AML细胞系表现出TAZ/TEAD复合体的组成型激活。这些耐药细胞不仅是遗传上不同,而且在机械上也是不同的。它们表现出对纤连蛋白和层粘连蛋白等微环境成分的更好黏附性,以及更高的内在可变形性,使其能够在拥挤骨髓的高压力、受限空间中导航并存活。
旁分泌信号:MSC的联系
该研究还强调了白血病细胞与驻留间充质干细胞(MSCs)之间的关键交叉对话。在高物理限制条件下——模拟充满母细胞的骨髓过度拥挤——MSCs被发现表达更高水平的BMP4。这种MSC来源的BMP4作为旁分泌信号,特异性激活化疗耐药AML细胞表面的BMPR1B。这种相互作用似乎创造了一个保护性的“生态位效应”,其中疾病的物理应力触发了生存信号,保护母细胞免受化疗诱导的凋亡。
靶向机械组以敏感化母细胞
或许最具有临床意义的发现是药理学抑制的效果。利用3D人骨髓模型,研究人员证明靶向BMPR1B或TAZ/TEAD复合体可以打破耐药循环。当这些机械转导抑制剂与阿糖胞苷联合使用时,AML原代细胞的持续存在受到协同损害。通过阻断细胞感知和响应硬化、高压环境的能力,治疗有效地“揭开了”白血病细胞,使它们再次对常规细胞毒性治疗变得脆弱。
专家评论:机制见解和临床意义
Barral等人的发现代表了我们如何应对难治性AML的范式转变。传统上,我们将骨髓视为液体隔室,但这项研究迫使我们将其视为一个固体肿瘤微环境,在该环境中物理力量决定了细胞命运。
TAZ而非YAP的特定参与是一个特别有趣的生物学细节。在许多上皮癌中,YAP和TAZ通常共同激活,但白血病生态位可能对细胞施加独特的机械需求,从而偏向TAZ-TEAD转录程序。这种特异性为药物开发提供了更窄且可能更有效的治疗窗口。
然而,也有需要考虑的局限性。虽然3D BM样模型是一个重要的进步,但它无法完全复制人类患者的系统复杂性,包括免疫系统在生态位中的作用。此外,AML的髓内压是动态的;了解这些通路在诱导和巩固治疗各个阶段的波动对于机械转导靶向干预的时间至关重要。
从卫生政策和临床试验的角度来看,这些结果表明我们应该开始将生物力学标志物——可能通过高级成像或专门的活检分析——纳入AML的风险分层。如果患者出现特别硬或高压的骨髓,他们可能是早期干预BMPR1B或TAZ抑制剂的理想候选者。
结论:AML治疗的新支柱
确定BMPR1B和TAZ/TEAD是化疗耐药性的介质,为血液学-肿瘤学开辟了新的前沿。通过解决白血病骨髓的物理现实,我们可能最终能够克服长期以来困扰AML治疗的环境介导的药物耐药性。未来结合传统细胞静止剂与机械转导抑制剂的治疗策略有望为目前选择有限的患者带来更深的缓解和更低的复发率。随着我们迈向2026年及以后,生物物理学在临床肿瘤学中的整合可能会成为精准医疗的基石。
参考文献
- Barral L, Lespinasse N, Martin Cardozo C, 等. 靶向BMP和TAZ/TEAD机械转导通路可降低急性髓系白血病的化疗耐药性。Leukemia. 2026-03-18. PMID: 41851473.
- Lampi MC, Reinhart-King CA. 靶向细胞外基质硬度以减缓疾病进展。Sci Transl Med. 2018;10(422).
- Passaro D, 等. 髓内压升高导致造血干细胞丢失和骨髓增生异常。Cell Stem Cell. 2021.
- Dupont S, 等. YAP/TAZ在机械转导中的作用。Nature. 2011;474(7350):179-183.