亮点
Merus 公司展示了令人信服的中期临床证据,证明了 Petosemtamab(一种靶向 EGFR 和 LGR5 的双特异性抗体)在转移性结直肠癌 (mCRC) 中表现出高客观缓解率。与标准化疗方案 FOLFOX/FOLFIRI 联合使用时,在一线 (1L) 左侧 mCRC 中达到了 100% 的缓解率,总体缓解率 (ORR) 为 90%。在二线 (2L) 治疗中,ORR 为 62%,而在三线 (3L+) 及以上单药治疗中,ORR 为 10%。安全性与先前观察一致,未发现新的信号。
研究背景
转移性结直肠癌仍然是全球重要的临床挑战,其分子异质性和对标准化疗和靶向药物的反应率不一。抗表皮生长因子受体 (EGFR) 单克隆抗体在特定 mCRC 亚组中改善了预后,尤其是 RAS/BRAF 野生型肿瘤患者。然而,耐药机制和右半结直肠癌疗效有限仍是障碍。因此,需要新型疗法来提高疗效并保持安全性。
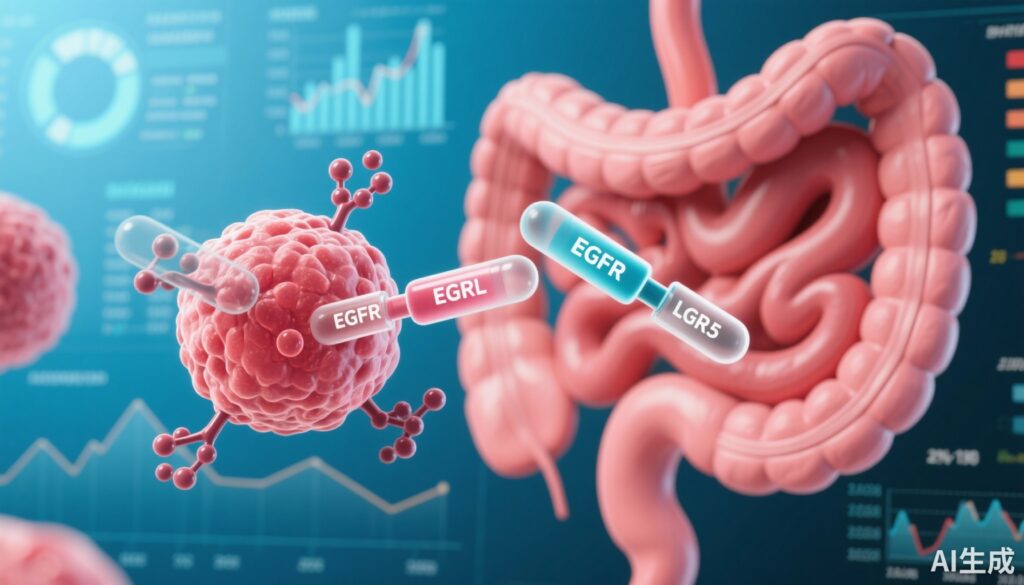
Petosemtamab 是一种人源化全长 IgG1 抗体,同时靶向 EGFR 和富含亮氨酸重复序列的 G 蛋白偶联受体 5 (LGR5),后者是与结直肠癌干细胞增殖和耐药相关的标志物。其多模式机制包括抑制 EGFR 信号传导、通过 LGR5 结合促进 EGFR 内化和降解,以及增强抗体依赖性细胞毒性 (ADCC) 和吞噬作用 (ADCP)。这些作用有望克服典型的耐药途径并改善 mCRC 的肿瘤控制。
研究设计
正在进行的 II 期临床试验包括根据治疗线和肿瘤位置分层的转移性结直肠癌患者。共纳入 54 名左半和/或右半、RAS/BRAF 野生型、微卫星稳定 (MSS) 的 mCRC 患者。患者每两周接受 1500 mg Petosemtamab 联合 FOLFOX 或 FOLFIRI 化疗(一线 [1L] 和二线 [2L]),或在三线 (3L) 及以上接受 Petosemtamab 单药治疗。值得注意的是,1L 和 2L 患者此前未接受过抗 EGFR 药物治疗,而 3L+ 患者至少接受过两种包括抗 EGFR 疗法在内的先前治疗方案。
疗效分析的资格要求包括至少接受一次 Petosemtamab 治疗,至少 8 周的随访时间,以及至少一次基线后的肿瘤评估或因进展、临床恶化或死亡而提前停药。
关键发现
一线治疗 (1L): 14 名患者接受了 Petosemtamab 联合 FOLFOX/FOLFIRI 治疗;10 名患者可评估疗效,其中 8 名患者为左侧肿瘤。在这 10 名患者中,客观缓解率为 80%(10 人中有 8 人),包括 1 例确认的完全缓解 (CR) 和 7 例部分缓解 (PR),其中 3 例未确认。在左侧肿瘤中,初始缓解率为 88%(8 人中有 7 人),在数据截止后重新分类 1 例稳定疾病 (SD) 为未确认 PR 后,缓解率提高至 100%(8 人中有 8 人)。考虑所有可评估患者后,1L 总体 ORR 提高到 90%,所有未确认 PR 持续无进展。
二线治疗 (2L): 14 名接受 Petosemtamab 联合化疗(主要是 FOLFIRI)治疗的患者进行了评估;13 名患者可评估。ORR 为 62%(13 人中有 8 人),全部为部分缓解,包括一些未确认的。其余患者出现稳定疾病或首次影像学检查前的早期临床恶化。未确认 PR 和 SD 患者持续治疗无进展。
三线及以上 (3L+): 26 名患者接受了 Petosemtamab 单药治疗;20 名患者可评估。ORR 为 10%(2 例部分缓解),9 名患者达到稳定疾病。5 例 SD 患者持续治疗无进展。
安全性概况: Petosemtamab 在各治疗线中耐受性良好,安全性与之前在复发/转移性头颈部鳞状细胞癌中的研究一致。与 FOLFOX/FOLFIRI 联合使用未导致额外或意外的毒性。未出现新的安全性信号。
专家评论
在一线治疗中,Petosemtamab 联合标准化疗,特别是左侧 mCRC 肿瘤中 100% 的缓解率,是一个显著的进展。左侧结直肠癌通常对 EGFR 靶向治疗反应更好,Petosemtamab 的双靶向机制可能通过同时阻断 EGFR 通路和靶向 LGR5 介导的肿瘤干细胞来放大这种效果。通过促进 EGFR 内化和降解,该抗体可能克服限制当前 EGFR 定向疗法的耐药机制。
二线结果显示在化疗失败后有良好的疾病控制,但缓解率较低,这与药物耐药性的增加一致。在经过大量预处理的患者中,单药 Petosemtamab 的疗效减弱,但仍表明值得进一步探索的活性。
安全性数据令人放心地支持联合使用不会加剧化疗相关毒性,这对于临床应用至关重要。
局限性包括样本量相对较小和数据的初步性质,一些缓解在数据截止时尚未确认。需要更长时间的随访以评估持久性和生存获益。入组仅限于 MSS 和 RAS/BRAF 野生型肿瘤,限制了对更广泛 mCRC 人群的推广。未来的随机试验对于验证这些发现至关重要。
结论
Petosemtamab 是一种新型双特异性抗体,靶向 EGFR 和 LGR5,在一线和二线转移性结直肠癌治疗中,尤其是在左侧肿瘤中,与标准化疗联合使用时表现出强大的抗肿瘤活性。其独特的机制可能克服现有疗法中的耐药屏障。安全性支持进一步开发。这些有前景的中期结果值得推进到更大规模的对照试验,以确认临床获益并定义其在 mCRC 管理中的角色。Petosemtamab 代表了一种潜在的进展,解决了这一难以治疗的癌症亚群中的未满足治疗需求。
资金和试验注册
该临床试验由 Merus 赞助,Petosemtamab 的开发者。新闻发布中未提供具体的试验注册号。
参考文献
- Cunningham D 等. Cetuximab 单药治疗和 Cetuximab 联合伊立替康在伊立替康难治性转移性结直肠癌中的疗效。N Engl J Med. 2004;351(4):337-345.
- Van Cutsem E 等. 抗 EGFR 疗法联合或不联合一线化疗在 mCRC 中的疗效:一项荟萃分析。Lancet Oncol. 2017;18(1):47-63.
- de Souza P 等. 结直肠癌干细胞中的 LGR5:信号通路和治疗靶点。Int J Mol Sci. 2020;21(4):1395.
- Merus 新闻稿,2024 年 6 月。Merus 宣布转移性结直肠癌二期 Petosemtamab 试验的积极中期数据。