亮点
与teprotumumab类似的IGF-1R抑制剂IBI311,在活动性中重度甲状腺眼病(TED)中国患者中,24周时的突眼反应率为85.8%,而安慰剂组为3.8%。
该试验显示临床活动评分(CAS)和突眼显著减少,证实了IBI311在活动性TED中的抗炎和解剖学益处。
IBI311表现出良好的安全性,仅报告了轻至中度不良事件,未报告严重不良事件。
研究背景
甲状腺眼病(TED)是一种主要影响眼眶和眶周组织的自身免疫性炎症性疾病,常与Graves病相关。临床上表现为突眼、眼睑退缩、复视和炎症,可能导致显著的外观畸形、视力损害和生活质量下降。TED在不同种族间存在表型变异,影响疾病的严重程度和对治疗的反应。尽管取得了进展,但治疗选择仍然有限,尤其是对于活动性中重度TED。
近年来的研究发现,胰岛素样生长因子1受体(IGF-1R)信号通路在TED发病机制中起核心作用。靶向IGF-1R的人类单克隆抗体teprotumumab于2020年获得FDA批准,主要是基于非亚洲人群的关键试验。然而,亚洲地区实际使用这种疗法的机会有限,且在亚洲,特别是中国人群中关于其有效性和安全性的数据很少。IBI311是一种与teprotumumab氨基酸序列相同的IGF-1R抑制剂,但在剂型上有所不同,旨在用于中国患者。
研究设计
RESTORE-1是一项多中心、随机、双盲、安慰剂对照的III期临床试验,于2023年5月至12月在中国20家三级医院进行。共纳入82名活动性中重度TED患者(定义为临床活动评分[CAS]≥3)。关键排除标准包括TED发病超过270天、威胁视力的TED以及既往接受过脉冲皮质类固醇、放疗或眼眶手术。
参与者按2:1的比例随机分配,每三周静脉注射一次IBI311或安慰剂,共21周,评估持续至第24周。主要终点是第24周时研究眼突眼减少≥2毫米的患者比例。
次要终点包括综合反应(突眼和CAS减少)、CAS改善、复视反应和以已知与IGF-1R抑制相关的不良事件为重点的安全性评估。
主要发现
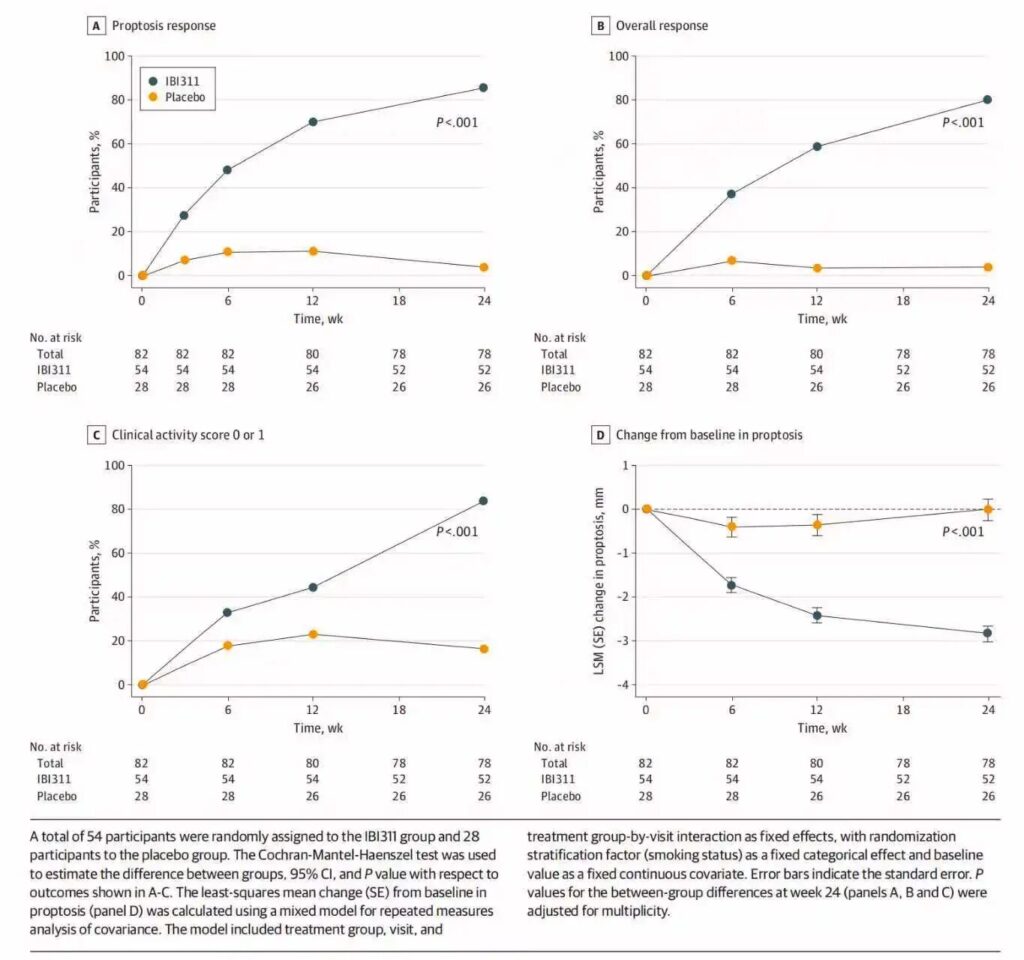
在82名随机分配的参与者中(平均年龄39.6岁;68.3%为女性),54名接受了IBI311,28名接受了安慰剂。第24周的结果令人瞩目:
突眼反应: IBI311组中有85.8%(45/52)的患者突眼减少,而安慰剂组为3.8%(1/26)(差异81.9个百分点;95% CI,69.8至93.9;P < .001)。总体反应: 突眼减少≥2毫米且CAS减少≥2的综合反应率,IBI311组为80.2%,安慰剂组为3.6%(差异76.3个百分点;95% CI,63.3至89.4)。CAS改善: 达到CAS评分为0或1的患者比例,IBI311组为83.5%,安慰剂组为16.6%(差异67.1个百分点;95% CI,49.4至84.8)。突眼幅度: 最小二乘均值变化为-2.85毫米(SE 0.18),安慰剂组为-0.02毫米(SE 0.24)(差异-2.83毫米;95% CI,-3.39至-2.27;所有P < .001)。复视反应: 至少降低一个等级的复视反应率,IBI311组为66.0%,安慰剂组为53.3%,但这一差异无统计学意义(P = .46)。
安全性分析显示,所有与输注反应、听力障碍、高血糖、肌肉痉挛、恶心或腹泻相关的不良事件均为轻至中度。IBI311组未发生严重不良事件或死亡。
专家评论
RESTORE-1试验强有力地证实了针对IGF-1R的IBI311能为中国活动性TED患者提供具有临床意义的改善,这是一个此前研究不足的群体。突眼减少(-2.85毫米)和CAS改善的程度与teprotumumab的关键试验相当,进一步证实了IGF-1R通路在TED中的机制作用。
重要的是,这项研究填补了TED临床研究中的种族和地区空白。鉴于表型变异和可能影响疗效和安全性的药代动力学差异,该研究在中国队列中的积极结果支持IBI311作为一种文化和地区适宜的治疗替代方案。
然而,一些局限性值得关注。该研究排除了威胁视力的疾病患者和长期TED(>270天)患者,因此结果可能不适用于所有TED患者。还需要更长时间的数据来评估反应的持久性和现实世界的有效性。此外,复视结果不够稳健,表明运动障碍的治疗效果可能更为多变。
结论
IBI311在治疗中国活动性中重度TED患者中表现出显著的疗效和令人放心的安全性。其氨基酸序列与teprotumumab相同,但剂型不同,能够扩大可及性,同时保持治疗效益。临床医生应考虑IBI311作为解决亚洲TED患者未满足需求的一种有前景的选择。
未来的研究将有助于评估长期结果、现实世界应用和在不同亚组中的使用。总体而言,IBI311代表了TED管理的重要进展,改善了患者预后并扩展了全球治疗选择。
资助和试验注册
本试验在ClinicalTrials.gov注册,标识符为NCT05795621。资金来源在主要出版物中未明确报告。
参考文献
Zhang H, Sun J, Li Y, Zhu L, Shan Z, Lu W, et al. IGF-1R Inhibitor IBI311 for the Treatment of Active Thyroid Eye Disease in Chinese Patients: The RESTORE-1 Randomized Clinical Trial. JAMA Ophthalmol. 2025 Oct 9:e253350. doi:10.1001/jamaophthalmol.2025.3350
IF: 9.2 Q1 B1 . Epub ahead of print. PMID: 41066129
IF: 9.2 Q1 B1 ; PMCID: PMC12512031
IF: 9.2 Q1 B1 .