亮点
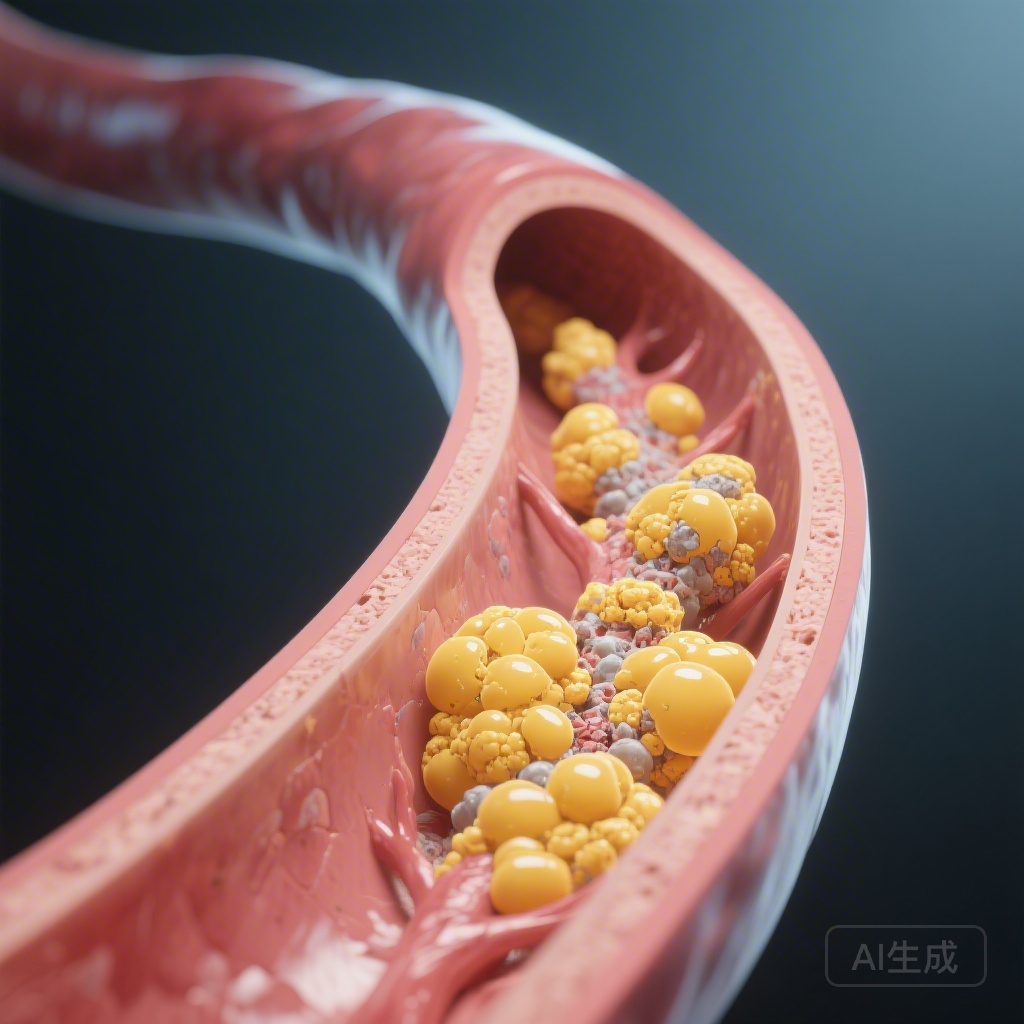
在一项涉及非转移性前列腺癌 (PCa) 男性的里程碑式随机临床试验中,与 GnRH 拮抗剂 relugolix 相比,GnRH 激动剂亮丙瑞林在 12 个月内总冠状动脉斑块体积 (TPV) 的增加显著更大。
斑块体积的增加主要由非钙化斑块体积 (NCPV) 驱动,这是一种常与更高脆弱性和急性冠状动脉综合征风险增加相关的动脉粥样硬化表型。
本研究提供了关键的机制证据,可能解释了不同类别的雄激素剥夺疗法 (ADT) 之间观察到的心血管安全性差异,为高心血管风险患者提供个性化治疗选择的潜在途径。
对年龄、他汀类药物使用和基线斑块体积的调整并未减轻研究结果,表明 ADT 类别是该人群中冠状动脉粥样硬化进展的独立驱动因素。
引言:泌尿肿瘤学与心血管健康的交汇点
雄激素剥夺疗法 (ADT) 是许多阶段前列腺癌治疗的基石,尤其是与局部高危疾病的放疗联合使用时。然而,ADT 的生存益处经常被其代谢和心血管副作用所掩盖。数十年来,临床医生观察到 ADT 与心肌梗死、中风和心血管死亡风险增加之间的关联。随着前列腺癌患者的寿命因肿瘤学进步而延长,心血管疾病 (CVD) 已成为这一人群非癌症死亡的主要原因。
这种风险的生物学基础一直是激烈争论的主题。传统理论认为,体重增加、胰岛素抵抗和血脂异常等代谢变化是主要原因。然而,最近的临床关注已转向 ADT 的具体药理机制。越来越多的证据表明,促性腺激素释放激素 (GnRH) 激动剂(如亮丙瑞林)和 GnRH 拮抗剂(如 relugolix)可能具有不同的心血管安全性特征。HERO 试验 (NCT03085030) 之前已证明 relugolix 与亮丙瑞林相比,主要不良心血管事件 (MACE) 减少了 54%,但这一差异的根本原因仍属猜测。这项发表在《JAMA Cardiology》上的新研究通过使用高级成像技术直接评估这些疗法对冠状动脉解剖的影响,旨在填补这一空白。
研究设计:亚特兰大随机临床试验
为了调查 ADT 类别是否影响动脉粥样硬化的进展速度,亚特兰大乔治亚州一所学术机构的四个中心的研究人员进行了一项开放标签随机临床试验。该研究招募了 65 名非转移性前列腺癌男性,这些男性是盆腔放疗和至少六个月 ADT 的候选者。重要的是,参与者此前未接触过 ADT,确保了观察疗法效果的干净基线。
患者群体和随机化
参与者以 1:1 的比例随机分配接受 GnRH 激动剂亮丙瑞林或 GnRH 拮抗剂 relugolix。在 65 名入组的男性中,62 名完成了完整的 12 个月方案,包括必要的成像。队列的平均年龄为 68.5 岁,56% 的人已经在服用他汀类药物,反映了存在心血管危险因素的典型临床人群。试验注册时间为 2022 年 6 月至 2024 年 3 月,数据分析于 2025 年中期完成。
主要和次要终点
主要终点是从基线到 12 个月的冠状动脉总斑块体积 (TPV) 变化,通过冠状动脉计算机断层扫描血管造影 (CCTA) 测量。CCTA 是一种高度敏感的无创成像方法,可以量化不同类型的斑块。次要终点包括非钙化斑块体积 (NCPV)、钙化斑块体积 (CPV) 和低衰减斑块体积 (LAPV) 的变化,后者通常被认为是高风险“易损”斑块的标志。
关键发现:量化斑块进展
试验结果显示,两类 ADT 对冠状动脉的影响存在显著差异。接受 GnRH 激动剂亮丙瑞林治疗的患者比接受拮抗剂 relugolix 治疗的患者经历了更严重的斑块进展。
总斑块体积和非钙化斑块体积
在调整基线斑块体积、年龄和他汀类药物使用后,亮丙瑞林组在 12 个月内的 TPV 增加显著大于 relugolix 组。估计差异为 +68.9 mm³(95% CI,23.2-114.5 mm³;P = .02)。从斑块成分来看,这种差异几乎完全由非钙化斑块体积驱动。亮丙瑞林组的 NCPV 增加估计比 relugolix 组多 64.5 mm³(95% CI,31.6-97.3 mm³;P = .004)。
钙化斑块和低衰减斑块
有趣的是,两组在钙化斑块体积 (CPV) 或低衰减斑块体积 (LAPV) 的变化方面没有统计学显著差异。虽然钙化斑块通常被视为“稳定”或较老的动脉粥样硬化,但非钙化斑块更具代谢活性且容易破裂。亮丙瑞林特别加速了非钙化斑块的进展,这表明冠状动脉健康发生了更急性和潜在危险的变化。
专家评论:机制见解和临床意义
这项试验的结果首次提供了随机证据,证明 ADT 类别直接影响冠状动脉粥样硬化的进展。但为什么 GnRH 激动剂可能比拮抗剂造成更多伤害?该领域的专家提出了几种机制理论。
FSH 假说
两种疗法之间的一个主要区别在于它们对卵泡刺激素 (FSH) 的影响。GnRH 激动剂最初会引起 LH 和 FSH 的激增,然后下调受体,但它们往往不能像 GnRH 拮抗剂那样完全或迅速地抑制 FSH 水平。一些临床前研究表明,FSH 受体在血管内皮细胞上表达,FSH 可能促进促炎途径和动脉壁内的脂质积累。
T 细胞活化和斑块稳定性
另一种理论涉及 T 细胞的作用。GnRH 受体存在于 T 淋巴细胞上。激动剂可能刺激这些受体,导致 T 细胞活化并随后释放使动脉粥样硬化斑块不稳定的细胞因子。拮抗剂通过阻断这些受体,可能防止这一炎症级联反应。这一点尤其相关,因为研究发现差异主要存在于非钙化斑块,这是最易受活动性炎症影响的亚型。
与 PRONOUNCE 试验的协调
临床医生可能会提到 PRONOUNCE 试验,该试验未能显示可注射拮抗剂地加瑞克与亮丙瑞林在 MACE 方面的差异。然而,专家指出,PRONOUNCE 可能样本量不足或受特定患者选择的限制。目前的研究使用了更敏感的替代标志物——斑块体积——可以在临床事件(如心肌梗死)发生前很长时间检测到生物变化。这表明,尽管 MACE 结果可能需要数年才能出现差异,但潜在病理在治疗开始后的前 12 个月内就开始发生变化。
结论:向心血管肿瘤学合作的转变
这项随机临床试验标志着我们对“心血管肿瘤学悖论”的理解向前迈出了一大步。通过证明 GnRH 激动剂亮丙瑞林与 relugolix 相比,冠状动脉斑块进展更大,该研究为在已有心血管疾病或高动脉粥样硬化风险的患者中选择 GnRH 拮抗剂提供了生物学依据。
对于泌尿科医生和放射肿瘤科医生,这些发现强调了在启动 ADT 之前进行心血管风险分层的重要性。对于心脏病学家,它突显了对接受 GnRH 激动剂治疗的患者进行密切监测的必要性。随着医疗界朝着更加个性化的护理方向发展,ADT 的选择不仅取决于肿瘤学疗效,还取决于保护患者心血管系统的需要。
未来的研究应关注这些基于成像的变化是否会在更广泛的人群中转化为长期临床结果的差异,以及积极的降脂治疗是否可以减轻 GnRH 激动剂引起的斑块进展。
资金和试验注册
该研究在亚特兰大乔治亚州一所学术机构的中心进行。数据分析于 2025 年 6 月完成。该试验在 ClinicalTrials.gov 注册,标识符为 NCT05320406。
参考文献
1. Patel SA, Yadalam AK, van Assen M, et al. 冠状动脉斑块在前列腺癌男性接受雄激素剥夺疗法后的进展:一项随机临床试验。JAMA Cardiology. 2026; doi:10.1001/jamacardio.2025.xxxx (2026 年 2 月 18 日发表)。
2. Shore ND, Saad F, Cookson MS, et al. 口服 relugolix 用于晚期前列腺癌的雄激素剥夺疗法 (HERO 试验)。N Engl J Med. 2020;382(23):2187-2196。
3. Lopes RD, Higano CS, Sloane EM, et al. 地加瑞克与亮丙瑞林在前列腺癌患者中的心血管安全性:PRONOUNCE 随机试验。Circulation. 2021;144(16):1295-1307。
4. Bhatia N, Santos M, Jones LW, et al. 雄激素剥夺疗法对前列腺癌男性的心血管影响。Circulation. 2016;133(19):1904-1914。