亮点
– 对两例猪到人心脏异种移植的多模式表型分析发现,早期内皮细胞激活和以先天免疫细胞(CD15+中性粒细胞和CD68+单核细胞/巨噬细胞)为主的轻度微血管炎症。
– 基因表达谱显示,与单核细胞/巨噬细胞激活、中性粒细胞激活、干扰素-γ反应、NK细胞负担、内皮细胞激活、凋亡和修复相关的通路上调——尽管毛细血管中未见C4d沉积,但其分子模式类似于抗体介导排斥。
– 观察到的表型在多个对照猪心脏中不存在,包括经历缺血/再灌注和脑死亡的野生型心脏,支持特定于异种的宿主反应。
– 多模式精准诊断平台(形态学、免疫表型、超微结构、自动多重免疫荧光和分子谱型)可以增强早期检测和机制理解,指导靶向干预。
背景
![]()
![]()
![]()
![]()
![]()
![]()
![]() 心力衰竭仍然是全球致病和致死的主要原因之一,而供体短缺是挽救生命移植的关键障碍。经过基因工程改造的猪器官已成为解决器官稀缺问题的近期主要解决方案。最近的临床级进展,包括多基因编辑供体猪和改进的围手术期护理,最终实现了首例报道的猪到人心脏异种移植。尽管取得了这些里程碑,但人类对猪心脏组织的免疫反应——即异种免疫反应——的性质和时间仍未完全明确。了解再灌注后早期组织水平事件对于区分预期的缺血/再灌注(I/R)变化和真正的排斥反应至关重要,以优化监测并设计适当的靶向免疫调节策略。
心力衰竭仍然是全球致病和致死的主要原因之一,而供体短缺是挽救生命移植的关键障碍。经过基因工程改造的猪器官已成为解决器官稀缺问题的近期主要解决方案。最近的临床级进展,包括多基因编辑供体猪和改进的围手术期护理,最终实现了首例报道的猪到人心脏异种移植。尽管取得了这些里程碑,但人类对猪心脏组织的免疫反应——即异种免疫反应——的性质和时间仍未完全明确。了解再灌注后早期组织水平事件对于区分预期的缺血/再灌注(I/R)变化和真正的排斥反应至关重要,以优化监测并设计适当的靶向免疫调节策略。
研究设计
目的
使用集成多模式诊断管道,表征猪到人心脏异种移植早期异种免疫损伤的组织学、细胞学、超微结构和转录组特征。
受试者和样本
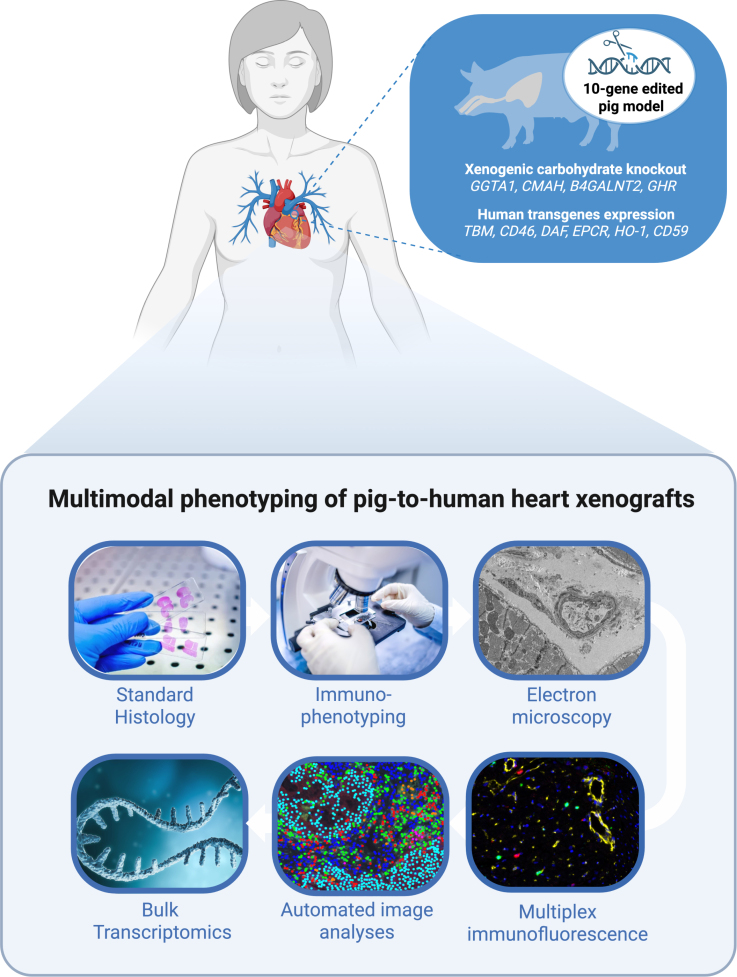
两例正位猪到人心脏异种移植,来自10基因编辑供体猪,移植至脑死亡人体受者。在再灌注后66小时收集心肌活检标本。对照组织包括植入前取样的供体异种移植和在有或无脑死亡及有或无缺血/再灌注损伤条件下获得的多个野生型猪心脏。
方法
对66小时活检标本应用多模式表型分析:常规组织病理学、免疫表型、电子显微镜(超微结构)、深度学习支持的自动量化多重免疫荧光(mIF)和基因表达谱型(整体/转录组)。组合方法使形态学、细胞类型组成、微解剖和分子通路之间能够进行关联。
主要发现
1. 形态学和微血管炎症
两例异种移植活检标本均表现出内皮细胞激活和轻度微血管炎症。经典的毛细血管C4d沉积,即同种移植中补体激活和抗体介导排斥的经典标志,在此缺失。光镜显示局部微血管白细胞聚集,但在这一早期时间点未见广泛的心肌细胞坏死。
2. 细胞组成:先天免疫为主
免疫表型和自动mIF定量识别出CD15+细胞(主要是中性粒细胞)和CD68+细胞(单核细胞/巨噬细胞)为主要炎症细胞类型,存在于微血管和血管周围空间。66小时时,淋巴细胞群体(CD3+ T细胞、CD20+ B细胞)相对较少。
3. 超微结构特征
电子显微镜显示内皮细胞肿胀和激活,偶尔可见血管内白细胞黏附或部分跨内皮迁移。此时未见一致的补体介导膜攻击复合物的超微结构证据。
4. 分子特征与抗体介导和先天激活一致
转录组谱型显示,与单核细胞/巨噬细胞激活、中性粒细胞脱颗粒/激活、干扰素-γ反应、NK细胞负担、内皮细胞激活、凋亡和组织修复途径相关的基因集上调。这些途径共同类似于在人同种移植中描述的抗体介导排斥(AMR)的分子模式,尽管组织学上未见C4d。
5. 对照组未复制异种移植表型
所有对照猪心脏——包括经历脑死亡和缺血/再灌注损伤的野生型心脏——均缺乏在异种移植中观察到的复合分子和细胞特征。这表明观察到的表型与物种差异和/或宿主对猪抗原的反应有关,而不是非特异性移植相关损伤。
6. 解释性综合
综合多模式数据描述了一种早期、以先天免疫为主的异种免疫反应,特征为内皮细胞激活和以中性粒细胞和巨噬细胞为主的微血管炎症。分子模式类似于AMR,暗示早期异种移植后可能涉及体液机制、Fc受体介导的效应功能、补体独立的抗体途径或混合的先天-体液相互作用。
专家评论和机制考虑
研究结果在生物学上合理,并与再灌注后早期显著先天免疫参与的临床前异种移植工作一致。关键机制点:
– 内皮细胞激活是哨兵事件。内皮细胞表达物种特异性碳水化合物和蛋白质抗原,可被预先形成的天然抗体和诱导的体液反应识别。即使在经典补体沉积(C4d)缺失的情况下,抗体也可以驱动Fc介导的髓系细胞激活,或触发补体独立的内皮信号传导,导致粘附分子和趋化因子的上调,从而招募中性粒细胞和单核细胞。
– 先天细胞作为效应器。中性粒细胞和单核细胞衍生的巨噬细胞是对组织损伤和外来抗原的快速反应者。它们可以介导微血管阻塞、活性氧释放和细胞因子产生,放大移植物损伤并随时间招募适应性效应器。
– 无C4d的分子AMR特征。干扰素-γ反应、NK细胞负担和巨噬细胞激活的组合特征是通过Fc受体或补体独立机制作用的供体特异性抗体(DSA)介导的抗体过程。需要连续时间进程研究来阐明补体激活是否在后期变得更加显著。
需要考虑的局限性:
– 样本量小(两例异种移植)和单一早期时间点(66小时)限制了普遍性和时间解释。
– 受者处于脑死亡状态,这种生理状态可以改变全身炎症和血流动力学;这可能加剧或修改与活体受者相比的观察到的反应成分。
– 供体猪进行了10基因编辑;特定基因编辑组合可以影响抗原性和先天免疫相互作用。研究报告了编辑,但每种编辑对观察到的表型的相对贡献尚不清楚。
临床和转化意义
1. 诊断策略:研究展示了将常规组织学与定量mIF和分子谱型结合的价值,以检测可能被单模式评估遗漏的早期异种免疫特征。对于未来的临床异种移植项目,标准化多模式监测(包括早期时间点的协议活检和靶向分子面板)可以改善早期检测和损伤的机制分类。
2. 治疗靶点:研究结果强调了除标准T细胞定向免疫抑制之外的潜在靶点:策略包括减少先天髓系招募/激活(巨噬细胞抑制剂、中性粒细胞CXCR2途径阻断),调节Fc受体信号传导,以及内皮稳定剂(抗炎内皮调节剂、如果补体激活在后期出现则使用补体抑制剂)。早期先天途径的突出表明,针对先天免疫的围手术期方案可能至关重要。
3. 生物标志物:这里确定的分子特征成分可以为开发非侵入性生物标志物(血浆特征、供体来源的游离DNA模式或血清细胞因子)提供信息,以补充组织监测并减少对侵入性活检的依赖。
4. 研究重点:关键下一步包括在活体受者中进行连续采样,与循环中的DSA和补体激活产物相关联,并在不同基因编辑组合之间进行对照比较,以绘制哪些编辑实质性地影响早期异种免疫级联。
结论
这项对两例猪到人心脏异种移植在再灌注后66小时的详细多模式分析记录了早期异种免疫表型,特征为内皮细胞激活和轻度、以先天细胞为主的微血管炎症,伴有类似抗体介导损伤的转录程序。该表型与暴露于缺血/再灌注和脑死亡的对照猪心脏不同,支持特定于异种的宿主反应。这些观察结果强调了在临床异种移植项目中整合组织学、高级免疫表型、超微结构和分子谱型的精准诊断的必要性,并指出先天免疫和内皮细胞定向干预作为传统免疫抑制的重要补充。
资金和临床试验注册
作者在主要出版物(Giarraputo等,Circulation 2025)中报告了资金和试验注册详情。本摘要中未提供clinicaltrials.gov标识符;读者应查阅原始文章以获取完整的资金、利益冲突和监管信息。
参考文献
Giarraputo A, Morgand E, Stern J, Mezine F, Coutance G, Goutaudier V, Sannier A, Certain A, Hauet T, Giraud S, Kerforne T, Allain G, Ayares D, Khalil K, Kim J, Mehta S, Narula N, Reyentovich A, Smith D, Tissier R, Saraon T, Kadosh B, Divita M, Goldberg R, Pass H, Mangiola M, Bruneval P, Griesemer A, Moazami N, Montgomery RA, Loupy A. 使用多模式诊断系统表征猪到人心脏异种移植的免疫反应。Circulation. 2025年12月2日;152(22):1552-1563. doi: 10.1161/CIRCULATIONAHA.125.074971 . Epub 2025年10月2日。PMID: 41036838 ;PMCID: PMC12655869 。