亮点
- 与同步给药相比,序贯派姆单抗(在放化疗后)显著改善了局部晚期头颈癌患者的4年局部区域控制(LRC)。
- 两种治疗策略均达到了疗效和安全性标准,但序贯治疗在无进展生存期和总生存期方面显示出数值上的优势。
- 基于派姆单抗给药时间的不同,在肿瘤微环境中观察到了不同的免疫抑制变化,这可能为未来的免疫治疗策略提供信息。
- 这项随机II期试验解决了关于在高风险HNSCC中如何最佳整合免疫治疗与标准放化疗的关键问题。
研究背景和疾病负担
头颈鳞状细胞癌(HNSCC)是一组具有高度侵袭性的恶性肿瘤,尤其在局部晚期阶段,其发病率和死亡率较高。尽管标准的同步放化疗(CRT)联合顺铂治疗,但疗效仍不理想,存在显著的局部区域和远处失败风险。免疫检查点抑制剂(如派姆单抗)的出现改变了复发/转移性疾病的治疗格局。然而,对于新诊断的局部晚期疾病,派姆单抗与CRT的最佳联合时机尚不清楚。这个问题具有重要的临床意义,因为整合免疫治疗可以增强肿瘤控制,但也可能增加重叠的毒性和潜在的免疫抑制相互作用。
研究设计
这是一项随机、开放标签的II期试验(NCT02777385),共纳入80名新诊断的局部晚期HNSCC患者(主要是IV期,T4和/或N2疾病)。入选标准包括HPV阳性和HPV阴性肿瘤。患者按HPV状态和N分期分层,并以1:1的比例随机分配至:
- 同步组:派姆单抗200 mg每3周一次,共8个周期,从CRT开始前1周开始(顺铂40 mg/m²每周一次 + 放疗70 Gy)
- 序贯组:派姆单抗200 mg每3周一次,共8个周期,从CRT完成后2周开始
主要复合终点要求每个组达到以下三个标准:1年局部区域失败(LRF)率<60%,1年无进展生存期(PFS)≥60%,剂量限制性毒性≤20%。如果两个组都达到这些标准,则1年PFS较高的组被认为是优胜者(选择优胜者设计)。次要终点包括4年局部区域控制(LRC)、PFS、总生存期(OS)以及肿瘤微环境(TME)变化的转化分析。
主要发现
患者群体:80名患者接受治疗(41名同步组,39名序贯组),其中92.5%为IV期疾病,伴有大量和/或淋巴结阳性的肿瘤。
疗效结果:
- 两个组均达到了预设的主要疗效和安全性终点:1年LRF(同步组26%,序贯组13%),1年PFS(同步组60%,序贯组74%),剂量限制性毒性(均≤20%)。
- 4年局部区域控制(LRC):序贯组的LRC显著优于同步组(96% vs 64%;HR 0.11,95% CI 0.01–0.89,P=0.012)。
- 4年无进展生存期(PFS):序贯组的PFS数值上更高(69% vs 49%;HR 0.55,95% CI 0.25–1.22,P=0.132),但无统计学差异。
- 4年总生存期(OS):序贯组在数值上优于同步组(83% vs 71%;HR 0.51,95% CI 0.19–1.37,P=0.17)。
- 在接受最佳顺铂剂量(≥200 mg/m²)的患者中,序贯组的4年LRC仍然优于同步组(96% vs 73%;HR 0.17,95% CI 0.02–1.43,P=0.063)。
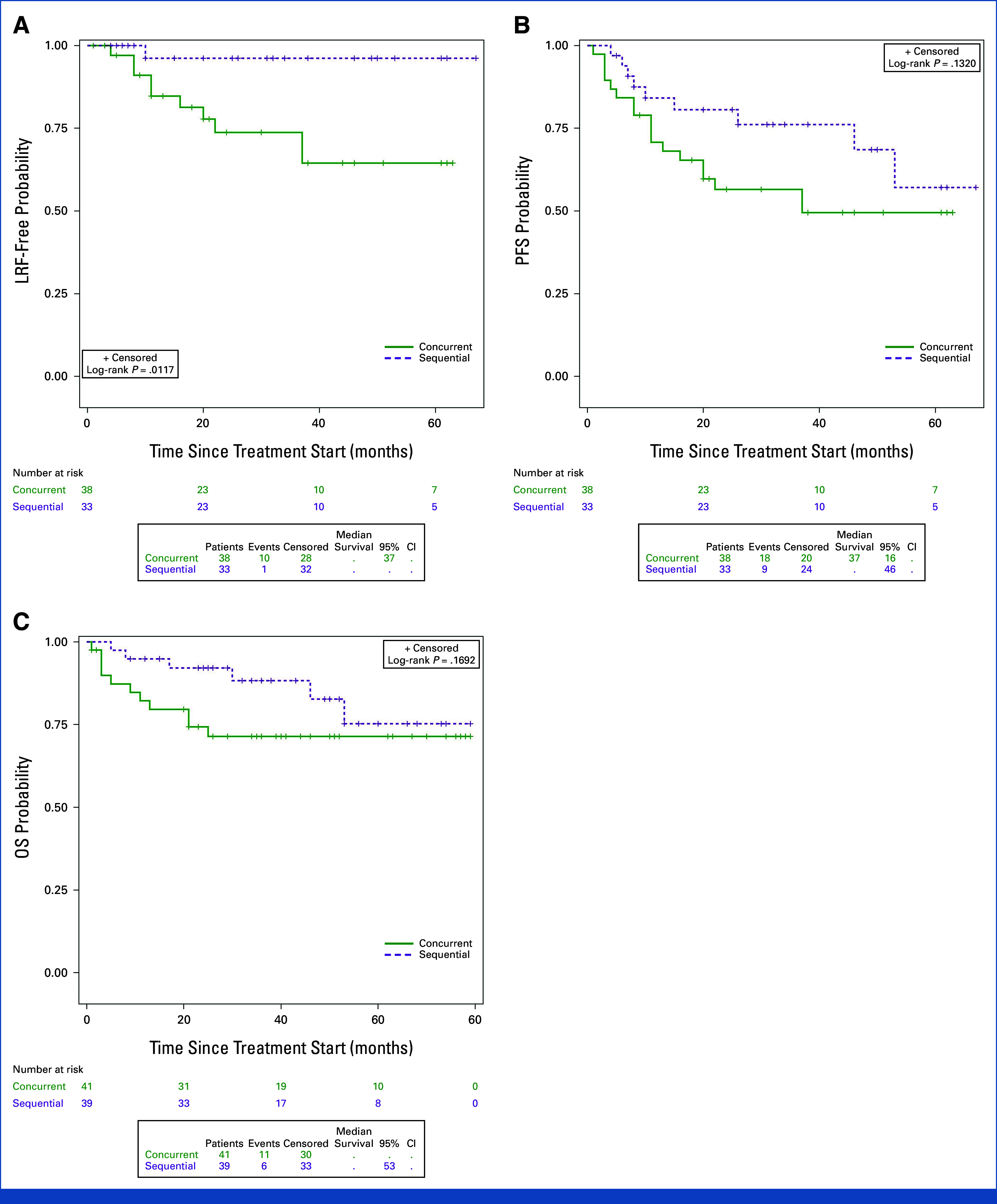
Evaluation of outcomes by treatment arm.
失败模式:序贯组的大多数进展为远处进展(5/6),而同步组则表现为更多的局部区域失败(8/12)。
安全性:两种策略的毒性均可管理,未发现意外的安全信号或显著的依从性差异。
转化见解:肿瘤活检显示,同步组的巨噬细胞、PD-L1+巨噬细胞和PD-L1+肿瘤细胞显著增加,而序贯组则没有这种变化,表明早期派姆单抗暴露前的CRT可能导致TME中早期的免疫抑制变化。
专家评论
该试验提供了首个随机证据,证明相对于CRT,免疫检查点抑制剂的给药顺序对高风险HNSCC的长期局部区域控制有显著影响。尽管同步组的初始应答率较高,但其LRC较差,这表明早期派姆单抗引起的TME免疫抑制变化可能抵消潜在的益处。相比之下,推迟免疫治疗直到CRT之后,可能允许恢复抗肿瘤免疫,利用放疗和化疗的免疫原性效应。重要的是,两种方法都是可行且安全的,但只有序贯组实现了持久的控制。
这些发现挑战了简单地将免疫治疗添加到标准CRT方案的趋势,并强调了优化这些模式的时间整合机制和临床研究的必要性。局限性包括相对较小的样本量和需要在更大规模的III期试验中验证。两组之间TME生物学的差异为未来的相关研究和生物标志物开发提供了宝贵的基础。
结论
在局部晚期HNSCC患者中,序贯派姆单抗联合放化疗在长期局部区域控制方面显著优于同步给药,且在无进展生存期和总生存期方面有有利趋势。该试验突显了治疗顺序的重要性,并为进一步研究CRT后的免疫治疗策略提供了依据。这些结果可能为未来指南和个人化治疗策略的制定提供信息。
参考文献
1. Zandberg DP, Vujanovic L, Clump DA, et al. Randomized Phase II Study of Concurrent Versus Sequential Pembrolizumab in Combination With Chemoradiation in Locally Advanced Head and Neck Cancer. J Clin Oncol. 2025 Aug 10;43(23):2572-2582. doi: 10.1200/JCO-24-01580 . Epub 2025 May 27. PMID: 40424564 ; PMCID: PMC12316147 .2. ClinicalTrials.gov Identifier: NCT02777385.