亮点
- Obrixtamig(BI 764532),一种DLL3/CD3 IgG样T细胞接合剂,在DLL3阳性小细胞肺癌和神经内分泌癌患者的I期剂量递增研究中进行了评估。
- 该研究探索了多种给药方案,包括逐步增加剂量策略,建立了耐受性而未达到最大耐受剂量。
- 与治疗相关的细胞因子释放综合征常见但大多可管理和可逆。
- 所有队列的总体缓解率为23%,其中肺大细胞神经内分泌癌的缓解率最高(70%)。
- 结果支持对这些难以治疗的DLL3表达肿瘤进行进一步临床研究。
研究背景和疾病负担
小细胞肺癌(SCLC)和肺外神经内分泌癌(epNEC),包括肺大细胞神经内分泌癌(LCNEC-L),代表具有较差预后和有限治疗选择的侵袭性恶性肿瘤,尤其是在多线治疗后。DLL3(Notch配体3)是SCLC和相关神经内分泌癌中过表达的抑制性Notch配体,但在正常组织中几乎不存在,使其成为有吸引力的治疗靶点。当前的治疗方法效果有限,持久反应罕见,因此需要新的策略。奥布里克塔米格(BI 764532)是一种双特异性T细胞接合剂,设计用于将CD3阳性T细胞重定向至DLL3表达的肿瘤细胞,以触发免疫介导的细胞毒性,提供了一种新的免疫治疗手段来治疗DLL3阳性肿瘤。
研究设计
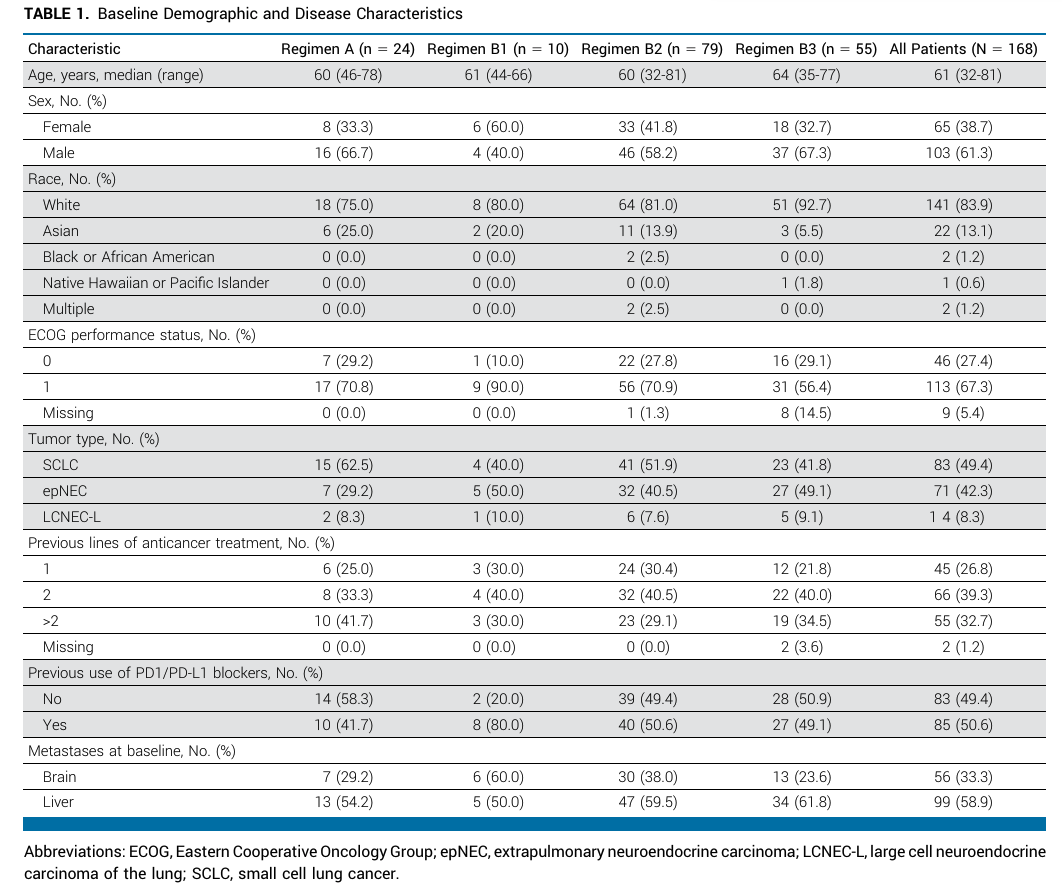
这项首次人体、开放标签、多中心剂量递增I期试验招募了168名先前接受过治疗的DLL3阳性SCLC、epNEC或LCNEC-L患者。符合条件的患者大多已经接受过多线系统治疗,包括免疫检查点抑制剂(51%)。
Obrixtamig通过静脉注射使用四种给药方案:
– 方案A:每3周固定剂量一次
– 方案B1:每周固定剂量一次
– 方案B2:前2周每周逐步增加剂量,然后每周目标剂量
– 方案B3:前3周每周逐步增加剂量,随后每周目标剂量3周,之后每3周一次
主要目标是确定最大耐受剂量(MTD)。次要目标包括安全性分析、药代动力学评估和根据RECIST 1.1标准评估肿瘤反应。
关键发现
在168名患者中,72%至少接受过两次抗癌治疗,反映了重度预治疗的人群。在MTD评估期间发生了7例剂量限制性毒性(DLTs)——方案A中1例,方案B2中6例——但未达到MTD。
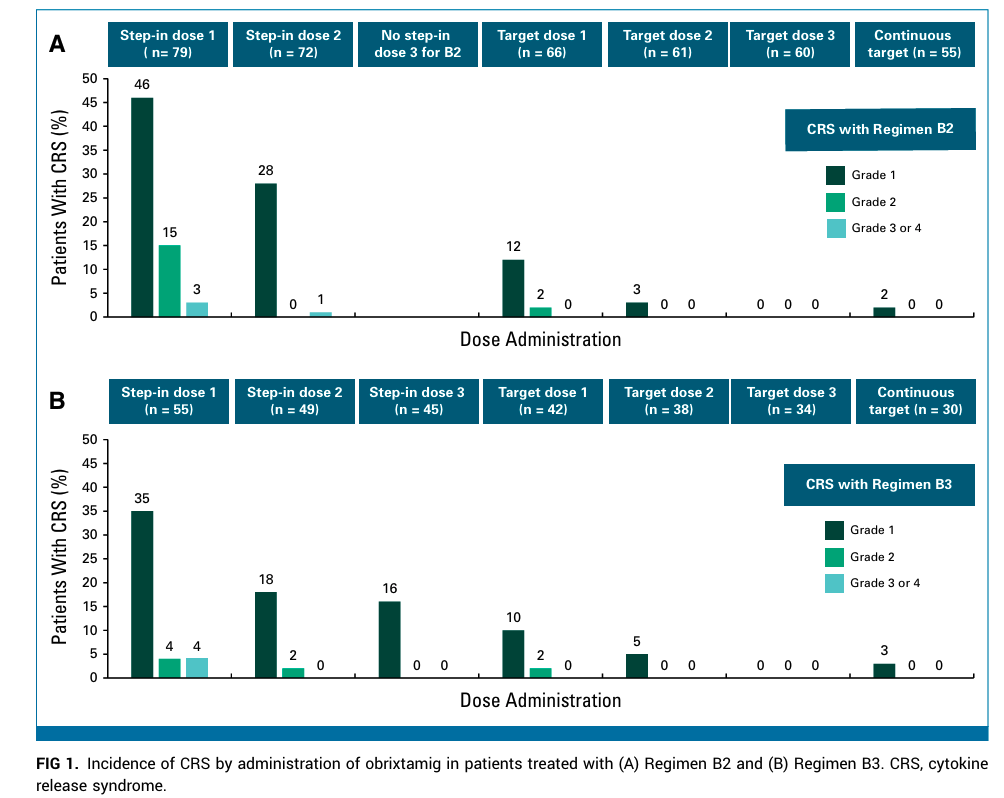
最常见的治疗相关不良事件(AE)是细胞因子释放综合征(CRS),在各方案中发生率为57%。然而,3级或更高级别的CRS仅在3%的患者中观察到,症状通常在治疗早期出现,并且在适当管理下可逆。其他不良事件与T细胞接合剂的预期安全性一致。
结合所有方案和肿瘤类型的疗效分析显示,总体缓解率(ORR)为23%(95%置信区间[CI],17.4%至30.2%)。中位缓解持续时间(DoR)为8.5个月(95% CI,6.2至未达到),6个月DoR率为70%(95% CI,53%至88%),表明对反应者具有持久的临床获益。
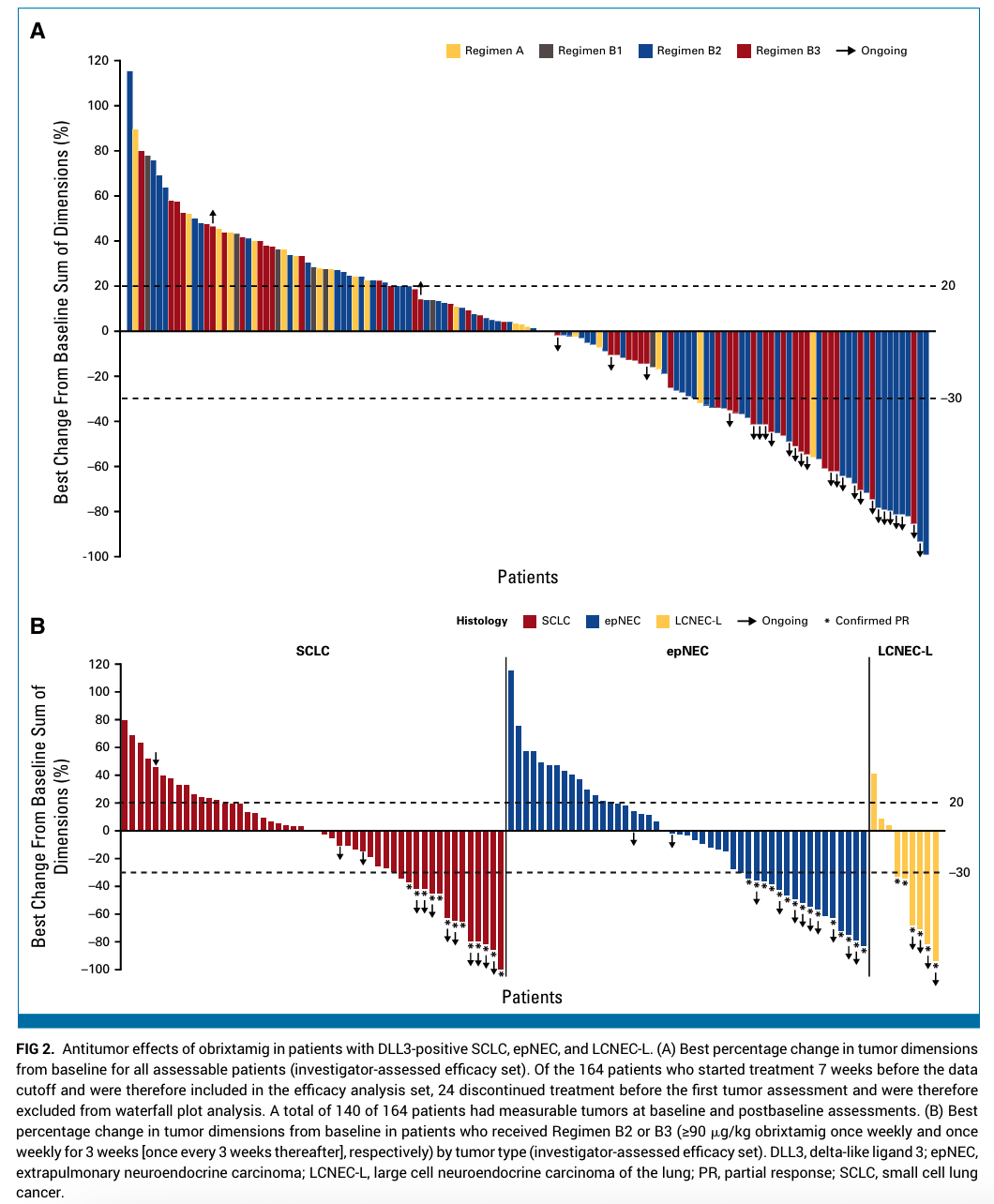
在使用方案B2/B3接受最小有效剂量(≥90 μg/kg)的患者中,ORR提高到28%(95% CI,20.7%至35.9%),表明优化的给药策略增强了疗效。
方案B2/B3的肿瘤特异性缓解率为:
– 小细胞肺癌:21% ORR(95% CI,12.9%至33.1%)
– 肺外神经内分泌癌:27% ORR(95% CI,17.4%至39.6%)
– 肺大细胞神经内分泌癌:70% ORR(95% CI,39.7%至89.2%)
这些发现表明显著的抗肿瘤活性,特别是在LCNEC-L亚型中,这种亚型之前缺乏有效的治疗方法。
药代动力学评估显示血浆浓度呈剂量比例增加,支持所使用的给药方案。
专家评论
Obrixtamig的I期结果代表了针对DLL3这一临床上难以利用的抗原的免疫治疗进展。可控的安全性特征,主要是轻度至中度CRS早期解决,与已知的T细胞接合剂的毒性相符。值得注意的是,尽管观察到DLTs,但未达到MTD,这表明其治疗窗口相对较宽。
在重度预治疗的患者群体中(包括那些先前接受过抗PD-1/PD-L1治疗的患者)的持久反应突显了Obrixtamig作为新型治疗模式的潜在临床意义。LCNEC-L中的显著缓解率尤其引人注目,因为这种侵袭性癌症的有效治疗方法很少。
本研究的局限性包括其早期阶段设计和缺乏对照组,这需要谨慎解读。进一步的II/III期试验对于确认疗效、定义最佳给药方案和探索联合方法至关重要,可能增强获益。
从机制上讲,Obrixtamig的双特异性结合能够直接招募细胞毒性T细胞到肿瘤部位,绕过常规抗原呈递过程,可能克服神经内分泌肿瘤中常见的肿瘤免疫逃逸策略。
结论
这项Obrixtamig的I期剂量递增试验展示了在重度预治疗的DLL3阳性小细胞肺癌和神经内分泌癌患者中具有前景的耐受性和初步疗效。逐步增加剂量方案最终每周或三周一次的目标剂量在90至1080 μg/kg之间表现出可控的安全性和23%的总体缓解率,缓解具有显著的持久性。
肺大细胞神经内分泌癌中的特别高缓解率值得进一步集中研究。这些结果证明了正在进行和未来的临床试验的合理性,以更好地定义Obrixtamig的治疗作用并优化其在DLL3表达的神经内分泌恶性肿瘤治疗范式中的整合。
参考文献
Wermke M, Gambardella V, Kuboki Y, Felip E, Sanmamed MF, Alese OB, Sayehli CM, Arriola E, Wolf J, Villaruz LC, Bertulis J, Studeny M, Bouzaggou M, Fang X, Morgensztern D. Delta-Like Ligand 3/CD3 IgG-Like T-Cell Engager Obrixtamig (BI 764532) in Patients With Delta-Like Ligand 3+ Small Cell Lung Cancer or Neuroendocrine Carcinomas: Phase I Dose-Escalation Results. J Clin Oncol. 2025 Sep 20;43(27):3021-3031. doi: 10.1200/JCO-25-00363 IF: 41.9 Q1 . Epub 2025 Jul 24. PMID: 40706016 IF: 41.9 Q1 ; PMCID: PMC12440289 IF: 41.9 Q1 .
额外支持文献:
– Rudin CM, et al. Small cell lung cancer. Nat Rev Dis Primers. 2021;7(1):3.
– Stewart CA, et al. Targeting DLL3 in pulmonary neuroendocrine tumors. Cancer Immunol Res. 2020;8(2):177-182.
– Sigma-Aldrich T-Cell Engager Mechanism Review. ImmunoOncology. 2023;9(4):254-263.