亮点
– 暴露于某些抗生素(不包括大环内酯类和青霉素类)与接受帕博利珠单抗治疗的晚期非小细胞肺癌患者的总生存期(OS)降低相关。
– 对于帕博利珠单抗单药治疗,皮质类固醇剂量超过20毫克泼尼松当量,以及与化疗联合使用时剂量超过30毫克泼尼松当量,均与较差的生存率相关。
– 质子泵抑制剂(PPIs)独立地与该患者群体的较差总生存期相关。
– 这些发现强调了仔细评估联合用药以优化免疫治疗效果的必要性。
研究背景和疾病负担
非小细胞肺癌(NSCLC)是最常见的肺癌类型,是全球癌症相关死亡的主要原因。免疫检查点抑制剂(如帕博利珠单抗,一种程序性死亡受体1(PD-1)抑制剂)的出现已经改变了晚期非小细胞肺癌的一线治疗,改善了生存结果。然而,治疗效果在患者之间存在显著差异,不仅受到肿瘤分子特征的影响,还受到宿主因素(包括同时使用的药物)的影响。
抗生素、全身性皮质类固醇和质子泵抑制剂(PPIs)常用于各种合并症或癌症相关症状的癌症患者。越来越多的证据表明,这些药物可能通过改变肠道微生物群、调节免疫反应或影响药物代谢而对免疫检查点抑制剂的疗效产生负面影响。然而,关于这些药物与接受帕博利珠单抗治疗的晚期非小细胞肺癌患者生存结果之间的关联的人口规模数据有限。
研究设计
在这项大规模、全国性的回顾性队列研究中,研究人员利用法国国家医疗保健数据库中的目标试验模拟方法,考察了联合用药对晚期非小细胞肺癌总生存期的影响。纳入了2015年1月至2022年12月期间新诊断并开始一线帕博利珠单抗治疗且在治疗开始后两个月内仍然存活的患者。
排除标准排除了因感染性疾病、自身免疫性疾病或消化性溃疡住院的患者,以避免因研究的联合用药指征引起的混杂偏倚。
药物暴露定义如下:抗生素和PPI暴露要求从帕博利珠单抗开始日期前60天到后42天内至少有两次处方;皮质类固醇暴露要求从帕博利珠单抗开始日期前30天到后30天内至少有两次处方。皮质类固醇剂量强度也根据泼尼松当量每日剂量进行了评估。
主要终点是总生存期(OS)。采用逆概率治疗加权(IPTW)分析方法,在比较暴露组和未暴露组的结果时最小化混杂偏倚。
关键发现
研究人群包括41,529名接受一线帕博利珠单抗治疗的晚期非小细胞肺癌患者:其中男性27,826人(67%),中位年龄65岁(范围19-97岁)。其中,35.7%的患者接受了帕博利珠单抗单药治疗,而64.3%的患者接受了帕博利珠单抗联合化疗。
Figure 1. Weighted Distribution by Antibiotc, Steroid, or Proton Pump Inhibitor (PPI) Exposure.

在治疗开始时,41.9%的患者暴露于抗生素,59.1%的患者暴露于皮质类固醇,53.7%的患者暴露于PPIs。
抗生素: 经IPTW调整后,抗生素的使用与总生存期(OS)的适度但具有统计学意义的降低相关(风险比[HR] 1.08,95%置信区间[CI] 1.05-1.12;P < .001)。然而,这种关联并不是所有抗生素类别都一致——大环内酯类和青霉素类抗生素未显示对生存的不良影响,这表明抗生素类型可能存在异质性,可能与不同的微生物群破坏或免疫调节有关。
Figure 2. Assocications of Overall Survival (OS) With Antibiotic Exposure Among Those Receiving Pembrolizumab Alone and Pembrolizumab Plus Chemotherapy.

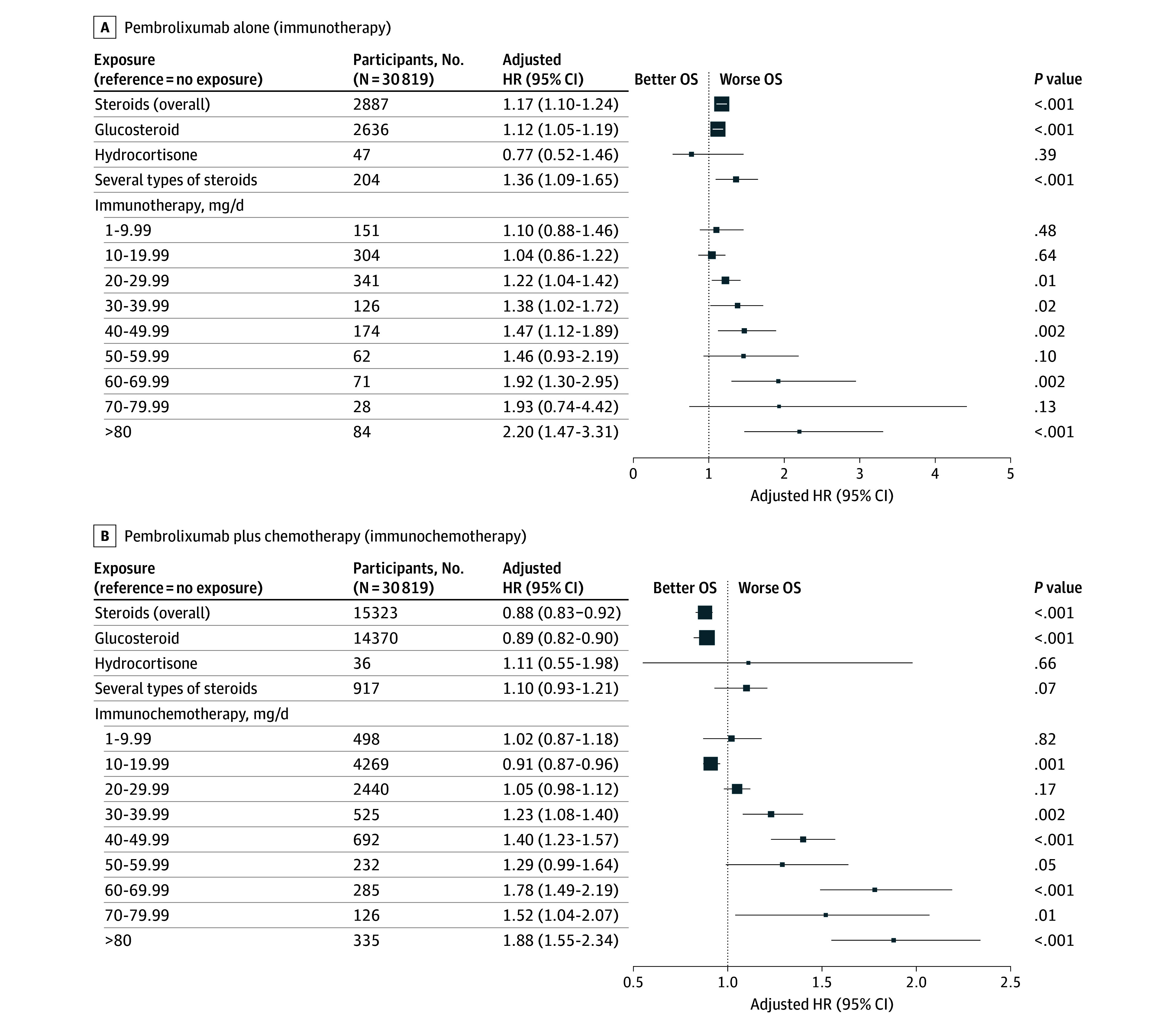
皮质类固醇: 总体皮质类固醇暴露与OS无显著相关性(HR 0.98,95% CI 0.95-1.02;P = .37)。然而,与帕博利珠单抗方案(单药治疗与联合化疗)之间发现了显著的交互作用(P < .001)。剂量依赖性分析显示,较高泼尼松当量剂量的生存情况恶化:>20毫克/天与单药治疗患者的不良结局相关(趋势P值 = .005),>30毫克/天与联合治疗患者的不良结局相关(趋势P值 < .001)。这表明较高剂量的皮质类固醇对免疫治疗期间的抗肿瘤免疫功能产生了免疫抑制作用。
Figure 3. Associations of Overall Survival (OS) With Steroid Exposure Among Those Receiving Pembrolizumab Alone and Pembrolizumab Plus Chemotherapy.
质子泵抑制剂(PPIs): PPI的使用与显著较差的OS相关(HR 1.13,95% CI 1.10-1.17;P < .001),与先前报告的PPI干扰肠道微生物群和损害免疫检查点抑制剂疗效的观点一致。
Figure 4. Proton Pump Inhibitor (PPI) Exposure and Overall Survival (OS).
专家评论
这项大型真实世界分析扩展了此前较小的研究,将联合用药与免疫治疗结果联系起来,提供了关于类别特异性和剂量依赖性效应的详细见解。观察到的抗生素类别效应符合微生物群扰动影响免疫治疗效果的假设。确定的皮质类固醇剂量阈值有助于细化临床决策,平衡症状控制和免疫保护。
尽管采用了复杂的IPTW调整,作为一项回顾性观察研究,仍可能存在残余混杂偏倚。无法完全排除因指示引起的混杂——需要这些药物的患者可能本身预后较差或疾病表现更为严重。研究排除某些合并症的措施减轻了但并未消除这一风险。
机制上,抗生素和PPIs可能损害对启动抗肿瘤T细胞反应至关重要的有益共生肠道细菌。高剂量皮质类固醇会减弱T细胞功能和对检查点阻断机制至关重要的细胞因子产生。未来需要进行前瞻性和机制研究,以充分阐明因果关系。
结论
这项全面的全国性队列研究表明,某些抗生素、高剂量皮质类固醇和PPIs与一线使用帕博利珠单抗治疗的晚期非小细胞肺癌患者的总生存期减少相关。这些发现强调了在进行免疫治疗时谨慎开具处方和密切监测联合用药的迫切需求。
临床医生应仔细评估抗生素和皮质类固醇的指征、选择和剂量,并在可能的情况下重新考虑PPI的使用,以优化免疫治疗效果。这些结果进一步证实了通过联合用药调节宿主和微生物群显著影响免疫检查点抑制剂有效性的证据。
正在进行的研究应整合微生物组谱型、免疫表型和前瞻性干预试验,以开发减轻负面联合用药效应并增强个性化癌症免疫治疗的策略。
参考文献
Rousseau A, Simon-Tillaux N, Michiels S, 等. 非小细胞肺癌一线使用帕博利珠单抗治疗期间联合用药与生存的关系. JAMA Netw Open. 2025;8(9):e2529225. doi:10.1001/jamanetworkopen.2025.29225。
Derosa L, Routy B, Kroemer G, Zitvogel L. 微生物组与免疫治疗:诊断和治疗潜力. Gastroenterology. 2021;160(7):2023-2041。
Arbour KC, Mezquita L, Long N, 等. 基线皮质类固醇对非小细胞肺癌患者程序性细胞死亡-1和程序性死亡配体1阻断疗效的影响. J Clin Oncol. 2018;36(28):2872-2878。
Pinato DJ, Howlett S, Ottaviani D, 等. 既往抗生素使用与癌症患者免疫检查点抑制剂治疗生存和反应的关系. JAMA Oncol. 2019;5(12):1774-1778。