自闭症谱系障碍(ASD)是一种复杂的神经发育障碍,特征是社交沟通和互动能力受损以及存在限制性和重复性行为。尽管ASD的病因尚未完全明了,但肠道微生物群失调(称为菌群失衡)已成为影响受累个体胃肠道(GI)和神经行为症状的有趣因素。ASD儿童常伴有胃肠道合并症,如便秘、腹泻和腹痛,这些症状可能加剧行为问题并影响整体生活质量。粪菌移植(FMT),即将健康供体的粪便衍生微生物转移到受者体内,作为针对菌群失衡以缓解ASD症状的潜在干预措施引起了关注。本文系统回顾了FMT在ASD儿童和青少年中的疗效和安全性,综合分析了随机对照试验(RCTs)和观察研究的结果,以指导临床实践和未来研究。
研究设计
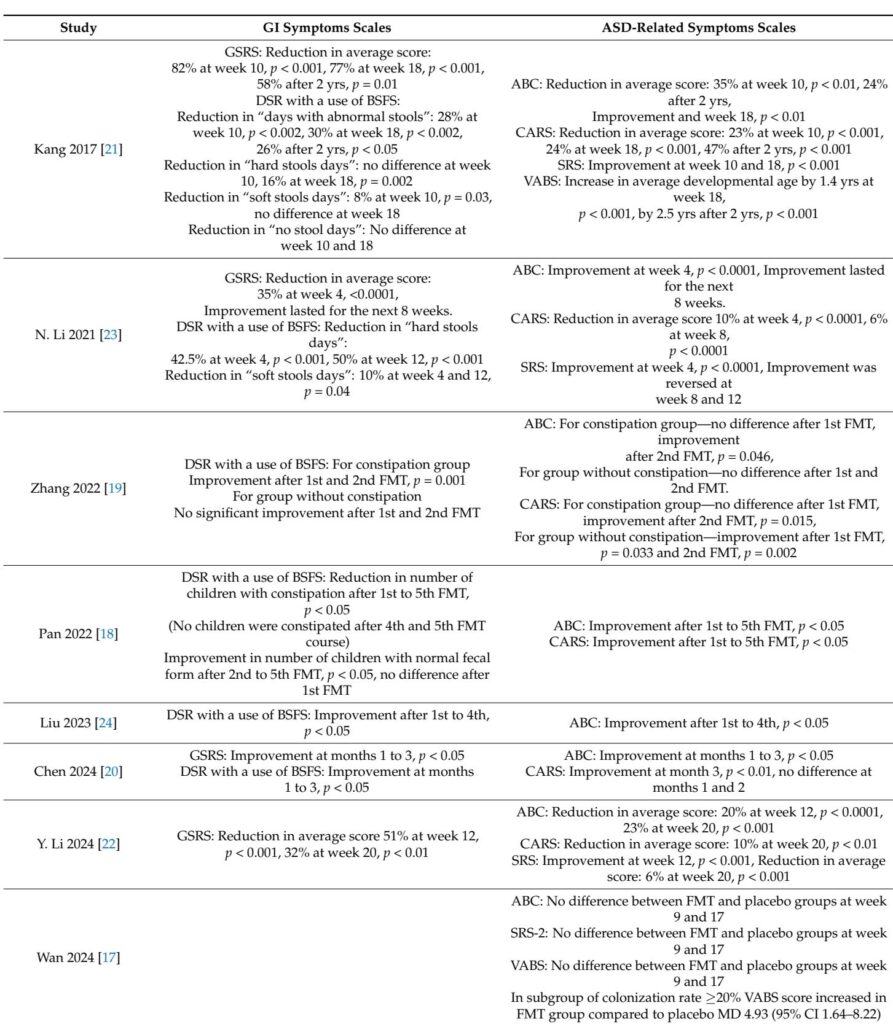
本综述包括两项双盲安慰剂对照RCT和七项前后对照研究,评估FMT在儿科ASD人群中的应用。参与者年龄在2至17岁之间,主要为男性,并根据标准诊断标准(DSM-5、ADOS-2或ADI-R)确诊。干预措施在FMT制备(冻干、冷冻或洗涤粪便材料)、给药途径(口服胶囊、鼻空肠、结肠镜或经内镜肠道)和给药方案上差异较大。一些研究纳入了肠道清洁和抗生素预处理等准备步骤,但协议各异。结果集中在通过布里斯托尔大便表(BSFS)和胃肠道症状评分量表(GSRS)评估的胃肠道症状,以及使用经过验证的量表(如异常行为清单(ABC)、儿童自闭症评定量表(CARS)、社会反应量表(SRS)和文兰适应行为量表(VABS))测量的ASD相关行为。安全性终点包括报告的不良事件。
关键发现
大多数前后对照研究报道,FMT后胃肠道和行为症状均有显著改善,表现为大便不规律、便秘率和GSRS评分的减少,显示出临床上有意义的胃肠道症状缓解。行为改善反映在ABC和CARS得分下降以及通过SRS和VABS测得的社会功能增强。值得注意的是,Kang等人记录了治疗后长达两年的症状持续改善和微生物多样性的增加。
RCT结果不一。Wang等人观察到FMT组与安慰剂组相比,胃肠道症状有显著改善,同时CARS和SRS的行为评分也有改善,但ABC评分无显著差异。相比之下,Wan等人发现FMT组与安慰剂组在ASD症状评分上无显著差异,但高供体微生物嵌合率的亚组表现出更好的社会适应性结果。两项RCT均证实了FMT的安全性,仅报告了类似于安慰剂的轻微、短暂的不良事件。
跨研究的微生物组分析显示,α多样性增加,有益菌群向富含双歧杆菌、普雷沃氏菌和其他与肠道健康相关的菌群转变。微生物组成与代谢标志物(包括短链脂肪酸和神经递质代谢物)之间的关联提示了FMT对神经行为影响的机制。
尽管有令人鼓舞的信号,但研究的局限性包括样本量小、协议异质性、依赖于易受偏倚影响的家长报告结果测量以及大多数研究的随访时间较短。缺乏标准化的FMT制备和给药方法,以及对预处理抗生素或肠道清洁的使用不一致,使直接比较和普遍适用性复杂化。
专家评论
肠道-大脑轴为FMT在ASD中的治疗原理提供了生物学上的合理框架,恢复微生物平衡可能减轻神经炎症过程并改善肠道屏障完整性,从而影响行为症状。然而,方法学限制和不一致的RCT结果抑制了热情,并强调了优化和标准化临床试验设计的关键需求。未来的研究应优先考虑客观的临床医生管理的行为评估,如自闭症诊断观察计划,并延长随访时间以评估持久性。此外,明确肠道清洁和抗生素等预处理方案的作用至关重要,因为来自其他临床背景的新兴证据表明,这些可能影响微生物嵌合和治疗成功。同时评估饮食因素和习惯性微生物调节暴露的影响,以减少混杂因素的影响。
结论
现有证据表明,FMT是一种安全的干预措施,可能改善ASD儿童和青少年的胃肠道和行为症状。尽管观察研究和部分RCT数据表明有益,但最终结论受到研究质量和变异性的限制。强有力的、充分样本量的、安慰剂对照的RCT,具有标准化的方案和全面的结果测量,对于验证FMT的疗效、阐明机制和指导临床实施至关重要。建立关于最佳FMT制备、给药和剂量的共识将是推进这一有前景的基于微生物组的疗法,以改善ASD患者生活的关键。
参考文献
Liber A, Więch M. The Impact of Fecal Microbiota Transplantation on Gastrointestinal and Behavioral Symptoms in Children and Adolescents with Autism Spectrum Disorder: A Systematic Review. Nutrients. 2025 Jul 7;17(13):2250. doi: 10.3390/nu17132250. PMID: 40647353; PMCID: PMC12252074.