亮点
- 多项前瞻性人体研究报道,在冠状动脉血液、体外循环(CPB)暴露的血液和颈动脉粥样硬化中检测到可检测的微塑料和纳米塑料(MNP)。
- MNP的存在与局部和系统性炎症标志物以及观察队列中的主要不良心血管事件(MACE)高风险相关。
- 尽管这些发现具有生物学上的合理性,但由于潜在污染、方法学异质性和残余混杂因素的影响,因果关系仍未得到证实。
研究背景和疾病负担
微塑料(<5毫米)和纳米塑料(<1000纳米)(MNP)是普遍存在的环境污染物,由较大塑料物品通过光化学、机械或生物过程降解产生。全球暴露途径包括摄入、吸入和皮肤接触;研究已在人体生物材料中检测到MNP,包括胎盘、母乳、尿液、血液、肺和肝脏。新兴毒理学文献——细胞培养和动物模型——显示MNP可以引发氧化应激、内皮炎症、细胞凋亡、心率改变、心肌功能障碍和纤维化以及血管功能障碍。心血管疾病(CVD)仍然是全球死亡的主要原因。如果MNP暴露对CVD风险有贡献,其公共卫生影响可能非常显著。然而,直到最近,直接将MNP负担与血管病理和临床事件联系起来的人类数据仍然很少。
三项研究的总结
以下是三项报告MNP检测和临床关联的前瞻性观察性人体研究的总结。
– 研究1:心肌梗死患者的冠状动脉血液(Zhang等,J Hazard Mater 2025)。一项前瞻性观察队列研究,涉及142名因心肌梗死接受冠状动脉造影的患者;通过热裂解-气相色谱-质谱法(Py-GC/MS)分析冠状动脉血液样本中的聚合物类型和浓度。110名患者的临床事件随访平均时间为31.5个月。
– 研究2:儿童体外循环暴露(Wu等,J Hazard Mater 2025)。一项前瞻性观察研究,涉及22名接受先天性心脏病手术并使用体外循环的儿童。通过Py-GC/MS和激光直接红外光谱法(LDIR)分析配对的术前和术后血液样本,并通过扫描电子显微镜进行颗粒可视化。还进行了临床实验室相关性分析(白细胞和中性粒细胞计数)。
– 研究3:颈动脉粥样硬化和心血管事件(Marfella等,N Engl J Med 2024)。一项多中心前瞻性观察研究,涉及304名因无症状颈动脉狭窄接受颈动脉内膜切除术的患者。通过Py-GC/MS、稳定同位素分析和电子显微镜分析切除的斑块;通过ELISA和免疫组化评估炎症生物标志物。主要终点:随访期间(平均约34个月)的心肌梗死、中风或死亡的复合终点。
Electron Microscopy Analysis of Atheromatous Plaque.
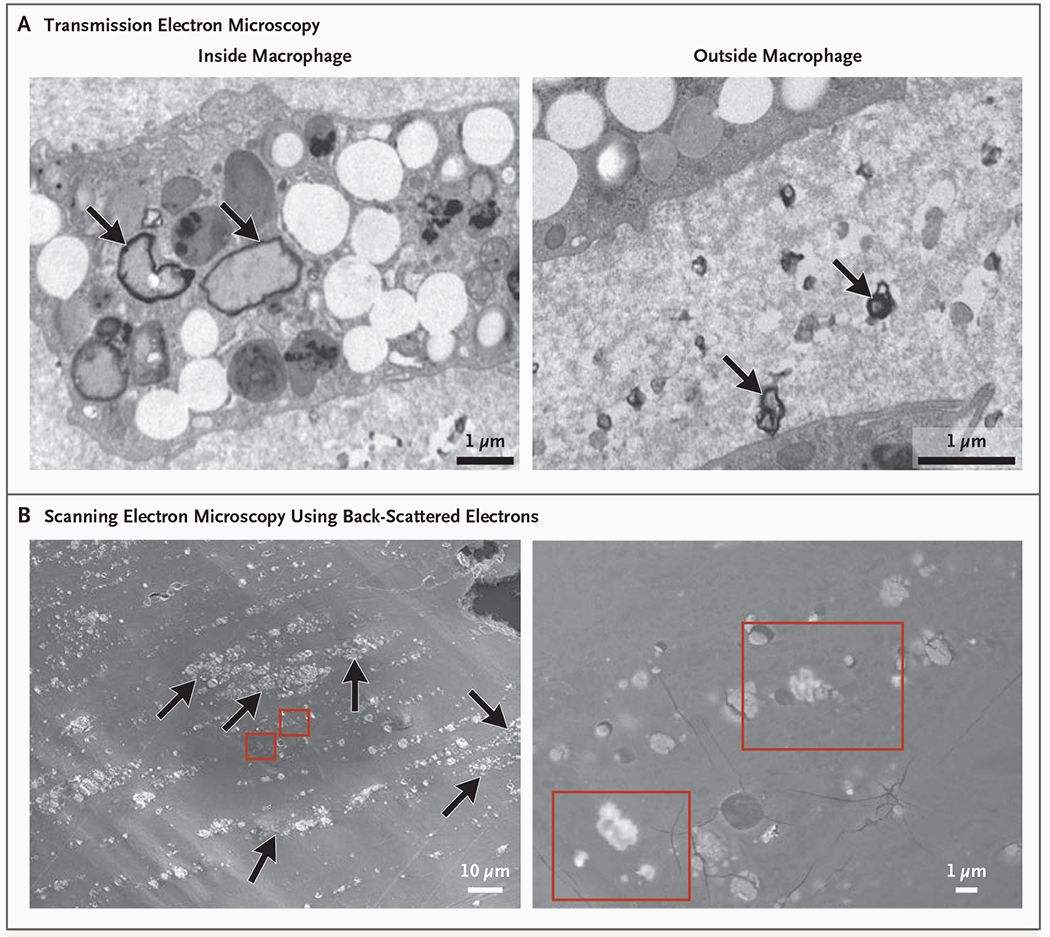
Inflammatory Markers in Plaque Samples.
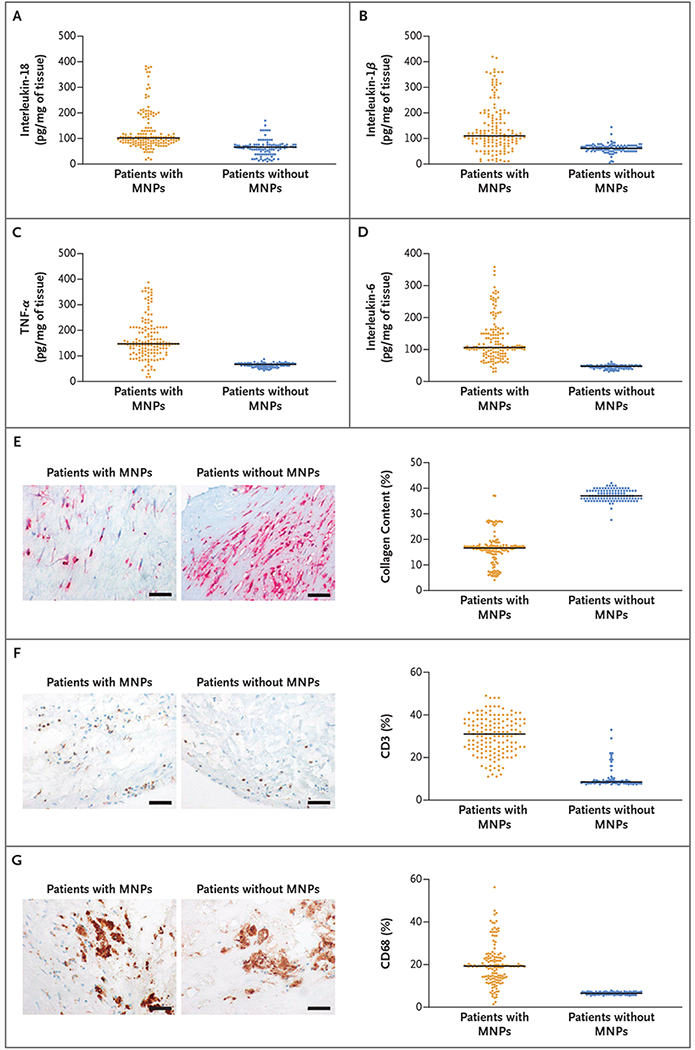
常用的实验室方法包括Py-GC/MS用于聚合物鉴定/定量,以及显微镜/光谱法用于颗粒可视化和元素分析。这些方法提供了互补的化学和形态学信息,但各有优缺点。
关键发现
本节总结了每项研究的主要结果,并对比其意义。
– 冠状动脉血液中的MI(Zhang等):在完成随访的110名患者中,冠状动脉血液中聚合物检测较为常见:聚苯乙烯占43.6%,聚乙烯占71.8%,聚氯乙烯(PVC)占95.4%,聚酰胺66占61.8%。在经历主要不良心脏事件(MACE)的患者中观察到更高的冠状动脉PVC浓度。PVC水平与促炎细胞因子(IL-1β、IL-6、IL-18和TNF-α)相关。回归分析报告,PVC与MACE相关的调整后比值比为1.090(95% CI 1.032–1.1523,P = 0.002),每单位(研究单位未完全标准化);值得注意的是,作者指出,PVC每增加10个单位,MACE的风险增加2.374倍(OR 2.374;95% CI 1.366–4.128;P = 0.002)。对21名MI患者的血液和血栓样本进行额外分析,发现冠状动脉血栓中的PVC水平与炎症标志物和单核细胞/巨噬细胞浸润相关。
– 儿童体外循环(Wu等):体外循环后的血液中总MNP浓度显著升高(p < 0.0001)。特定聚合物的增加在统计上显著,包括聚苯乙烯(p = 0.046)、聚乙烯(p = 0.038)、聚丙烯(p < 0.0001)、PVC(p < 0.0001)和聚酰胺6(p = 0.027)。体外循环时间与MNP暴露相关(r = 0.43,P = 0.047)。MNP暴露的增加与白细胞计数(r = 0.52,P = 0.013)和中性粒细胞(r = 0.46,P = 0.029)的增加相关。LDIR确认体外循环后颗粒计数较高(p = 0.015)。作者得出结论,体外循环回路——主要由塑料构成——可能是急性血液MNP暴露的直接来源。
– 颈动脉粥样硬化和心血管事件(Marfella等):在257个可评估的斑块中,150个(58.4%)检测到聚乙烯,平均水平为每毫克斑块21.7 ± 24.5 μg;31名患者(12.1%)检测到PVC,平均为5.2 ± 2.4 μg/mg。电子显微镜显示嵌入斑块巨噬细胞之间的锯齿状颗粒;放射性元素分析表明某些颗粒中含有氯(与PVC一致)。斑块中含有MNP的患者发生复合主要终点的发病率较高(危险比4.53;95% CI 2.00–10.27;P < 0.001),与斑块中未检测到MNP的患者相比。
Electron Microscopy Analysis of Atheromatous Plaque.

Inflammatory Markers in Plaque Samples.

比较解释:在所有研究中,MNP经常被检测到,并且与炎症标志物和不良临床结局(在颈动脉斑块和MI队列中)相关。体外循环研究展示了急性血管内MNP暴露的合理医源性途径以及短期内可观察到的炎症反应。
专家评论和批判性评价
生物学合理性:MNP与血管炎症的关联与体外和动物数据一致,这些数据显示颗粒诱导的氧化应激、内皮激活、细胞因子释放和免疫细胞募集。MNP还可能携带吸附的化学添加剂(增塑剂、阻燃剂)或微生物成分,从而放大炎症反应。
方法学优势:所有三项研究都是前瞻性的,并采用现代分析技术(Py-GC/MS、LDIR、电子显微镜),提供化学特异性和在某些情况下可视化的颗粒定位。颈动脉研究的多中心设计和临床终点增强了对有症状事件的外部有效性。
关键局限性和替代解释:
- 污染和分析标准化:塑料无处不在;严格的空白对照和程序控制至关重要。已发表的研究在污染控制报告和聚合物浓度单位的呈现方式上存在差异,这使得研究间比较变得复杂。
- 测量和颗粒表征:Py-GC/MS提供聚合物质量和化学特征,但不提供颗粒大小或形态;显微镜可以可视化颗粒,但在定量吞吐量和化学特异性方面有限。结合技术是一个进步,但标准协议尚未普遍采用。
- 观察性设计和混杂因素:关联并不证明因果关系。在颈动脉研究中,斑块中含有MNP的患者可能在未测量的方面(地理位置、职业暴露、饮食、社会经济因素)有所不同,这些因素会影响心血管风险。尽管进行了调整,但仍可能存在由已知CVD风险因素引起的残余混杂。
- 一些分析的小样本量:体外循环儿科队列(n=22)和血栓亚组(n=21)样本量较小;结果应被视为探索性的。
- 单位解释和剂量-反应:MI研究报告了PVC与MACE之间有趣的剂量关联,但解释需要明确测量单位和潜在的非线性。
临床意义:证据具有挑衅性,将理论风险推向了与炎症和观察队列中不良结局相关的人类暴露的可测量水平。然而,它尚未证明因果关系或建立用于临床决策的暴露阈值。当前数据支持两个实际考虑:(1)塑料医疗设备(例如,体外循环回路)可能导致急性医源性暴露的可能性,(2)研究和监管关注设备生物相容性和颗粒脱落的必要性。
结论和临床启示
近期的人类研究表明,MNP存在于冠状动脉血液、体外循环暴露的血液和颈动脉斑块中,并与炎症和更差的心血管结局相关。这些数据为预临床毒理学提供了合理的验证,并提示MNP可能作为CVD中被忽视的环境或医源性风险因素。然而,重要注意事项包括潜在污染、分析方法的异质性、残余混杂和证据的观察性质。临床医生应了解这些新出现的数据,支持进一步高质量的研究,并与设备制造商和监管机构合作,减少侵入性手术中的塑料颗粒脱落。
研究议程和政策优先事项
- 标准化采样、空白对照和分析流程(协调的Py-GC/MS、微FTIR、LDIR和电子显微镜),以实现可比性和剂量-反应评估。
- 大型前瞻性人群队列,基线评估MNP暴露并确定心血管结局,以评估时间顺序和混杂因素。
- 机制性人体研究(离体血管组织暴露、受控输注模型(伦理允许时))和转化工作,将颗粒属性(大小、形状、化学)与免疫和内皮反应联系起来。
- 重点评估医疗器械脱落(体外循环回路、导管、透析)并提出工程解决方案(材料、涂层、过滤器)和监管指导,以减少医源性暴露。
- 针对高暴露环境和易感人群的公共卫生监测和暴露缓解策略。
精选参考文献
- Marfella R, Prattichizzo F, Sardu C, et al. Microplastics and Nanoplastics in Atheromas and Cardiovascular Events. N Engl J Med. 2024;390(10):900-910. doi:10.1056/NEJMoa2309822 IF: 78.5 Q1 . 下载:PDF (808.8 KB)
- Zhang Y, Gao Q, Gao Q, et al. Microplastics and nanoplastics increase major adverse cardiac events in patients with myocardial infarction. J Hazard Mater. 2025 Jun 5;489:137624. doi:10.1016/j.jhazmat.2025.137624 IF: 11.3 Q1 .
- Wu Y, Chen Y, He R, Zhao T, Chen Z. Micronanoplastic exposure due to cardiopulmonary bypass in children: A prospective observational study. J Hazard Mater. 2025 Jun 5;489:137732. doi:10.1016/j.jhazmat.2025.137732 IF: 11.3 Q1 .
- Ragusa A, Svelato A, Santacroce C, et al. Plasticenta: First evidence of microplastics in human placenta. Environ Int. 2021;146:106274. doi:10.1016/j.envint.2020.106274 IF: 9.7 Q1 .

