ハイライト
- ルソリチニブは、コルチコステロイド抵抗性または依存性慢性移植片対宿主病(SR/D-cGVHD)の患者において、最良の可用治療法(BAT)と比較して、有意に長い無失敗生存(FFS)と反応持続期間(DOR)を提供します。
- 3年間を通じて、ルソリチニブは良好なベネフィット・リスクプロファイルを維持し、持続的な反応とBATよりも低い重度の有害事象の発生率を示しました。
- ステロイド節約効果が明らかで、ルソリチニブ群ではBAT群よりも多くの患者がステロイドの使用を中止することができました。
研究背景と疾患負担
慢性移植片対宿主病(cGVHD)は、同種異体造血幹細胞移植(HSCT)後の主要な合併症であり、最大50%の受容者に影響を与え、長期的な機能障害と死亡率に大きく影響します。コルチコステロイドは第一選択療法の中心ですが、50-60%の患者が抵抗性または依存性となり、効果的な第二選択療法が必要となります。最近まで、エビデンスに基づく代替治療法は限られており、長期的なステロイド使用は大きな毒性と生活の質の低下に関連しています。SR/D-cGVHDに対する持続的、安全、そしてステロイド節約効果のある治療法の未満足な需要により、ルソリチニブのような選択的JAK1/2阻害剤の評価が促されました。
研究デザイン
REACH3(NCT03112603)は、12歳以上の中等度から重度のSR/D-cGVHD患者を対象とした世界的、無作為化、多施設、オープンラベルの第III相試験です。参加者(N=329)は1:1の割合で、ルソリチニブ(1日2回10 mg)または医師選択の最良の可用治療法(BAT)のいずれかに無作為に割り付けられました。BATには、地域の標準に従うさまざまな免疫抑制剤が含まれます。主要な有効性期間は24週間で、その後、患者は割り付けられた治療を続けることができ、BAT群の患者は24週間以降にルソリチニブへの切り替えが可能でした。長期フォローアップは156週間(3年間)続き、有効性、安全性、コルチコステロイド使用、および生存結果が評価されました。
重要な評価項目には以下の通りです。
– 無失敗生存(FFS):再発、非再発死亡(NRM)、または新たな全身療法の必要性までの時間
– 反応持続期間(DOR)
– 全体生存(OS)
– 有害事象(AEs)、特にグレード≥3および重大な事象に焦点を当て
– コルチコステロイドの用量減少と中止率
主要な知見
有効性アウトカム
ルソリチニブはBATに対して明確かつ持続的な臨床的利点を示しました。
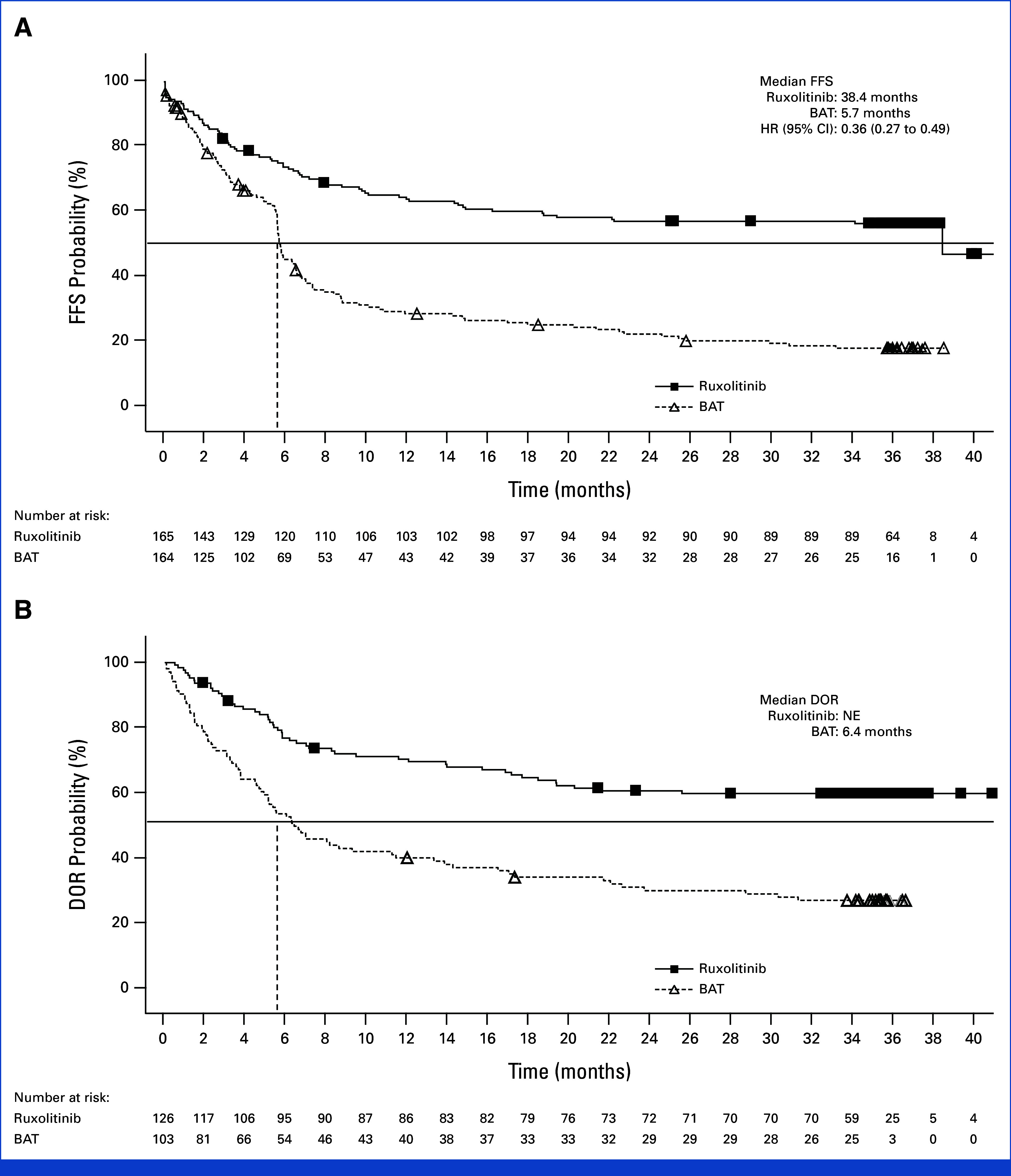
– ルソリチニブ群の中央値FFSは38.4ヶ月で、BAT群は5.7ヶ月(ハザード比[HR]0.36、95%信頼区間0.27~0.49)であり、失敗イベントのリスクが64%低下したことを示しています。36ヶ月時点で、ルソリチニブ群の56.5%の患者が失敗フリーであったのに対し、BAT群は18.2%でした。
– DORはルソリチニブ群ではデータカットオフ時点でも達成されていません(つまり、ほとんどの反応者は寛解状態を維持していました)。一方、BAT群では6.4ヶ月(95%信頼区間4.9~11.4)でした。36ヶ月時点で、ルソリチニブ群の59.6%の患者が反応を維持していたのに対し、BAT群は26.7%でした。
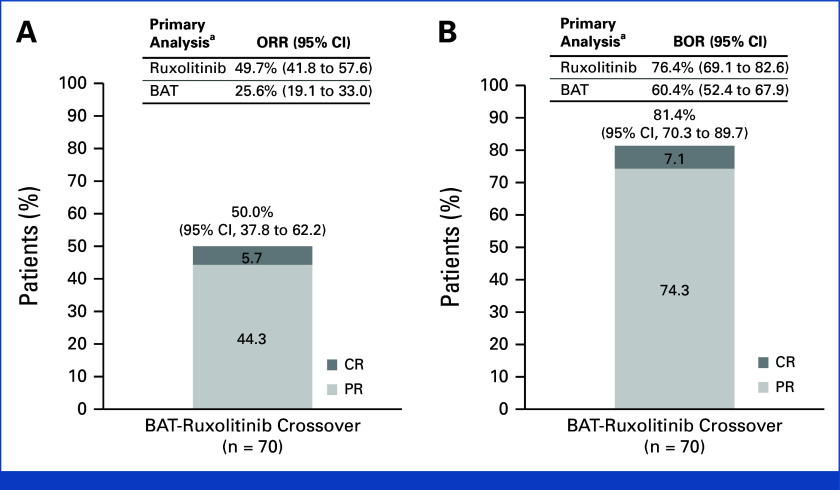
– 24週間後にルソリチニブを中止した患者のうち、21人のうち3人(14%)のみがcGVHDの再発を経験し、持続的な寛解の可能性を示唆しています。
– 中央値全体生存(OS)はどちらの群でも達成されておらず、死亡率は同等でした(HR 0.85、95%信頼区間0.54~1.33)。36ヶ月時点で非再発死亡と悪性腫瘍の再発/再発率は低く、両群で類似していました。
– コルチコステロイドの用量減少はルソリチニブ群で大きかったです:55.3%の患者が完全にステロイドを中止したのに対し、BAT群は36.4%でした。
– 肺や肝臓cGVHDなどの高リスクカテゴリーを含む器官関与によるサブグループで、ルソリチニブの持続的な利点が一貫していました。
安全性プロファイル
– 暴露量を調整した重大およびグレード≥3の有害事象は、ルソリチニブ群でBAT群よりも頻度が低かったです(グレード≥3のAEs:100患者治療年あたり94.1対120.9、重大なAEs:100患者治療年あたり43.3対63.9)。
– ルソリチニブで最も一般的な有害事象は貧血で、次いでクレアチニン上昇でした。これらは用量調整や補助ケアによって管理可能です。肺炎は中止の主な原因でしたが、発生率はBATと同等でした。
– 感染関連の合併症や二次性悪性腫瘍の増加は、ルソリチニブ群でBAT群と比較して有意ではありませんでした。
専門家のコメント
REACH3の3年間最終分析は、ステロイド失敗後のSR/D-cGVHDにおけるルソリチニブの標準治療としての強力な証拠を提供しています。FFSとDORの延長、管理可能な安全性プロファイル、そしてコルチコステロイドの使用量を減らしたり中止したりする能力は、歴史的な第二選択療法の制限を直接解決しています。これらの結果は、欧州血液・骨髄移植学会のガイドライン認定と米国および欧州での規制当局の承認と一致しています。
REACH3の注目すべき強みは、cGVHDの慢性化と変動性を捉える長期フォローアップと、現実世界の治療強化を反映するクロスオーバーの許可です。オープンラベルデザインとBATの異質性は制限要因ですが、ルソリチニブの利点の大きさと持続性は堅固です。今後の研究は、シーケンスの最適化、治療期間、組み合わせ戦略、および遅発性有害事象の長期モニタリングに焦点を当てるべきです。
結論
ルソリチニブは、コルチコステロイド抵抗性または依存性cGVHDの第二選択療法における新しい基準を設定し、持続的な疾患制御、ステロイド節約効果、および良好な長期安全性プロファイルを提供します。これらの知見は、その臨床実践への統合を支持し、慢性GVHDの個別化された患者中心の管理に関する継続的な研究の必要性を強調しています。
参考文献
1. Zeiser R, Russo D, Ram R, Hashmi SK, Chakraverty R, Middeke JM, Musso M, Giebel S, Uzay A, Langmuir P, Hamad N, Burock K, Gowda M, Stefanelli T, Lee SJ, Teshima T, Locatelli F. Ruxolitinib in Patients With Corticosteroid-Refractory or Corticosteroid-Dependent Chronic Graft-Versus-Host Disease: 3-Year Final Analysis of the Phase III REACH3 Study. J Clin Oncol. 2025 Aug 10;43(23):2566-2571. doi: 10.1200/JCO-24-02477 IF: 41.9 Q1 . Epub 2025 Jun 25. PMID: 40561385 IF: 41.9 Q1 ; PMCID: PMC12316163 IF: 41.9 Q1 .2. Jagasia MH, et al. Blood. 2015;125(8):1298-1307.3. European Society for Blood and Marrow Transplantation. Guidelines on cGVHD. 2021.4. U.S. FDA Ruxolitinib Approval Press Release. 2021.