ハイライト
- 早期妊娠中の低濃度カドミウム(Cd)曝露は、妊娠糖尿病(GDM)の発症リスクが2倍以上になることが示されています。
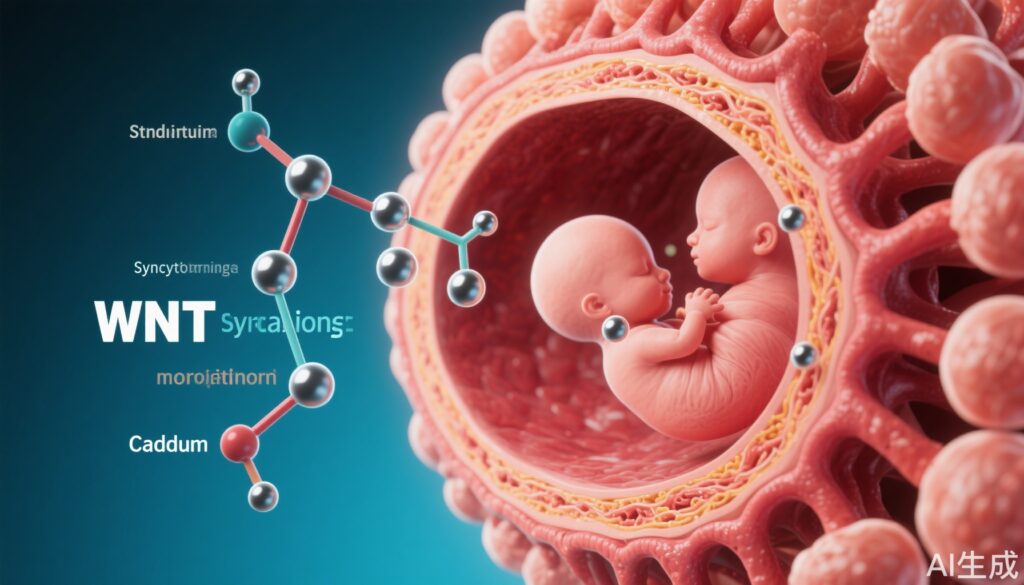
- カドミウムは胎盤シンシチオトロフォブラストの分化を促進し、ミトコンドリア代謝を変化させ、グルコース利用を偏らせ、インスリン抵抗性ホルモンの産生を強化します。
- メカニズムの洞察から、環境中のCdは胎盤の代謝再プログラムを通じてGDMのリスクを高める可能性があることがわかりました。これは、単なる母体の直接的な血糖値異常だけでなく、胎盤の影響が主であることを示唆しています。
研究背景と疾患負担
妊娠糖尿病(GDM)は一般的な妊娠合併症で、世界中で最大15%の妊娠に影響を与えています。GDMは、妊娠中に初めて認識されるまたは発症するグルコース耐容性の低下を特徴とし、増加した胎盤インスリン抵抗性ホルモンと十分な補償性インスリン分泌の不一致により引き起こされます。GDMは、子宮内膜症、巨大児、長期的な2型糖尿病など、母体と新生児の両方にとって悪影響を及ぼすリスクを高めます。古典的なリスク要因(肥満、年齢、遺伝子)はよく知られていますが、新規の証拠は環境毒素(重金属を含む)も寄与する可能性を示唆しています。カドミウム(Cd)は、食事、水、タバコを通じて遭遇する普遍的な環境汚染物質であり、内分泌攪乱物質として知られています。しかし、妊娠前の低濃度Cd曝露とGDMリスクとの関連性は不明確であり、その背後の胎盤メカニズムはほとんど未探索でした。
研究デザイン
Chen Hら(2025年)によって報告されたこの調査では、堅牢な出生コホートデザインが採用され、GDMを発症した462人の女性と同一人口からの924人の対照群が登録されました。早期妊娠時に血漿Cd濃度を測定するために血液サンプルが収集されました。生物学的メカニズムを解明するために、研究者は臨床データに加えてin vitro胎盤モデル(ヒューマントロフォブラストオルガノイドと分化したシンシチオトロフォブラスト(STBs))を使用しました。これらのモデルは、コホートで観察された濃度(0.08 μM、95パーセンタイルに対応)に準じたCdへの標的曝露とその後の代謝、シグナル伝達、ホルモン変化の評価を可能にしました。
主要な結果
疫学的関連性:
GDMを発症した女性は、対照群(0.12 μg/l)と比較して、早期妊娠時の平均血漿Cd濃度が有意に高かった(0.37 μg/l)。多変量分析では、Cdレベルの上昇とGDMリスクとの強い線形関連が示され、オッズ比(OR)は2.15(95% CI: 1.84–2.50)でした。年齢、BMI、産回数、社会経済的地位などの主要な混雑因子を調整しても、この関連性は持続し、Cd曝露の独立した貢献が強調されました。
胎盤モデルからのメカニズム洞察:
– WNTシグナル伝達とSTB分化: 低濃度Cd(0.08 μM)に曝露されたSTBでは、WNT経路のシグナル伝達が上昇し、脂肪酸β酸化に関与するACSM1遺伝子の発現が増加しました。WNTシグナル伝達の強化は、STBの分化と胎盤の発達に重要であり、Cdがこれらのプロセスを加速または異常制御する可能性を示唆しています。
– ミトコンドリア代謝: Cd処理は、グルコースが主な基質として同定されたSTBでのミトコンドリア呼吸を強化しました。興味深いことに、上昇したβ酸化はエネルギー産生のための三羧酸(TCA)サイクルの活動には転換せず、代わりに代謝中間体がステロイドホルモン合成を支援するために流用されているように見えました。
– ホルモン産生: 特に、Cdに曝露されたSTBは、インスリン抵抗性ホルモン(例えば、胎盤ラクトゲン、プロゲステロン)の産生量が高かったです。このホルモンの変化は、母体のインスリン抵抗性を増幅し、高血糖(GDMの特徴)を引き起こす微妙なバランスを崩す可能性があります。
統合的解釈:
研究結果は、妊娠前の低濃度Cd曝露が胎盤の代謝と内分泌機能を大幅に再プログラムできる可能性があることを示唆しています。膵臓や肝臓への直接的な影響ではなく、主要な損傷は母体-胎児インターフェースである胎盤で起こるようです。ここで、Cd誘発のSTB分化、ミトコンドリア代謝、ホルモン出力の変化が共同してGDMを促進する代謝環境を形成することが示されています。
専門家のコメント
これらの結果は、環境中のCd曝露とGDMリスクの関連性を結びつける強力な臨床的およびメカニズム的証拠を提供し、毒素が妊娠結果にどのように影響するかという理解の重要なギャップを埋めています。ヒューマントロフォブラストモデルの使用は生理学的関連性と翻訳的価値を追加し、単なる相関疫学から因果推論へと進展させます。ただし、いくつかの制限点について議論する必要があります。まず、コホートは詳細に特徴付けられ、混雑因子が調整されていましたが、未測定の変数(例えば、食事、共存曝露)による残存バイアスは排除できません。次に、in vitroモデルは情報提供が役立つものの、in vivo胎盤-母体相互作用の複雑さを完全に再現することはできません。それでも、この研究は環境リスクの中心的な仲介者としての胎盤の重要性を強調しており、他の毒素や妊娠合併症にも適用できる可能性のあるパラダイムを示しています。
公衆衛生の観点から、これらの結果は、特に生殖年齢の人口に対する環境中のCdの規制強化の必要性を強調しています。環境曝露のスクリーニングは、妊娠前および妊娠中のケアの重要な要素となる可能性があります。
結論
早期妊娠中の低濃度カドミウム曝露は、胎盤の代謝とホルモンの再プログラムを通じて、妊娠糖尿病の独立した強力なリスク要因です。これらの洞察は、GDMのリスク層別化と予防策に加えて、環境汚染物質が母体-胎児の健康にどのように影響するかのメカニズム的理解を進展させます。今後の研究は、介入研究、長期的な子供の結果、他の環境毒素との相加的または相乗効果の調査に焦点を当てるべきです。
参考文献
1. Chen H, Bin J, Cao Z, Luo Y, Song P, He J, Lu S, Mahai G, Zheng J, Li Y, Qin J. Role of low-dose cadmium exposure to the pathogenesis of gestational diabetes mellitus. Environ Pollut. 2025 Oct 1;382:126718. doi: 10.1016/j.envpol.2025.126718. Epub 2025 Jun 24. PMID: 40571113.
2. American Diabetes Association. Management of Diabetes in Pregnancy: Standards of Medical Care in Diabetes—2024. Diabetes Care. 2024;47(Suppl 1):S237–S248.
3. Kippler M, Tofail F, Gardner R, et al. Maternal cadmium exposure during pregnancy and size at birth: a prospective cohort study. Environ Health Perspect. 2012;120(2):284-289.