Nhấn mạnh
Liệu pháp kép chặn điểm kiểm tra miễn dịch bằng ipilimumab và nivolumab không cải thiện thời gian sống không tiến triển so với hóa trị liệu tiêu chuẩn temozolomide ở bệnh nhân mới chẩn đoán u nguyên bào thần kinh đệm MGMT không methy hóa. Thử nghiệm giai đoạn II không đạt được điểm cuối chính, dẫn đến việc ngừng sớm mà không tiếp tục sang giai đoạn III. Hồ sơ an toàn phù hợp với tác dụng đã biết, và không có tín hiệu bất lợi mới xuất hiện.
Các nghiên cứu tương quan phân tử và theo dõi sống còn tiếp theo có thể cung cấp thông tin cho các chiến lược điều trị trong tương lai đối với nhóm bệnh nhân khó điều trị này.
Nền tảng nghiên cứu và gánh nặng bệnh lý
U nguyên bào thần kinh đệm (GBM) vẫn là ung thư não nguyên phát phổ biến và hung hãn nhất ở người lớn, đặc trưng bởi tiên lượng kém mặc dù điều trị đa mô đun. Tiêu chuẩn điều trị hiện tại bao gồm phẫu thuật cắt bỏ an toàn tối đa theo sau là xạ trị kết hợp với hóa trị liệu temozolomide (TMZ). Tuy nhiên, bệnh nhân có u nguyên bào thần kinh đệm với trạng thái methy hóa O6-methylguanine-DNA methyltransferase (MGMT) không methy hóa (‘uMGMT’) ít hưởng lợi từ TMZ do kháng thuốc bẩm sinh. Nhóm này đối mặt với thời gian sống không tiến triển (PFS) và sống còn tổng thể (OS) ngắn hơn đáng kể, làm nổi bật nhu cầu cấp bách về các liệu pháp mới.
Các chất ức chế điểm kiểm tra miễn dịch nhắm vào CTLA-4 (ipilimumab) và PD-1 (nivolumab) đã thay đổi các mô hình điều trị trong nhiều loại ung thư nhưng chưa chứng minh được lợi ích rõ ràng trong u nguyên bào thần kinh đệm. Các nghiên cứu giai đoạn I trước đó, bao gồm thử nghiệm NRG Oncology BN002, đã xác lập tính an toàn và gợi ý tín hiệu hiệu quả tiềm năng của việc kết hợp ipilimumab và nivolumab ở bệnh nhân mới chẩn đoán GBM. Điều này thúc đẩy thiết kế của thử nghiệm ngẫu nhiên NRG Oncology BN007 giai đoạn II/III nhằm vào nhóm bệnh nhân uMGMT, kiểm tra liệu liệu pháp kép chặn điểm kiểm tra miễn dịch có cải thiện kết quả so với TMZ tiêu chuẩn hay không.
Thiết kế nghiên cứu
NRG Oncology BN007 là một thử nghiệm lâm sàng ngẫu nhiên, có đối chứng, mở nhãn giai đoạn II/III tuyển chọn người lớn mới chẩn đoán, xác nhận tổ chức học MGMT không methy hóa u nguyên bào thần kinh đệm. Bệnh nhân đủ điều kiện có trạng thái hoạt động Karnofsky (KPS) ≥ 70 và đã trải qua phẫu thuật cắt bỏ an toàn tối đa.
Người tham gia được ngẫu nhiên hóa 1:1 để nhận xạ trị kết hợp với liệu pháp miễn dịch (ipilimumab cộng nivolumab) hoặc hóa trị liệu tiêu chuẩn temozolomide. Các yếu tố phân tầng bao gồm lớp phân tích đệ quy (RPA) (III, IV, V) và việc sử dụng dự kiến các trường điều trị khối u.
Các đặc điểm chính của phác đồ bao gồm cấm sử dụng corticosteroid khi bắt đầu liệu pháp miễn dịch để giảm thiểu ức chế miễn dịch và xác nhận trung tâm về chẩn đoán, trạng thái dấu ấn sinh học (methy hóa MGMT) và sự kiện PFS. Điểm cuối chính của giai đoạn II là thời gian sống không tiến triển (PFS), với khả năng phát hiện tỷ lệ nguy cơ (HR) ≤ 0.58 ủng hộ liệu pháp miễn dịch ở mức ý nghĩa một phía 0.15. Thành công trong PFS giai đoạn II sẽ kích hoạt tiếp tục sang phân tích OS giai đoạn III.
Kết quả chính
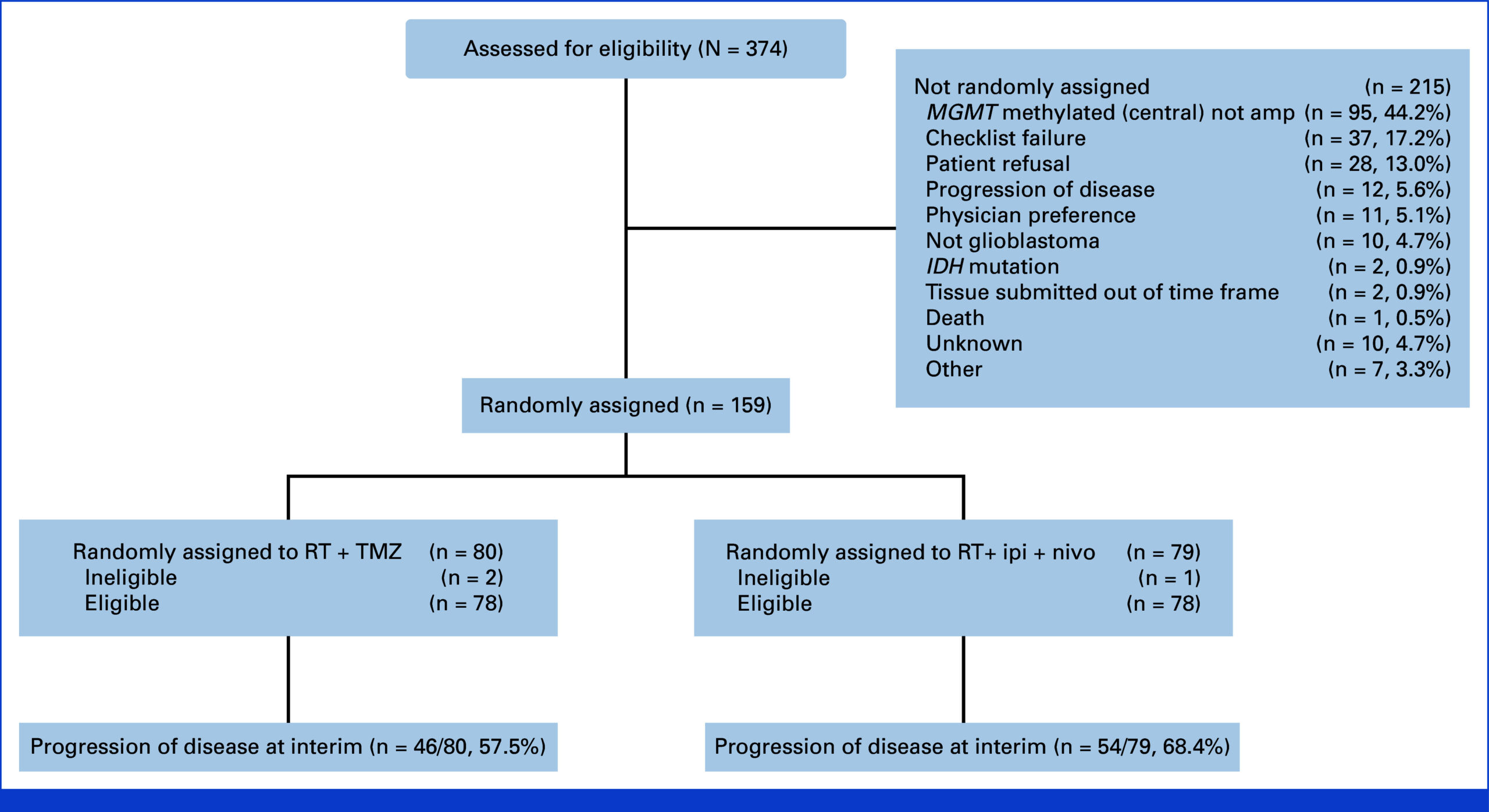
Từ việc hoàn thành tuyển chọn đến phân tích giữa kỳ theo kế hoạch, 159 bệnh nhân đã được ngẫu nhiên hóa: 79 vào nhóm liệu pháp miễn dịch và 80 vào nhóm TMZ. Đặc điểm nhân khẩu học và lâm sàng ban đầu được cân đối tốt, với độ tuổi trung bình 60 tuổi, 66% nam giới, đa số (61%) có KPS 90-100, và 65% đạt cắt bỏ toàn bộ. Phân phối các lớp RPA chủ yếu là lớp IV (73%).
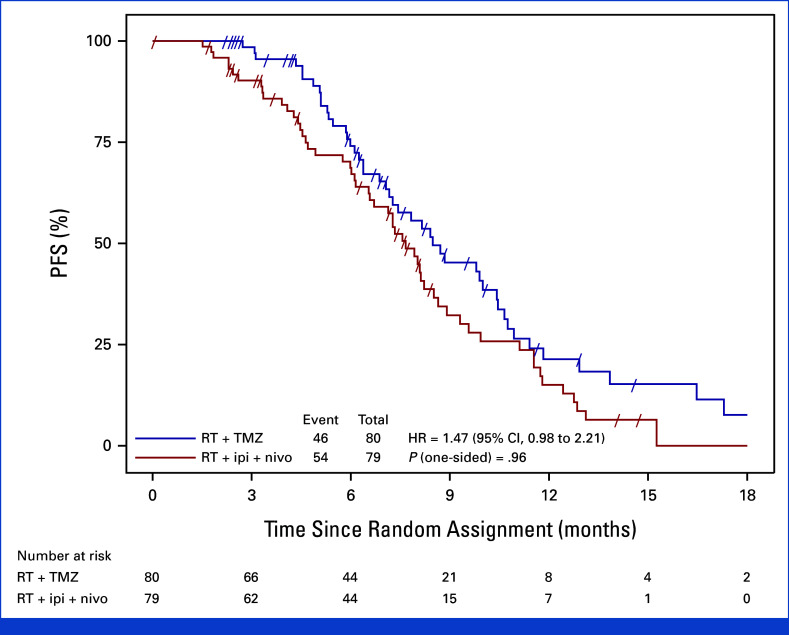
Sau 100 sự kiện tiến triển được xác định trung tâm, phân tích giữa kỳ cho thấy không có cải thiện PFS với liệu pháp miễn dịch so với TMZ. Thời gian PFS trung bình là 7.7 tháng trong nhóm ipilimumab cộng nivolumab so với 8.5 tháng trong nhóm TMZ (tỷ lệ nguy cơ, 1.47; khoảng tin cậy 70%, 1.19 đến 1.83). Giá trị P một phía là 0.96, chỉ ra không có ý nghĩa thống kê ủng hộ nhóm thử nghiệm.
Dữ liệu sống còn tổng thể vẫn chưa chín muồi với hơn 50% người tham gia còn sống tại thời điểm phân tích; thời gian OS trung bình khoảng 13 tháng ở cả hai nhóm (tỷ lệ nguy cơ, 0.95; khoảng tin cậy 95%, 0.61 đến 1.49; P = 0.36), cho thấy không có lợi thế sống còn với liệu pháp kép chặn điểm kiểm tra miễn dịch.
Về an toàn, không có tín hiệu độc tính mới xuất hiện ngoài hồ sơ tác dụng bất lợi đã biết của ipilimumab và nivolumab. Các tác dụng bất lợi liên quan đến miễn dịch có thể quản lý và không khác biệt đáng kể so với các báo cáo trước đây. Đáng chú ý, corticosteroid bị cấm khi bắt đầu liệu pháp miễn dịch để tối ưu hóa đáp ứng miễn dịch.
Bình luận chuyên gia
Thử nghiệm này bổ sung vào cơ sở bằng chứng ngày càng tăng rằng chất ức chế điểm kiểm tra miễn dịch, mặc dù có tác động đáng kể lên nhiều khối u rắn, có thể có hiệu quả hạn chế ở bệnh nhân mới chẩn đoán u nguyên bào thần kinh đệm, đặc biệt là trong nhóm MGMT không methy hóa. Các yếu tố môi trường vi mô, thách thức hàng rào máu-não và sự xâm nhập hạn chế của tế bào T có thể là nguyên nhân gây ra những kết quả thất vọng này.
Sự thất bại trong việc cải thiện PFS hoặc OS với ipilimumab và nivolumab xác nhận các kết quả tương tự từ các nghiên cứu liệu pháp miễn dịch khác trong GBM. Thiết kế vững chắc của thử nghiệm với xác nhận trung tâm về trạng thái phân tử, dân số được phân tầng tốt và quản lý cẩn thận corticosteroid tăng cường sự tin tưởng vào những kết luận này.
Hạn chế bao gồm phân tích giữa kỳ tương đối sớm và dữ liệu OS chưa chín muối, mặc dù tỷ lệ nguy cơ PFS mạnh mẽ chống lại lợi ích của liệu pháp miễn dịch. Nghiên cứu trong tương lai nên khám phá các phương pháp kết hợp nhằm tăng cường xâm nhập miễn dịch hoặc nhắm vào các điểm yếu bổ sung của khối u cùng với ức chế điểm kiểm tra.
Kết luận
Thử nghiệm ngẫu nhiên NRG Oncology BN007 giai đoạn II cho thấy việc kết hợp ipilimumab với nivolumab không cải thiện thời gian sống không tiến triển so với temozolomide ở bệnh nhân mới chẩn đoán u nguyên bào thần kinh đệm MGMT không methy hóa đang điều trị xạ trị. Do đó, thử nghiệm đã bị đóng cửa vĩnh viễn trước khi chuyển sang phân tích OS giai đoạn III.
Những phát hiện này nhấn mạnh thách thức đang diễn ra trong việc phát triển liệu pháp miễn dịch trong u nguyên bào thần kinh đệm và nhu cầu cấp bách về các chiến lược thay thế trong nhóm bệnh nhân này. Các nghiên cứu phân tử và tương quan tiếp theo từ thử nghiệm này có thể cung cấp thông tin cho các cách tiếp cận liệu pháp miễn dịch cá nhân hóa trong tương lai.
Tham khảo
1.Lassman AB, Polley MC, Iwamoto FM, Sloan AE, Wang TJC, Aldape KD, Wefel JS, Gondi V, Gutierrez AN, Manasawala MH, Gilbert MR, Sulman EP, Wolchok JD, Green RM, Neil EC, Lukas RV, Goldlust SA, Snuderl M, Galbraith K, Dignam JJ, Won M, Mehta MP. Dual Immune Check Point Blockade in MGMT-Unmethylated Newly Diagnosed Glioblastoma: NRG Oncology BN007, a Randomized Phase II/III Clinical Trial. J Clin Oncol. 2025 Sep 20;43(27):3032-3040. doi: 10.1200/JCO-25-00618 IF: 41.9 Q1
2. Stupp R, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 2005;352(10):987-96.
3. Reardon DA, et al. Immunotherapy advances for glioblastoma. Neuro Oncol. 2020;22(4):555-565.
4. Clarke JL, et al. The role of immune checkpoint blockade in glioblastoma: mechanisms and clinical outcomes. Nat Rev Clin Oncol. 2021;18(4):234-246.