Nhấn mạnh
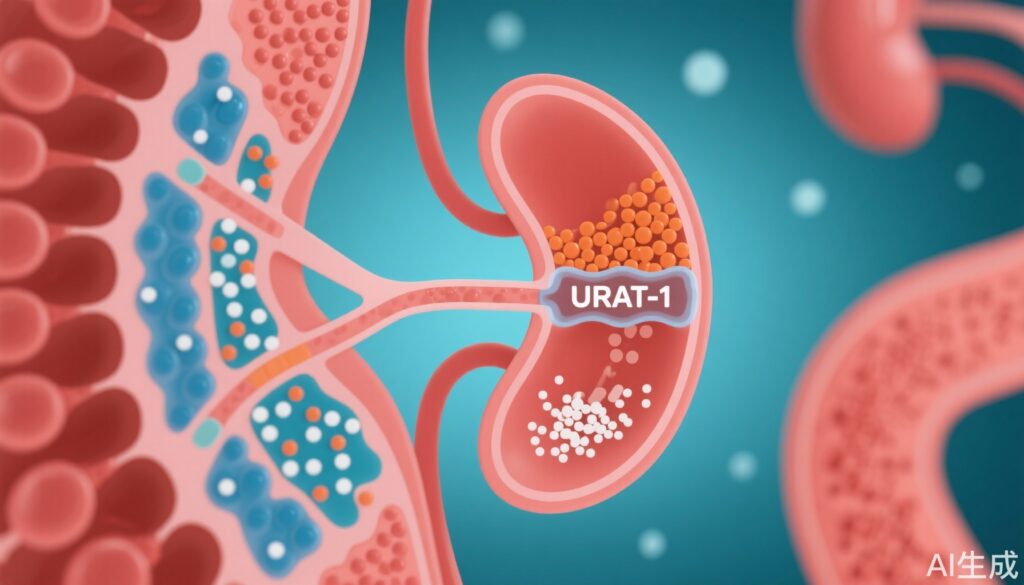
- Hyperinsulinemia có mối tương quan nghịch với phân suất bài tiết uric acid (FEUA), chỉ ra rằng sự tái hấp thu uric acid do URAT1 đóng vai trò quan trọng trong hyperuricemia.
- Sự phosphoryl hóa của URAT1 tại Thr408 bởi các kinase AKT và SGK1, được gây ra bởi hyperinsulinemia và chế độ ăn mặn, lần lượt tăng cường hoạt động của URAT1 và mức uric acid trong huyết thanh.
- Các biến thể di truyền của SLC22A12 (đặc biệt là rs147647315 và rs475688) điều chỉnh ảnh hưởng của hyperinsulinemia đối với uric acid trong huyết thanh, làm nổi bật tương tác giữa gen và môi trường.
- Những phát hiện này hỗ trợ tiếp cận cá nhân hóa trong điều trị hyperuricemia, xem xét trạng thái chuyển hóa và nền tảng di truyền.
Nền tảng Nghiên cứu và Gánh nặng Bệnh tật
Hyperuricemia, đặc trưng bởi mức uric acid trong huyết thanh cao, có tính di truyền mạnh mẽ và là yếu tố nguy cơ trung tâm cho bệnh gout, một dạng viêm khớp đau đớn và phổ biến. Nó thường đi kèm với đề kháng insulin và hyperinsulinemia, các đặc điểm của hội chứng chuyển hóa, nhưng cơ chế phân tử chính xác liên kết hyperinsulinemia với sự thay đổi chuyển hóa uric acid vẫn chưa rõ ràng. Hiểu rõ cách các yếu tố di truyền và ảnh hưởng từ môi trường như chế độ ăn mặn điều chỉnh sự cân bằng uric acid là điều quan trọng để phát triển các chiến lược điều trị hiệu quả và cá nhân hóa cho hyperuricemia và các biến chứng liên quan.
Thiết kế Nghiên cứu
Nghiên cứu này áp dụng phương pháp đa tầng. Lâm sàng, trong số 162 người tham gia ngoại trú, các nhà nghiên cứu đã đánh giá mối liên hệ giữa chỉ số hyperinsulinemia (chỉ ra mức insulin và đề kháng) và phân suất bài tiết uric acid (FEUA), một thước đo về khả năng thanh thải uric acid của thận. Để giải mã các cơ chế phân tử, các phân tích transcriptome đơn tế bào và các thử nghiệm hoạt động kinase đã được tiến hành, bổ sung bằng các thí nghiệm nuôi cấy tế bào đánh giá việc điều chỉnh URAT1.
Hơn nữa, một phân tích dịch tễ học quy mô lớn đã được thực hiện trên 377.358 người tham gia từ UK Biobank (UKBB). Nghiên cứu đã xem xét uric acid trong huyết thanh, các dấu hiệu của hyperinsulinemia (chỉ số TyG) và chế độ ăn mặn tự báo cáo. Các biến thể nucleotide đơn (SNVs) trong SLC22A12, mã hóa vận chuyển uric acid URAT1, đã được đánh giá về tương tác giữa gen và môi trường ảnh hưởng đến mức uric acid trong huyết thanh.
Kết quả Chính
Lâm sàng, chỉ số hyperinsulinemia có mối liên hệ nghịch đáng kể với FEUA, độc lập với các yếu tố nhiễu, chỉ ra rằng sự thanh thải uric acid của thận giảm khi mức insulin tăng.
Các hiểu biết về cơ chế cho thấy rằng sự hiện diện của URAT1 trên bề mặt tế bào và hoạt động vận chuyển uric acid của nó được điều chỉnh bởi sự phosphoryl hóa tại threonine 408, được xúc tác bởi các kinase serin/threonine AKT (được kích hoạt bởi hyperinsulinemia) và SGK1 (được gây ra bởi chế độ ăn mặn). Residue Arg405 là quan trọng đối với sự phosphoryl hóa do kinase, nhấn mạnh mục tiêu phân tử cụ thể. Sự phosphoryl hóa này tăng cường chức năng của URAT1, thúc đẩy sự tái hấp thu uric acid.
Phân tích dịch tễ học ở UKBB xác nhận các mối liên hệ độc lập giữa hyperinsulinemia và chế độ ăn mặn với mức uric acid trong huyết thanh cao hơn. Cả hai yếu tố môi trường đều kích hoạt các con đường hội tụ, tăng cường sự giữ lại uric acid do URAT1.
Phân tích di truyền xác định rằng những người mang biến thể SLC22A12 rs147647315 có mức uric acid trong huyết thanh thấp đáng kể, với hiệu ứng mạnh hơn so với SNP phổ biến rs475688. Quan trọng hơn, phân tích tương tác cho thấy xu hướng có ý nghĩa đối với tương tác gen-môi trường âm giữa chỉ số TyG và rs147647315 (β = -7.50, P=0.096), cho thấy biến thể này làm giảm sự tăng mức uric acid trong huyết thanh do hyperinsulinemia. Ngược lại, rs475688 hoạt động như một locus định lượng biểu hiện (eQTL) tăng cường sự liên kết dương giữa uric acid trong huyết thanh và hyperinsulinemia.
Nghiên cứu cũng nhấn mạnh tầm quan trọng của các vận chuyển uric acid khác, như GLUT9 được mã hóa bởi SLC2A9, các đột biến của nó gây ra hypouricemia thận loại 2, củng cố bức tranh di truyền phức tạp của chuyển hóa uric acid.
Bình luận Chuyên gia
Nghiên cứu toàn diện này làm sáng tỏ một nút giao giữa sinh hóa và di truyền nơi hyperinsulinemia và muối ăn cùng nhau điều chỉnh URAT1 thông qua sự phosphoryl hóa, điều chỉnh sự xử lý uric acid của thận. Việc xác định các vị trí phosphoryl hóa chính và các kinase liên quan (AKT và SGK1) cung cấp các mục tiêu phân tử có thể hành động.
Hơn nữa, việc tích hợp dữ liệu di truyền cho thấy rằng các biến thể phổ biến và hiếm gặp trong SLC22A12 có thể điều chỉnh sự nhạy cảm cá nhân đối với hyperuricemia trong bối cảnh các yếu tố môi trường và chuyển hóa. Những phát hiện này phù hợp với các mô hình mới nổi lên, theo đó tương tác giữa gen và môi trường ảnh hưởng quan trọng đến các đặc điểm chuyển hóa phức tạp.
Các bác sĩ nên xem xét hồ sơ chuyển hóa, thói quen ăn uống và nền tảng di truyền khi quản lý hyperuricemia, đặc biệt là ở bệnh nhân có đề kháng insulin hoặc hội chứng chuyển hóa. Tuy nhiên, bản chất quan sát của nghiên cứu và các xu hướng liên kết di truyền (một số chỉ vừa đủ ý nghĩa) yêu cầu diễn giải thận trọng, và các nghiên cứu can thiệp trong tương lai là cần thiết.
Kết luận
Nghiên cứu này thuyết phục rằng URAT1, được mã hóa bởi SLC22A12, trung gian mối liên hệ giữa hyperinsulinemia và hyperuricemia thông qua việc điều chỉnh phụ thuộc phosphoryl hóa bị ảnh hưởng bởi cả các yếu tố chuyển hóa và môi trường. Các biến thể di truyền điều chỉnh thêm sự tương tác này, cung cấp cơ sở phân tử cho quản lý hyperuricemia cá nhân hóa.
Những hiểu biết này mở đường cho các chiến lược điều trị nhắm mục tiêu xem xét bản đồ di truyền cụ thể của bệnh nhân, trạng thái insulin và các yếu tố lối sống như chế độ ăn mặn, có thể cải thiện kết quả lâm sàng cho bệnh gout và các rối loạn chuyển hóa liên quan.
Tài liệu tham khảo
Fujii W, Yamazaki O, Hirohama D, et al. Tương tác giữa gen và môi trường điều chỉnh mối liên hệ giữa hyperinsulinemia và mức uric acid trong huyết thanh thông qua SLC22A12. J Clin Invest. 2025 Mar 18;135(10):e186633. doi:10.1172/JCI186633 . PMID: 40100301 ; PMCID: PMC12077893 .