Giới thiệu
Bệnh lymphoma đại B tái phát hoặc lờn thuốc (LBCL) vẫn là thách thức lâm sàng, nơi các liệu pháp truyền thống thường mang lại kết quả dài hạn không như mong đợi. Mặc dù có những tiến bộ, bệnh nhân mắc LBCL lờn thuốc nguyên phát hoặc tái phát sớm trong vòng 12 tháng sau liệu pháp đầu tiên thường đối mặt với tiên lượng kém, làm nổi bật nhu cầu y tế chưa được đáp ứng cho các liệu pháp điều trị thứ hai cải tiến. Các liệu pháp tế bào T với thụ thể kháng nguyên chimeric (CAR) đã xuất hiện như một lựa chọn hứa hẹn, sử dụng tế bào T tự thân được thiết kế để nhắm vào tế bào lymphoma biểu hiện CD19, có thể mang lại sự thuyên giảm bền vững hoặc chữa khỏi.
Thiết Kế Nghiên Cứu
Nghiên cứu TRANSFORM giai đoạn III (NCT03575351) là một thử nghiệm ngẫu nhiên, mở nhãn, toàn cầu so sánh lisocabtagene maraleucel (liso-cel), một sản phẩm tế bào T CAR định hướng CD19, với liệu pháp tiêu chuẩn do bác sĩ chọn (SOC) như liệu pháp thứ hai cho người lớn mắc LBCL lờn thuốc nguyên phát hoặc tái phát sớm (trong vòng 12 tháng) đủ điều kiện để ghép tế bào gốc tự thân (ASCT). Các tiêu chí bao gồm chính yêu cầu bệnh có thể đo lường, và bệnh nhân được ngẫu nhiên 1:1 để nhận liso-cel (liều mục tiêu 100 × 106 tế bào T dương tính CAR) hoặc SOC (hóa miễn dịch dựa trên platium theo sau là hóa trị liều cao và ASCT nếu đáp ứng). Liệu pháp hỗ trợ được phép để kiểm soát bệnh trong quá trình sản xuất liso-cel.
Mục tiêu chính của thử nghiệm là thời gian sống không sự kiện (EFS) được đánh giá bởi ủy ban xem xét độc lập (IRC), với các mục tiêu phụ bao gồm tỷ lệ đáp ứng hoàn toàn (CR), thời gian sống không tiến triển (PFS), thời gian sống tổng thể (OS) và an toàn.
Dân Số Bệnh Nhân
Tổng cộng 184 bệnh nhân được ngẫu nhiên và điều trị (92 bệnh nhân mỗi nhóm). Đặc điểm cơ bản được cân đối tốt, bao gồm các loại LBCL, phân bố độ tuổi (trung bình 59 tuổi), giai đoạn bệnh và tình trạng lờn thuốc trước đó. Khoảng 66% bệnh nhân SOC đủ điều kiện chuyển sang nhận liso-cel khi tiến triển hoặc theo các tiêu chí quy định.
Kết Quả Chính
Tại thời điểm theo dõi trung bình 33,9 tháng, liso-cel đã chứng minh lợi ích lâm sàng vượt trội và bền vững hơn so với SOC:
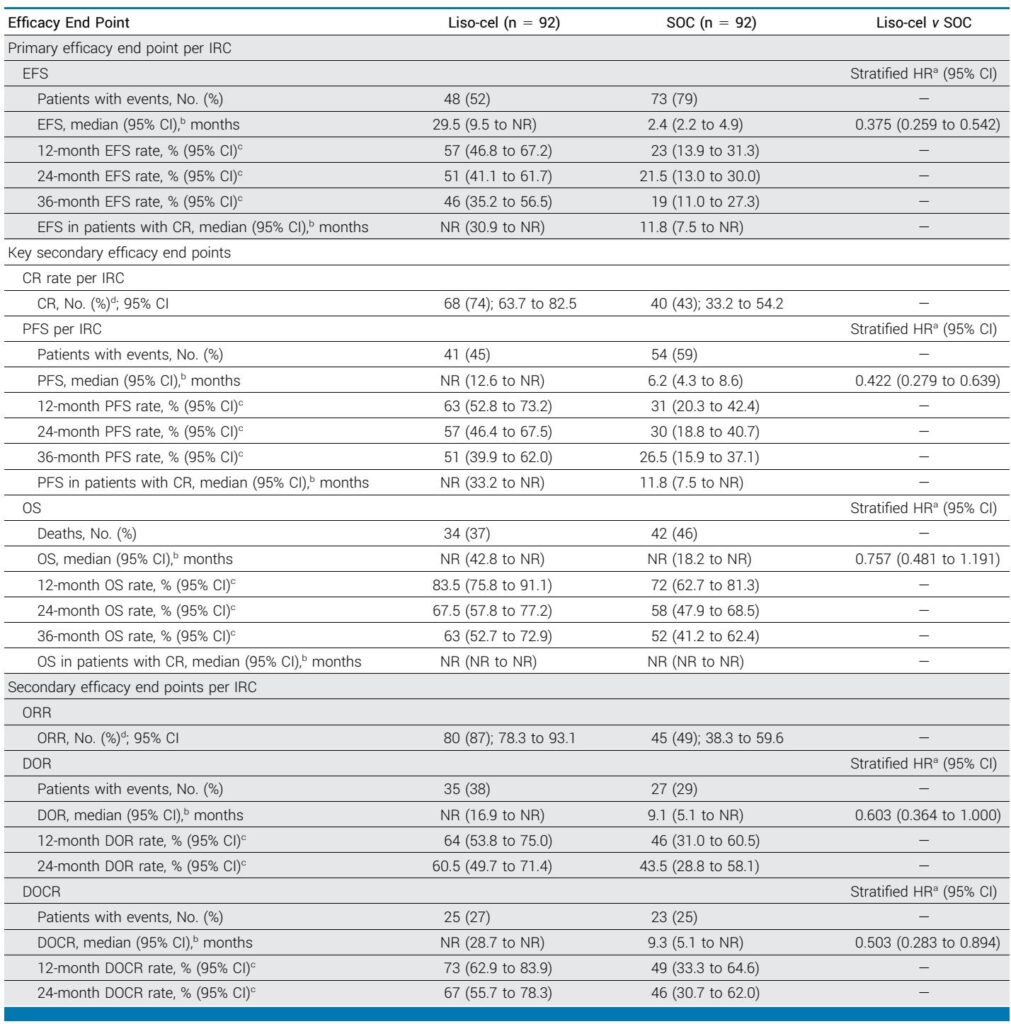
- Thời Gian Sống Không Sự Kiện: Thời gian EFS trung bình là 29,5 tháng (95% CI: 9,5 đến không đạt) cho liso-cel so với 2,4 tháng (95% CI: 2,2 đến 4,9) cho SOC, tương ứng với tỷ lệ nguy cơ (HR) 0,375 (95% CI: 0,259–0,542), chỉ ra việc giảm 62,5% nguy cơ sự kiện hoặc tử vong.
- Thời Gian Sống Không Tiến Trình: Thời gian PFS trung bình không đạt cho liso-cel (95% CI: 12,6 đến NR) so với 6,2 tháng (95% CI: 4,3 đến 8,6) cho SOC (HR 0,422; 95% CI: 0,279–0,639). Tỷ lệ PFS sau 36 tháng ủng hộ liso-cel ở mức 51% so với 26,5%.
- Tỷ Lệ Đáp Ứng: Tỷ lệ CR theo IRC cao hơn đáng kể với liso-cel ở mức 74% (95% CI: 63,7–82,5) so với 43% (95% CI: 33,2–54,2) trong SOC. Thời gian kéo dài CR rõ rệt hơn với liso-cel (trung bình không đạt so với 9,3 tháng trong SOC; HR 0,503).
- Thời Gian Sống Tổng Thể: Thời gian OS trung bình không đạt ở cả hai nhóm; tuy nhiên, tỷ lệ OS sau 36 tháng là 63% cho liso-cel so với 52% cho SOC. Quan trọng là, các phân tích điều chỉnh phù hợp cho 66% bệnh nhân SOC chuyển sang liso-cel cho thấy lợi ích về OS ủng hộ liso-cel với HR 0,566 (95% CI: 0,359–0,895).
Các kết quả nhất quán ủng hộ liso-cel trong các nhóm con khác nhau, bao gồm bệnh nhân lớn tuổi, những người có chỉ số tiên lượng cao hơn và các loại LBCL khác nhau.
Hồ Sơ An Toàn
Liso-cel thể hiện hồ sơ an toàn có thể quản lý theo các báo cáo trước đây. Mặc dù thiếu máu kéo dài (cấp độ ≥3 sau 35 ngày truyền) phổ biến hơn với liso-cel, hầu hết các trường hợp đều giải quyết trong vòng hai tháng. Tỷ lệ nhiễm trùng nặng tương đương giữa các nhóm bất chấp tình trạng thiếu máu nhiều hơn với liso-cel. Không có tín hiệu an toàn mới xuất hiện qua theo dõi kéo dài. Các ung thư nguyên phát thứ cấp thấp và cân bằng giữa các nhóm. Đáng chú ý, một số nhiễm trùng liên quan đến COVID-19 cấp độ ≥3 đã xảy ra trong nhóm liso-cel trong thời gian sau điều trị, bao gồm một trường hợp tử vong.
Bàn Luận
Dữ liệu theo dõi 3 năm từ nghiên cứu TRANSFORM củng cố rằng liso-cel cung cấp sự thuyên giảm vượt trội, sâu hơn và bền vững hơn so với SOC ở bệnh nhân LBCL tái phát/lờn thuốc lần thứ hai có nguy cơ cao. Mức độ cải thiện EFS và PFS, cùng với tỷ lệ CR cao hơn và đáp ứng bền vững, nhấn mạnh tiềm năng của liệu pháp tế bào T CAR để thay đổi mô hình điều trị vượt qua hóa trị cứu chữa và ASCT. Sự khác biệt OS hạn chế ở thời điểm này phản ánh việc chuyển nhóm hiệu quả và nghiên cứu không được thiết kế để đánh giá OS; tuy nhiên, các điều chỉnh thống kê tinh vi xác nhận lợi ích về OS cho liso-cel.
Những phát hiện này phù hợp với các báo cáo trước đây về liệu pháp tế bào T CAR trong bối cảnh này và mở rộng bằng chứng dài hạn hỗ trợ khả năng chữa khỏi của liso-cel. Hồ sơ an toàn phù hợp với các tác dụng phụ đã biết, và các sự cố bất lợi vẫn có thể quản lý tại các trung tâm chuyên môn.
Hạn chế bao gồm tính chất mở nhãn và thiết kế chuyển nhóm ảnh hưởng đến việc diễn giải OS, nhưng những hạn chế này được cân bằng bởi phương pháp ngẫu nhiên mạnh mẽ và đánh giá độc lập. Khả năng áp dụng rộng rãi cho các dân số khác nên xem xét các tiêu chí lựa chọn bệnh nhân và khả năng tiếp cận các trung tâm tế bào T CAR chuyên biệt.
Kết Luận
Lisocabtagene maraleucel cải thiện đáng kể thời gian sống không sự kiện và thời gian sống không tiến triển với các đáp ứng hoàn toàn bền vững so với liệu pháp thứ hai tiêu chuẩn ở bệnh nhân LBCL lờn thuốc nguyên phát hoặc tái phát sớm đủ điều kiện để ghép tế bào gốc tự thân. Hồ sơ an toàn và hiệu quả dài hạn thuận lợi hỗ trợ liso-cel là một lựa chọn điều trị thứ hai biến đổi với khả năng chữa khỏi, xứng đáng được tích hợp vào thực hành lâm sàng và các hướng dẫn trong tương lai.
Tham Khảo
Kamdar M, Solomon SR, Arnason J, et al. Lisocabtagene Maraleucel Versus Standard of Care for Second-Line Relapsed/Refractory Large B-Cell Lymphoma: 3-Year Follow-Up From the Randomized, Phase III TRANSFORM Study. J Clin Oncol. 2025;43(23):2671-2678. doi:10.1200/JCO-25-00399