ハイライト
- アザシチジン、ベネトクラクス、およびレヴーメニブの組み合わせは、新規診断のNPM1変異またはKMT2A重配列AMLを有する高齢者において88.4%の全般的反応率を達成しました。
- 1~2サイクル後には難治性疾患が観察されず、ほとんどの寛解は最初のサイクル内で達成されました。
- 安全性プロファイルは管理可能で、分化症候群やQTc延長は治療中止を必要としませんでした。
- 評価されたすべての反応者は中央検査所による流動細胞術で測定可能残留病変が検出されないことを達成しました。
研究背景と疾患負荷
急性骨髄性白血病(AML)は非常に攻撃的な血液悪性腫瘍であり、高齢者に偏って影響を与えています。アザシチジンとベネトクラクスの組み合わせなどの低強度治療法の導入にもかかわらず、60歳以上の患者、特にNPM1変異(NPM1m)やKMT2A重配列(KMT2Ar)などの不利益な分子特徴を持つ患者の長期予後は依然として満足できるものではありません。これらの遺伝子サブタイプは独自の生物学的脆弱性をもたらしますが、再発率が高く持続的な寛解が得にくいという課題も抱えています。レヴーメニブのような強力な経口メニン阻害剤の出現は、疾患生物学を活用し、これらの高リスク集団の予後を改善する新しい道を開く可能性があります。
研究デザイン
本研究は、第1相、オープンラベル、用量増加および拡大試験(ClinicalTrials.gov: NCT03013998)であり、新規診断のAMLを有し、60歳以上のNPM1mまたはKMT2Arを有する患者におけるアザシチジン、ベネトクラクス、およびレヴーメニブの組み合わせの安全性と効果を評価しました。レヴーメニブは2つの用量レベル(113 mgまたは163 mgを12時間ごとに経口投与)で、CYP3A4阻害作用の強いアゾール抗真菌薬とともに、標準用量のアザシチジンとベネトクラクスとともに投与されました。主な目的は、第2相の推奨用量を決定し、安全性を評価することでした。副次的エンドポイントには、反応率、反応までの時間、寛解の持続期間、測定可能残留病変(MRD)ステータスが含まれました。
主要な知見
2つの用量レベルにわたって合計43人の患者が登録され、治療を受けました。注目に値するのは、レヴーメニブの最大耐容用量(MTD)は定義されなかったことから、この治療法の実現可能性が支持されました。安全性プロファイルは一般的に受け入れ可能でした:
- 分化症候群は8人(19%)で観察され、これはメニン阻害に伴う既知のリスクですが、管理可能であり、恒久的な中止を必要としませんでした。
- QTc延長(フリデリシア補正)は19人(44%)で観察されましたが、これも恒久的なレヴーメニブの中止を必要としませんでした。
効果の結果は、この高リスクの高齢者コホートにおいて特に顕著でした:
- 全般的反応率(ORR)は88.4%(95% CI, 74.9–96.1%)でした。ジェノタイプ別に分類すると、NPM1mでは85.3%、KMT2Arでは100%でした。
- 複合完全寛解(CR + 部分的/不完全な血液学的回復を伴うCR)は81.4%(95% CI, 66.6–91.6%)で、単独のCRは67.4%(95% CI, 51.5–80.9%)でした。
- 1~2サイクルの治療後に難治性疾患を示す患者はいませんでした。
- 最初の反応までの中央値は28日で、84%の反応者が最初のサイクル内で寛解に入りました。これは急速な疾患制御を示唆しています。
- 評価可能な37人の患者全員が高感度中央検査所による流動細胞術でMRD陰性を達成しました。これは持続的な寛解の有望な代替指標です。
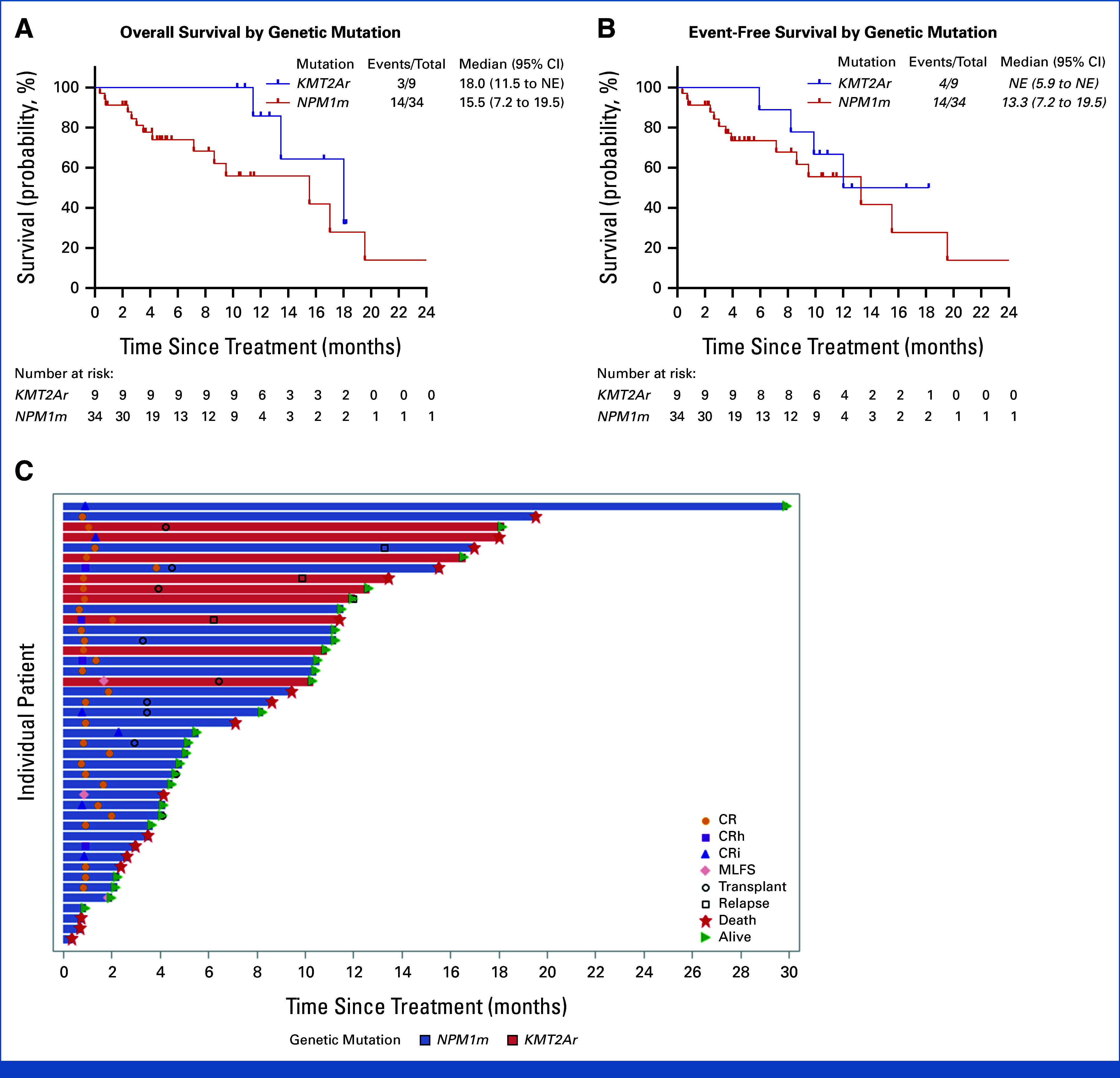
Overall and event-free survival. (A) Median overall survival in KMT2Ar was 18.0 months (95% CI, 11.5 to not reached) and that in NPM1m was 15.5 months (95% CI, 7.2 to 19.5). (B) Median event-free survival in KMT2Ar was not reached and that in NPM1m was 13.3 months (95% CI, 7.2 to 19.5). (C) Swimmer plot describing response, relapse, transplant, and death.
新たな安全信号はありませんでした。組み合わせ療法は蓄積毒性を引き起こさず、用量中断や調整は容易に管理できました。重要なのは、結果が両方の遺伝子サブタイプに一貫していたことで、分子的に定義されたAMLにおけるメニン阻害の広範な効果の可能性が示されました。
専門家のコメント
経口メニン阻害剤であるレヴーメニブを標準的なアザシチジン-ベネトクラクス治療に組み込むことは、従来の治療法で予後が不良だったNPM1mとKMT2Ar AMLの2つのサブグループに対する著しい進歩を示しています。深部寛解の急速な達成、特に評価された患者全員がMRD陰性であったことは、このトリプレット療法が多くの患者の疾患経過を変える可能性があることを示唆しています。第1相データは本来的に初步的であり、サンプルサイズが限られているため、総生存率や遅発毒性に関する確定的な結論を導き出すことはできません。しかし、初期サイクル後の難治性疾患の不在と管理可能な毒性プロファイルは希望的です。
制限点には、小規模なコホートと短い追跡期間があり、全体生存率や遅発毒性に関する確定的な結論を導き出すことはできません。MRD陰性の持続性、移植適格患者の最適な治療シーケンス、そして広範な実践における観察された心臓への影響の最善の管理方法など、未解決の問題が残っています。それでも、これらの結果は進行中の第2/3相試験の情報提供源となり、分子的に特徴付けられたAMLの前線治療の再構築につながる可能性があります。
機構的には、メニン阻害はNPM1変異とKMT2A融合によって駆動される白血病性転写プログラムを乱します。これは、確立された低メチル化とBCL-2阻害との合理的で生物学に基づいた組み合わせを提供します。このアプローチは、AMLにおける精密医療の約束を象徴しています。
結論
アザシチジン、ベネトクラクス、およびレヴーメニブの組み合わせは、新規診断のNPM1変異またはKMT2A重配列AMLを有する高齢者において、安全で、非常に活性が高く、急速で深部の寛解を誘導することができます。より長期の追跡調査と大規模な無作為化試験が必要ですが、これらの知見は高リスクAMLの予後改善に向けて重要な一歩を表しています。医師は新規データに注意を払い、適切な患者の臨床試験参加を検討すべきです。AMLの治療環境は引き続き進化しています。
参考文献
Zeidner JF, Lin TL, Welkie RL, Curran E, Koenig K, Stock W, Madanat YF, Swords R, Baer MR, Blum W, Stein EM, Olin RL, Schiller G, Nichols A, Odenike O, Traer E, Lachowiez C, Duong VH, Hochman MJ, Cai SF, Smith C, Stefanos M, Martycz M, Huang Y, Rosenberg L, Marcus S, Chen TL, Yocum AO, Druker BJ, Levine RL, Borate U, Byrd JC, Mims AS. Azacitidine, Venetoclax, and Revumenib for Newly Diagnosed NPM1-Mutated or KMT2A-Rearranged AML. J Clin Oncol. 2025 Aug 10;43(23):2606-2615. doi: 10.1200/JCO-25-00914 .