亮点
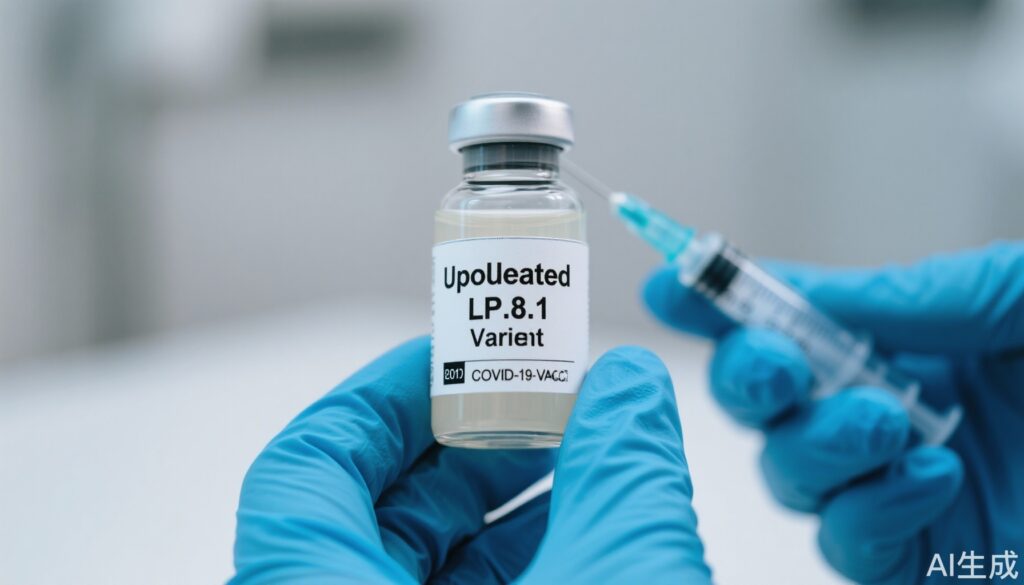
- 美国 FDA 批准了辉瑞和莫德纳更新的 COVID-19 疫苗,针对 LP.8.1 亚谱系。
- 疫苗适用于 65 岁及以上的成人,以及 5 至 64 岁有高风险基础疾病的个体。
- 辉瑞的 COMIRNATY 和莫德纳的 SPIKEVAX 和 mNEXSPIKE 疫苗在临床和临床前研究中显示了安全性和改善的免疫反应。
- 更新的疫苗已获得全球监管批准,准备立即分发。
研究背景和疾病负担
持续的 COVID-19 大流行继续对公共卫生构成重大挑战,特别是由于病毒能够进化并逃避免疫反应。SARS-CoV-2 的变异株出现了突变,可能降低疫苗的有效性,尤其是对老年人和有基础健康状况的个体,这些个体患严重 COVID-19 结果的风险增加。这些人群对住院、并发症和 COVID-19 死亡的高度易感性导致了未满足的医疗需求,需要更新的疫苗来应对流行的变异株,以维持保护性免疫力并减少疾病负担。
研究设计和监管批准背景
美国食品药品监督管理局(FDA)最近授予了辉瑞和莫德纳更新的 COVID-19 疫苗的补充生物制品许可申请(sBLA)批准。这些疫苗针对 LP.8.1 亚谱系,反映了病毒的抗原进化。
莫德纳的 SPIKEVAX 被更新并批准用于 6 个月至 64 岁有至少一种高风险基础疾病的个体,以及所有 65 岁及以上的成人。此外,莫德纳的新疫苗 mNEXSPIKE 获得批准用于 12 至 64 岁有符合条件的高风险条件的个体和 65 岁或以上的成人。
辉瑞的更新 COMIRNATY 疫苗被批准用于所有 65 岁及以上的成人和 5 至 64 岁有高风险条件的个体。这些决定基于临床试验数据,展示了安全性和有效性,包括 5-11 岁儿童组的数据,并由针对多种流行亚谱系的临床前免疫原性数据支持。
主要发现
两家制造商的疫苗都设计为增强对 LP.8.1 亚谱系的免疫力,符合 FDA 的指导原则。辉瑞疫苗的批准得到了数据的强烈支持,这些数据显示了强大的安全性特征和各年龄段(包括儿童)的改善中和抗体反应。临床试验包括预防有症状的 COVID-19 感染和评估不良事件的终点,这些终点符合 FDA 对有效性和安全性的标准。
莫德纳的更新疫苗也显示了强大的免疫原性和安全性特征。重要的是,mNEXSPIKE 疫苗扩展了年龄适应症,有效针对高风险人群。这些配方结合了更新的 mRNA 序列,以扩大对抗原漂移变异株的免疫覆盖范围。
更新的疫苗代表了 COVID-19 疫苗接种计划的战略演变,旨在面对病毒进化时保持保护。两家公司报告称,这些疫苗已准备好立即发货,并应在几天内可供临床医生使用,从而促进针对最脆弱人群的快速免疫接种活动。
专家评论
专家认为,FDA 批准这些更新的疫苗是适应 SARS-CoV-2 动态景观的免疫策略的关键步骤。结合特定变异株的序列增强了疫苗生物学上的合理性,以提高保护效果。值得注意的是,将适用范围扩展到有高风险条件的年轻患者反映了流行病学数据的演变,这些数据表明尽管进行了先前的免疫工作,但仍然存在持续的风险。
局限性包括长期有效性对抗新兴变异株仍在监测中,鉴于病毒突变的快速速度。此外,还需要更广泛的人群数据,以了解疫苗在一般人群中的效用范围,而不仅仅是高风险和老年成人。
结论
FDA 批准辉瑞和莫德纳更新的 COVID-19 疫苗,针对 LP.8.1 亚谱系,是保护高风险群体和老年成人免受当前 SARS-CoV-2 变异株侵害的重要进展。这些批准扩展了年龄和风险群体的适应症,并得到了严格的临床和免疫学数据的支持。立即可用性将使及时的疫苗接种努力得以实施,以减轻严重后果。持续的研究和监测仍然是解决持续的病毒进化和优化疫苗部署策略的关键。
参考文献
- FDA 新闻发布. FDA 批准针对特定人群的更新 COVID-19 疫苗. 2024.
- 莫德纳公司. FDA 批准更新的 SPIKEVAX 和 mNEXSPIKE 疫苗的新闻稿. 2024.
- 辉瑞公司. FDA 批准更新的 COMIRNATY 疫苗的新闻稿. 2024.
- 美国疾病控制与预防中心. 针对高风险个体的 COVID-19 疫苗接种指南. 2024.
- 世界卫生组织. COVID-19 变异株跟踪和疫苗建议. 2024.