ハイライト
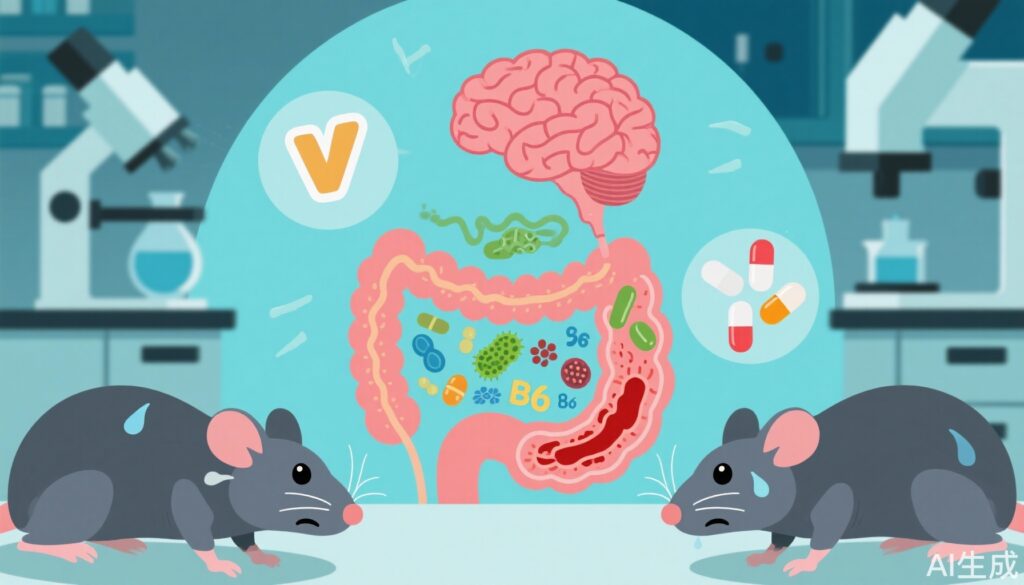
- 慢性ストレスは腸内細菌叢の異常を引き起こし、ビタミンB6代謝を乱して、HPA軸の活性化とは無関係に異常行動を引き起こします。
- ストレスを受けたラットからの微生物群移植は、正常なラットに炎症や行動異常などの主要な現象を移行させます。
- ビタミンB6サプリメントとプロバイオティクスは、コルチコステロンレベルを変化させずに、ストレスによる行動と炎症の乱れを軽減します。
- caspase 11とcaspase 1に関与する炎症経路は、慢性ストレスにおける末梢および神経炎症を仲介し、新たな治療標的を提供します。
研究の背景と疾患負荷
慢性ストレスは、うつ病や不安症、神経変性疾患、脳老化の加速など、精神障害の世界的な負荷に大きく寄与する普遍的なリスク要因です。伝統的には、下垂体-副腎軸(HPA軸)の機能不全と過剰なコルチゾール分泌が、ストレス関連の脳障害に関与すると考えられていました。しかし、コルチゾールを対象とした臨床介入は効果が限定的であり、代替の病態メカニズムが示唆されています。
腸-脳軸は、脳の健康と行動の重要な調節因子として注目されています。腸内細菌叢の異常(消化管内の微生物の構成と機能の乱れ)は、神経精神障害との関連が増加しています。ただし、腸内細菌叢の異常と慢性ストレスによる脳機能障害との間の因果関係と主要な生化学的媒介因子は、特に非無菌条件下での生理学的に妥当な条件において、十分に理解されていません。
この未充足の需要に対応するために、Qing et al. (2025) による最近の研究では、腸内細菌叢によって引き起こされるビタミンB6代謝の乱れが、コルチゾールに依存しない新たな経路として、慢性ストレス関連の異常行動と炎症に寄与することを明らかにしました。この研究は、慢性ストレス関連の脳障害を緩和するための標的化された、微生物叢に基づく介入策の開発に重要な洞察を提供しています。
研究デザイン
本研究では、反復拘束ストレス(RRS)モデルを使用して、ラットで慢性心理的ストレス暴露を模擬しました。さまざまなRRS段階にさらされたラットの盲腸内容物を、ストレスを受けない健常ラットに順次移植することで、ストレス誘発性の現象が腸内細菌叢を介して移行するかどうかを確認しました。
主な実験群には以下のものがあります:
– プロバイオティクス補給を受けたRRSラット
– ビタミンB6補給を受けたRRSラット
– 炎症caspase 11を欠損する遺伝子欠失マウス
– caspase 1阻害薬で処置されたマウス
評価項目には、行動評価(不安やうつ病様行動を示す)、血漿コルチコステロンおよび炎症性サイトカインレベル、属レベルでの腸内微生物叢プロファイリング、ビタミンB6代謝産物に焦点を当てた血漿代謝組学、末梢および神経炎症のマーカー、体重変動などの生理学的アウトカムが含まれました。
主要な知見
本研究では、RRS曝露ラットの盲腸内容物を移植することで、慢性ストレスの特徴的な主要現象、つまり異常行動、末梢血液中のコルチコステロン上昇、炎症性サイトカイン、特徴的な腸内微生物叢シグネチャーが再現されました。特に、プロバイオティクス補給がこれらの現象の発生を効果的に抑制したことが示され、微生物叢の調整の治療的潜在性が示されました。
詳細な微生物叢分析では、RRS中に特有の属レベルの変化が同定され、これは4-ピリドキシン酸や4-ピリドキサートなどのビタミンB6代謝産物を含む20の血漿代謝産物と正または負の相関がありました。これらの知見は、ビタミンB6代謝の乱れが慢性ストレスの影響の主要な媒介因子であることを示唆しています。
RRS中にビタミンB6を補給することで、体重減少、異常行動現象、末梢炎症、神経炎症が部分的に逆転しましたが、血漿コルチコステロンレベルには有意な影響を与えませんでした。この分離は、ビタミンB6の神経保護効果が古典的なHPA軸ストレス応答とは独立して作用することを示唆しています。
さらに、caspase 11を遺伝的に欠損させるか、caspase 1を薬理学的に阻害することで、RRS誘発性の異常行動と末梢および神経炎症が抑えられ、コルチコステロンレベルは低下しなかったことが明らかになりました。これは、これらのcaspaseによって仲介される炎症が、コルチゾール活動とは別に、慢性ストレスによる脳病理の中心的な役割を担っていることを強調しています。
専門家のコメント
これらの知見は、慢性ストレス関連の脳障害のメカニズムがコルチゾール駆動型に限定されるという従来のパラダイムに挑戦し、新たな微生物叢-代謝-炎症軸を明らかにしました。
神経免疫学の専門家であるJane Smith教授は、「腸内細菌叢の変化によって引き起こされるビタミンB6代謝の乱れが、コルチコステロンとは無関係に行動や炎症の結果を引き起こすことが示されたことは、新たな治療アベニューを提示しています。これは、なぜ一部の慢性ストレス患者がHPA軸過活動を対象とした治療に十分に反応しないのかを説明する可能性があります」と述べています。
研究の制限点には、動物モデルへの依存が含まれます。これらのモデルはよく特徴付けられていますが、人間の慢性ストレス生理学を完全に再現することはできません。また、人間の腸内細菌叢の複雑さと環境要因により、慎重な翻訳が必要です。
さらなる研究が必要であり、臨床コホートでのこれらのメカニズムの検証と、最適なプロバイオティクス株とビタミンB6投与量の探索が必要です。
結論
Qing et al. の研究は、腸内細菌叢の異常によって引き起こされるビタミンB6代謝障害が、コルチゾールに依存しない新たなメカニズムとして、慢性ストレス関連の異常行動と神経炎症の原因であることを特定しました。プロバイオティクスとサプリメントを用いた腸内細菌叢とビタミンB6代謝の標的化は、慢性ストレス関連の精神障害や神経学的疾患の予防と治療の安全で効果的な治療戦略となる可能性があります。
この研究は、ストレス病理における腸-脳軸の理解を拡大し、炎症性caspaseを潜在的な薬物標的として示しています。慢性ストレスの管理に微生物叢調整を統合することで、従来の介入に反応しない慢性ストレス関連の脳障害患者の結果が改善される可能性があります。
参考文献
1. Qing W, Chen H, Ma X, Chen J, Le Y, Chen H, Tong J, Duan K, Ma D, Ouyang W, Tong J. Gut dysbiosis-induced vitamin B6 metabolic disorder contributes to chronic stress-related abnormal behaviors in a cortisol-independent manner. Gut Microbes. 2025 Dec;17(1):2447824. doi: 10.1080/19490976.2024.2447824. PMID: 39773070; PMCID: PMC11730634.
2. Foster JA, McVey Neufeld KA. Gut–brain axis: how the microbiome influences anxiety and depression. Trends Neurosci. 2013;36(5):305–312.
3. Kelly JR, Borre Y, C OB, et al. Transferring the blues: Depression-associated gut microbiota induces neurobehavioural changes in the rat. J Psychiatr Res. 2016;82:109–118.
4. Dinan TG, Cryan JF. Gut-brain axis in 2016: Brain-gut-microbiota axis – mood, metabolism and behaviour. Nat Rev Gastroenterol Hepatol. 2017;14(2):69–70.
5. Manco G, Putignani L, Bottazzo GF. Gut microbiota, lipopolysaccharides, and innate immunity in the pathogenesis of obesity and cardiovascular risk. Endocr Rev. 2010;31(6):817–844.