ハイライト
- 狂犬病モノクローナル抗体(RmAb)と精製されたVERO細胞狂犬病ワクチン(PVRV)を組み合わせると、3級露出に対する有効な暴露後予防(PEP)が得られます。
- インドで行われた第4相、オープンラベル無作為化試験では、3994人の治療を受けた患者の1年間で狂犬病の発症は見られませんでした。
- RmAbとワクチンの安全性プロファイルは良好で、軽度で一時的な副作用のみが報告され、重篤な副作用は治療に関連していませんでした。
- 免疫原性は強固で、14日目以降も持続的な狂犬病ウイルス中和抗体レベルが確認されました。
研究背景と疾患負担
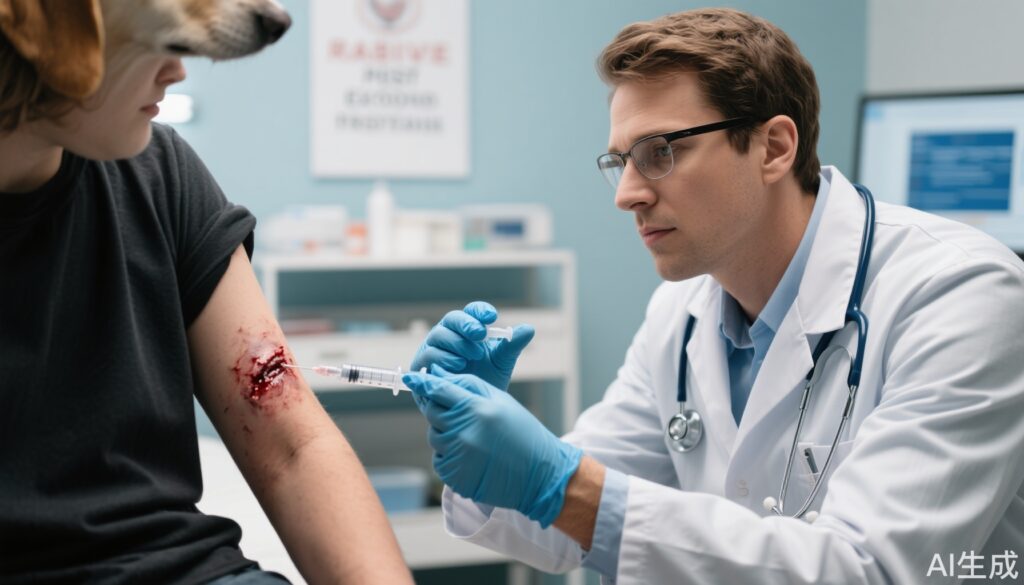
狂犬病は、臨床症状が発現すると普遍的に致死的なウイルス性動物由来感染症です。特にインドのような低・中所得国では、世界中で毎年数千人の死亡者を出す重要な疾患です。潜在的な狂犬病暴露後に疾患の発症を防ぐために、狂犬病免疫グロブリンによる被動免疫と積極的なワクチン接種を含む暴露後予防(PEP)が重要です。従来、被動免疫には馬由来の狂犬病免疫グロブリン(ERIG)が使用されていましたが、供給の制限、バッチ間の変動、および副作用のリスクなどの制限がありました。Rabishieldなどの狂犬病モノクローナル抗体(RmAb)の開発と承認により、より良い安全性、一貫した効力、および拡大可能性を持つ有望な被動予防の代替手段が導入されました。本研究では、WHO 3級疑い狂犬病露出に対するRmAbと精製VERO細胞狂犬病ワクチン(PVRV)を組み合わせたPEPレジメンの長期安全性、免疫原性、および有効性を、ERIGとPVRVの標準的な組み合わせと比較することを目的としています。
研究デザイン
この第4相、オープンラベル、無作為化、能動制御試験は、2019年8月から2022年3月までインドの15の三級医療施設で実施されました。対象者は、2歳以上のWHO 3級疑い狂犬病動物からの露出で、登録前の72時間以内または高リスク部位(顔、首、手、指)への露出の場合24時間以内に暴露があった人々でした。
参加者は3:1の割合で2つのグループに無作為に割り付けられました:(1) RmAb(Rabishield 3.33 IU/kg)とPVRV(Rabivax-S)、(2) ERIG(Equirab 40 IU/kg)とPVRV。両方の被動剤は、WHO 2018ガイドラインに従って、0日目に傷部及其周囲に浸透させました。各グループはさらに1:1の割合で、PVRVを皮内(0日目、3日目、7日目、28日目に0.1 mL + 0.1 mL)または筋肉内(0日目、3日目、7日目、14日目、28日目に1.0 mL)で投与されるように無作為に割り付けられました。
主要評価項目は、免疫化後365日までの治療関連重篤な有害事象(SAE)の発生率で、すべての治療を受けた参加者で評価しました。二次評価項目には、参加者のサブセットにおける狂犬病ウイルス中和抗体(RVNA)の幾何平均濃度(GMC)と、追跡期間中の狂犬病の発生が含まれました。
無作為化は、ランダムなブロックサイズ8の順列ブロックを使用し、中央のインタラクティブウェブレスポンスシステムで管理されました。本研究はオープンラベルで、参加者や施設スタッフには盲検化が行われませんでした。
主要な知見
合計4059人の参加者が登録され、無作為化され、3994人が治療を受けました(RmAbとPVRVグループ2996人、ERIGとPVRVグループ998人)。そのうち3622人(90.7%)が1年間の完全な追跡調査を完了しました。
安全性:
- RmAbグループで11件、ERIGグループで17件の有害事象(AE)が治療との因果関係があると考えられました。
- ほとんどのAEは軽度で一時的であり、予想されるワクチン接種後の反応と一致していました。
- RmAbグループで7件のSAEが発生しましたが、すべて治療とは無関係と判定されました。
- ERIGグループで1件の重篤なAEが治療との因果関係があると判定されました。
免疫原性:
- 暴露後14日目に、RmAbグループではRVNAの幾何平均濃度が16.05 IU/mL(95% CI 13.25–19.44)、ERIGグループでは13.48 IU/mL(95% CI 9.51–19.11)に上昇しました。
- GMCの比率の点推定値は1.19(95% CI 0.82–1.72)で、両グループ間の免疫原性が同等であることを示唆しています。
有効性:
- 1年間の追跡調査期間中に、どの参加者にも狂犬病の発症は報告されず、両レジメンによる効果的な保護が示されました。
追加のサブグループ分析では、ワクチンの投与経路(皮内または筋肉内)が免疫原性や安全性の結果に大きな影響を与えていないことが確認されました。
専門家コメント
本研究は、疑い狂犬病動物への3級露出患者におけるRmAbと精製VERO細胞狂犬病ワクチンを組み合わせたPEP戦略の使用を支持する堅固な証拠を提供しています。確立されたERIGレジメンと比較して同等の免疫応答と安全性プロファイルは、RmAbが伝統的な免疫グロブリンの代わりに使用できる可能性を示しており、供給と副作用の制限を克服することができます。
特に、WHO 2018ガイドラインに厳密に準拠した浸透と接種スケジュールは、これらの知見の臨床的意義を強化しています。オープンラベルデザインは、有害事象報告における潜在的な評価バイアスの観点から制限とみなされるかもしれませんが、大規模なサンプルサイズと長い追跡期間は信頼性を向上させます。
治療を受けた患者に狂犬病の発症がないことは、高リスク集団におけるこのレジメンの保護効果を確認しています。また、持続的な抗体レベルは、狂犬病予防における持続的な免疫を示唆しており、重要な考慮事項となっています。
これらの知見は、感染症管理におけるモノクローナル抗体療法への世界的な関心の高まりと一致し、スケーラブルで標準化された被動免疫化の選択肢を提供しています。
結論
狂犬病モノクローナル抗体と精製VERO細胞狂犬病ワクチンの組み合わせは、WHO 3級狂犬病露出に対する安全で耐容性が高く効果的な暴露後予防です。インドで行われたこの第4相臨床試験は、12ヶ月の追跡期間中に長期的な免疫原性、良好な安全性プロファイル、および0件の狂犬病発症を示し、改善された被動免疫化戦略に対する重要なニーズを満たしています。
RmAbベースの予防策の実装は、特に馬由来の免疫グロブリンへのアクセスが制限されている地域で、狂犬病PEPの利用可能性と標準化を向上させる可能性があります。
今後の研究では、費用対効果、アクセス性、および地域の狂犬病対策プログラムへの統合を探索するとともに、多様な集団における実世界の有効性をモニタリングする必要があります。
参考文献
Kulkarni PS, Potey AV, Kapse D, Bhamare C, Gawande A, Munshi R, Pawar S, Gogtay NJ, Agarwal A, Tambe M, Thakre S, Samuel CJ, Khan SMS, S RH, Rana D, Singh N, Kamath V, Bhalla HL, Poonawalla CS, Mani RS, Gunale B; RAB-04 study group. Post-exposure prophylaxis regimen of rabies monoclonal antibody and vaccine in category 3 potential exposure patients: a phase 4, open-label, randomised, active-controlled trial. Lancet. 2025 Aug 9;406(10503):627-635. doi: 10.1016/S0140-6736(25)00735-4. PMID: 40783290.
World Health Organization. WHO Expert Consultation on Rabies. Third report. WHO Technical Report Series, No. 1012. Geneva: WHO; 2018.