ハイライト
- オブリクタミグ(BI 764532)は、DLL3/CD3 IgG様T細胞エンゲージャーで、DLL3陽性の小細胞肺がん(SCLC)や神経内分泌がん患者を対象とした第1相用量増加試験で評価されました。
- この研究では、ステップアップ投与法を含む複数の投与スケジュールが検討され、最大耐容用量に達することなく忍容性が確立されました。
- 治療関連サイトカイン放出症候群(CRS)は一般的でしたが、主に管理可能かつ逆転可能でした。
- 全コホートにおける全体奏効率(ORR)は23%で、最高の奏効率は肺大細胞神経内分泌がん(70%)で観察されました。
- これらの結果は、これらの難治性DLL3発現腫瘍に対するオブリクタミグのさらなる臨床調査を支持しています。
研究の背景と疾患負担
小細胞肺がん(SCLC)や肺外神経内分泌がん(epNEC)、肺大細胞神経内分泌がん(LCNEC-L)は、予後が不良で治療選択肢が限られている侵襲的な悪性腫瘍です。特に多次の治療を受けた後でも、DLL3(デルタ様リガンド3)はSCLCや関連する神経内分泌がんで過剰発現し、正常組織ではほとんど存在しないため、治療標的として魅力的です。現在の治療法は効果が限定的で持続的な奏効は稀であり、新しい戦略が必要とされています。オブリクタミグ(BI 764532)は、CD3陽性T細胞をDLL3発現腫瘍細胞に誘導して免疫介在性細胞障害を引き起こす双特異的T細胞エンゲージャーで、DLL3陽性腫瘍を治療する新しい免疫療法アプローチを提供します。
研究デザイン
この初回ヒト試験の第1相、オープンラベル、多施設の用量増加試験では、以前に治療を受けたDLL3陽性のSCLC、epNEC、またはLCNEC-Lを有する168人の患者が登録されました。対象患者の多くは、免疫チェックポイント阻害薬(51%)を含む複数の前治療を受けていました。オブリクタミグは、以下の4つの投与スケジュールで静脈内投与されました:
– スケジュールA: 固定用量、3週間に1回
– スケジュールB1: 固定用量、週1回
– スケジュールB2: 週1回、2週間のステップアップ投与、その後週1回の目標用量
– スケジュールB3: 週1回、3週間のステップアップ投与、3週間の目標用量投与、その後3週間に1回
主要目的は最大耐容用量(MTD)の決定でした。副次的目的には安全性プロファイル、薬物動態評価、RECISTバージョン1.1に基づく腫瘍反応評価が含まれました。
主要な知見
168人の患者のうち、72%が少なくとも2つの抗癌治療を受けた経験があり、重篤な前治療を経験した集団を反映していました。MTD評価中に7つの用量制限毒性(DLTs)が発生しました。これはスケジュールAで1件、スケジュールB2で6件で、MTDは達成されませんでした。
最も頻繁な治療関連有害事象(AE)はサイトカイン放出症候群(CRS)で、各スケジュールで57%の患者で発生しました。しかし、グレード3以上のCRSは3%に留まり、症状は通常早期に現れ、適切な管理により逆転可能でした。その他の有害事象はT細胞エンゲージャーの予想される安全性プロファイルと一致していました。
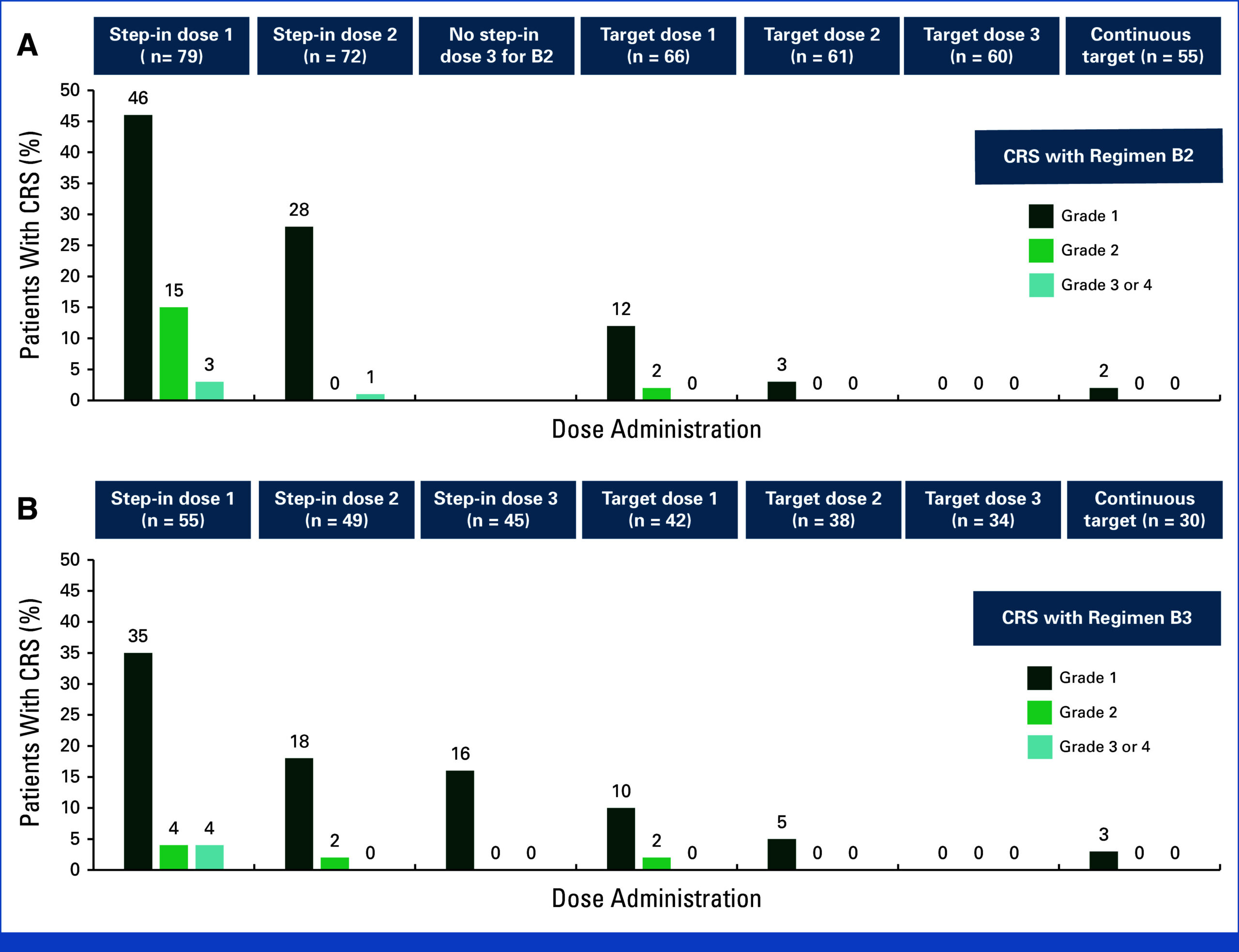
Incidence of CRS by administration of obrixtamig in patients treated with (A) Regimen B2 and (B) Regimen B3. CRS, cytokine release syndrome.
全スケジュールと腫瘍タイプを組み合わせた効果解析では、全体奏効率(ORR)が23%(95%信頼区間[CI]、17.4%〜30.2%)でした。奏効期間(DoR)の中位値は8.5ヶ月(95% CI、6.2〜未達)、6ヶ月のDoR率は70%(95% CI、53%〜88%)で、奏効者において持続的な臨床ベネフィットが示されました。
最小有効用量(≥90 μg/kg)を投与されたスケジュールB2/B3の患者に焦点を当てると、ORRは28%(95% CI、20.7%〜35.9%)に改善し、最適化された投与スケジュールによる効果の向上が示されました。
スケジュールB2/B3の腫瘍特異的奏効率は以下の通りでした:
– 小細胞肺がん: 21% ORR(95% CI、12.9%〜33.1%)
– 肺外神経内分泌がん: 27% ORR(95% CI、17.4%〜39.6%)
– 肺大細胞神経内分泌がん: 70% ORR(95% CI、39.7%〜89.2%)
これらの知見は、特にLCNEC-Lにおいて、著しい抗腫瘍活性を示しており、これまでの治療成功が限られていたサブタイプでの効果を示しています。
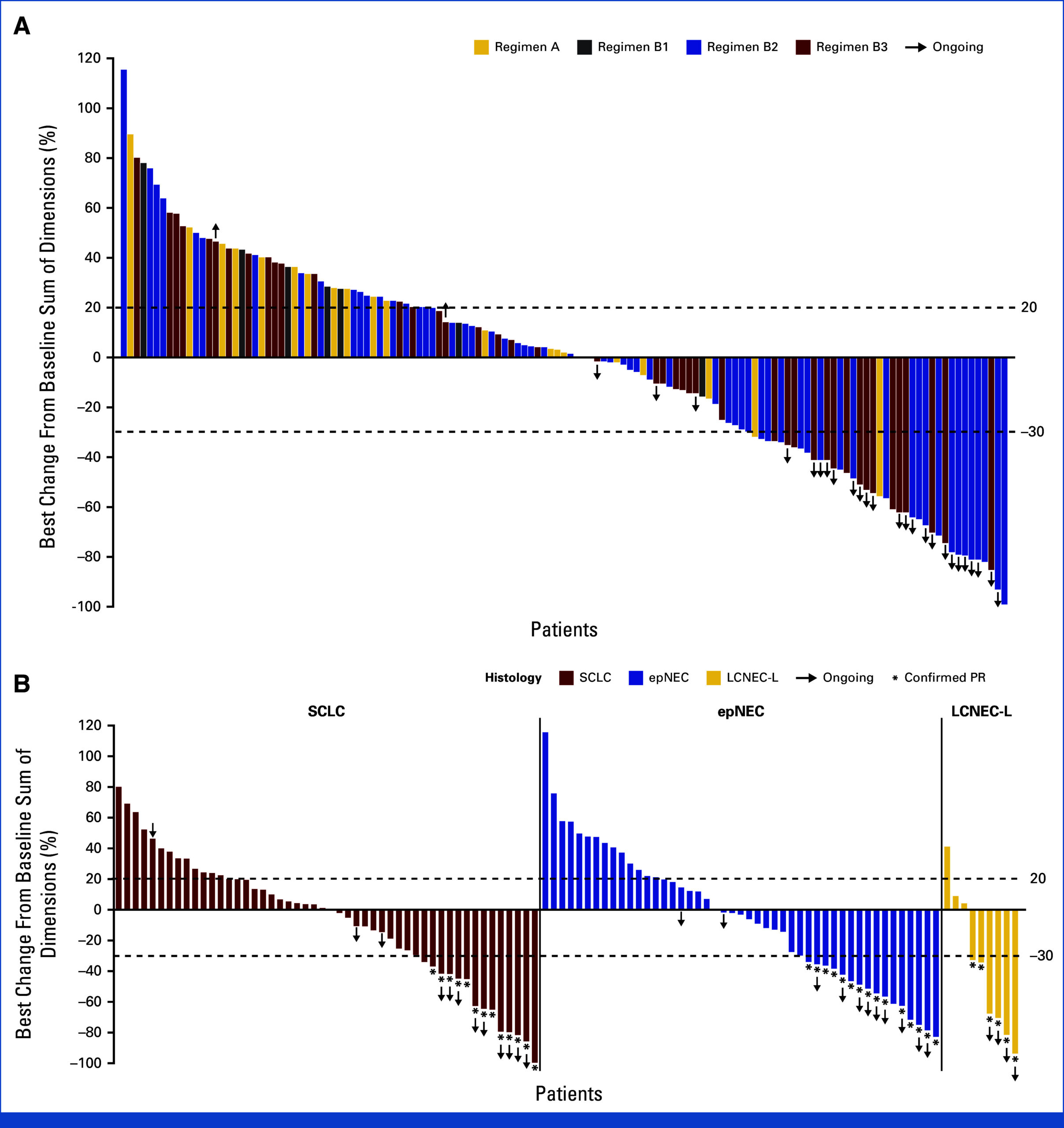
Antitumor effects of obrixtamig in patients with DLL3-positive SCLC, epNEC, and LCNEC-L. (A) Best percentage change in tumor dimensions from baseline for all assessable patients (investigator-assessed efficacy set). Of the 164 patients who started treatment 7 weeks before the data cutoff and were therefore included in the efficacy analysis set, 24 discontinued treatment before the first tumor assessment and were therefore excluded from waterfall plot analysis. A total of 140 of 164 patients had measurable tumors at baseline and postbaseline assessments. (B) Best percentage change in tumor dimensions from baseline in patients who received Regimen B2 or B3 (≥90 μg/kg obrixtamig once weekly and once weekly for 3 weeks [once every 3 weeks thereafter], respectively) by tumor type (investigator-assessed efficacy set). DLL3, delta-like ligand 3; epNEC, extrapulmonary neuroendocrine carcinoma; LCNEC-L, large cell neuroendocrine carcinoma of the lung; PR, partial response; SCLC, small cell lung cancer.
薬物動態評価では、血漿中濃度の用量依存性増加が確認され、使用された投与スケジュールを支持しています。
専門家のコメント
オブリクタミグの第1相結果は、DLL3という臨床的に利用するのが難しい抗原を標的とする免疫療法における有望な進歩を示しています。主に軽度から中等度のCRSが早期に解決され、T細胞エンゲージャーの既知の毒性と一致する管理可能な安全性プロファイルは、良好な結果を示しています。DLTsが観察されたにもかかわらずMTDが達成されなかったことは、比較的広い治療窓を示唆しています。
重篤な前治療を経験した患者集団、特に以前に抗PD-1/PD-L1療法を受けた患者における持続的な奏効は、オブリクタミグの新たな治療モダリティとしての潜在的な臨床的重要性を強調しています。特に、効果的な治療法が限られている侵襲的なLCNEC-Lにおける高い奏効率は注目に値します。
本研究の制限点には、初期フェーズの設計と比較群の欠如が含まれており、慎重な解釈が必要です。さらなる第II/III相試験が、効果の確認、最適な投与スケジュールの定義、組み合わせアプローチの探索を行い、ベネフィットの向上を目指すことが重要です。
メカニズム的には、オブリクタミグの双特異的結合により、細胞性免疫細胞を直接腫瘍部位に誘導することが可能となり、従来の抗原提示の必要性を回避し、神経内分泌腫瘍に一般的な腫瘍免疫回避戦略を克服できる可能性があります。
結論
オブリクタミグの第1相用量増加試験は、重篤な前治療を経験したDLL3陽性の小細胞肺がんや神経内分泌がん患者における有望な忍容性と初步的な効果を示しています。週1回または3週間に1回の目標用量(90〜1080 μg/kg)までのステップアップ投与スケジュールは、管理可能な安全性と23%の全体奏効率を示し、奏効の持続性が注目されます。
特に、肺大細胞神経内分泌がんにおける高い奏効率は、さらなる集中した調査を必要とします。これらの結果は、オブリクタミグの治療的役割をより明確に定義し、DLL3発現神経内分泌悪性腫瘍の治療パラダイムへの最適な統合を追求するための継続的および将来の臨床試験を正当化しています。
参考文献
Wermke M, Gambardella V, Kuboki Y, Felip E, Sanmamed MF, Alese OB, Sayehli CM, Arriola E, Wolf J, Villaruz LC, Bertulis J, Studeny M, Bouzaggou M, Fang X, Morgensztern D. Phase I Dose-Escalation Results for the Delta-Like Ligand 3/CD3 IgG-Like T-Cell Engager Obrixtamig (BI 764532) in Patients With Delta-Like Ligand 3+ Small Cell Lung Cancer or Neuroendocrine Carcinomas. J Clin Oncol. 2025 Sep 20;43(27):3021-3031. doi: 10.1200/JCO-25-00363 IF: 41.9 Q1 . Epub 2025 Jul 24. PMID: 40706016 IF: 41.9 Q1 ; PMCID: PMC12440289 IF: 41.9 Q1 .
追加の支援文献:
– Rudin CM, et al. Small cell lung cancer. Nat Rev Dis Primers. 2021;7(1):3.
– Stewart CA, et al. Targeting DLL3 in pulmonary neuroendocrine tumors. Cancer Immunol Res. 2020;8(2):177-182.
– Sigma-Aldrich T-Cell Engager Mechanism Review. ImmunoOncology. 2023;9(4):254-263.