研究背景与疾病负担
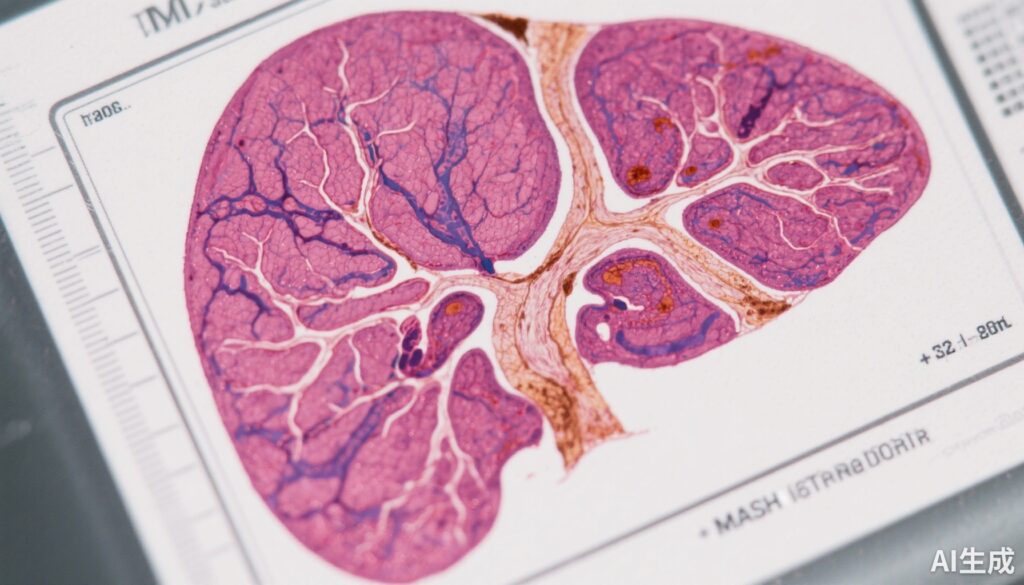
代谢功能障碍相关性脂肪性肝炎(MASH),以前被认为是非酒精性脂肪性肝炎(NASH)的一部分,是一种日益普遍的肝脏疾病,其特征是肝脏炎症、脂肪变性和进行性纤维化,通常与2型糖尿病和肥胖等代谢并发症有关。MASH中的纤维化进展会增加肝硬化、肝衰竭和肝细胞癌的风险,目前尚缺乏获批的治疗药物,这构成了重要的临床挑战。MASH的发病机制涉及血糖调节异常、慢性低度炎症和脂质代谢异常。
游离脂肪酸受体(FFARs),特别是FFAR1和FFAR4,是表达在多种细胞类型上的G蛋白偶联受体,包括肝细胞、免疫细胞和胰岛β细胞。它们调节葡萄糖稳态、胰岛素敏感性和炎症反应,表明它们作为MASH治疗靶点的吸引力。二十碳丁酸是一种口服双重FFAR1/FFAR4激动剂,旨在通过这些机制改善肝脏组织学和全身代谢参数。
研究设计
ICONA研究是一项为期52周的IIb期、多中心、随机、安慰剂对照试验,旨在评估口服二十碳丁酸在成人MASH患者中的安全性和有效性,这些患者的纤维化分期为F1至F3(轻度至重度纤维化但无肝硬化)。共有187名患者以1:1:1的比例随机分配接受每日一次口服300毫克二十碳丁酸、600毫克二十碳丁酸或安慰剂治疗。主要终点是在600毫克组中,一年内实现MASH组织学缓解且纤维化无恶化的患者比例。
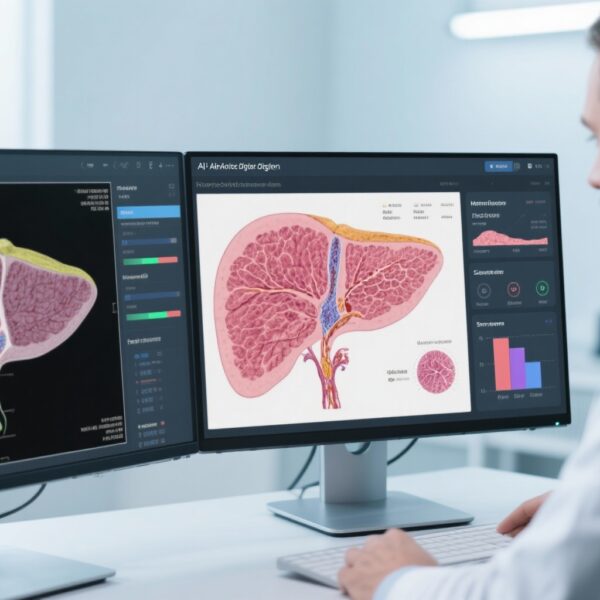
次要终点包括通过常规组织病理学和人工智能辅助数字病理学评估的≥1级纤维化改善、肝损伤和炎症的循环生物标志物变化、血糖控制参数以及安全性和耐受性指标。
关键发现
在分析的187名患者中(安慰剂组n=62;300毫克组n=58;600毫克组n=67),600毫克二十碳丁酸组在MASH缓解且纤维化无恶化方面显示出数值上的优势,但未达到统计显著性(23.9% vs. 14.5%;比值比2.01;95% CI 0.8至5.08;p=0.13)。尽管未达到预设的主要终点,但这些结果表明潜在的趋势。
重要的是,300毫克和600毫克二十碳丁酸组在≥1级纤维化改善方面的比例高于安慰剂组:300毫克组为29.3%(比值比2.89;95% CI 1.09至7.70),600毫克组为23.9%(比值比2.4;95% CI 0.90至6.37),而安慰剂组为11.3%。这一纤维化益处得到了人工智能辅助数字病理学的验证,该方法提供了对纤维化变化的敏感和定量测量。
此外,接受二十碳丁酸治疗的患者表现出明显的血清生物标志物减少,这些标志物指示肝损伤和炎症。还观察到与血糖控制相关的代谢参数有所改善,这与FFAR1/FFAR4的机制作用一致。
安全性分析显示,二十碳丁酸总体上耐受良好,报告了轻度至中度的治疗出现的不良事件。值得注意的是,未观察到药物引起的肝损伤,这在易发生肝相关不良事件的人群中显示出良好的安全性。
专家评论
ICONA试验提供了早期阶段的令人鼓舞的证据,支持在MASH中靶向FFAR1和FFAR4的治疗。尽管未能在统计学上显著达到主要组织学终点,但在常规和新型人工智能基础组织学评估中观察到的稳健纤维化改善突显了二十碳丁酸的潜力。鉴于纤维化分期是MASH不良临床结局的最强预测因子,抗纤维化效果尤其具有临床意义。
纤维化改善与MASH缓解缺乏统计显著性的不一致可能源于研究的统计功效、疾病的异质性或组织学终点的已知局限性。人工智能辅助数字病理学增加了检测传统评分无法识别的细微纤维化变化的创新和更敏感的视角。
未来的挑战包括优化患者选择,亚组分析表明,纤维化分期较重(F2-F3)且伴有2型糖尿病的患者可能获益更大。结合代谢和抗炎效应可以解决MASH的多方面病理生理学,支持二十碳丁酸的治疗原理。
需要更大规模、富集队列和更长时间随访的未来研究来确定明确的临床益处和对肝相关结局的影响。ICONA数据补充了新兴证据,表明FFAR激动剂是脂肪肝疾病的一种可行的药物类别。
结论
二十碳丁酸的IIb期ICONA研究显示,在纤维化MASH患者中具有良好的安全性,并且有令人鼓舞的纤维化改善证据。尽管未达到MASH缓解且纤维化无恶化的首要终点,但总体的组织学、生物标志物和代谢数据支持进一步临床开发二十碳丁酸。这包括在纤维化分期较重和代谢并发症的患者中进行潜在的靶向使用。二十碳丁酸可能是解决MASH关键致病轴的创新治疗策略,这是肝病领域的一个迫切需求。
参考文献
Harrison SA, Alkhouri N, Ortiz-Lasanta G, Rudraraju M, Tai D, Wack K, Shah A, Besuyen R, Steineger HH, Fraser DA, Sanyal AJ; ICONA Study Investigators. A phase IIb randomised-controlled trial of the FFAR1/FFAR4 agonist icosabutate in MASH. J Hepatol. 2025 Aug;83(2):293-303. doi: 10.1016/j.jhep.2025.01.032. Epub 2025 Feb 10. PMID: 39938653.