亮点
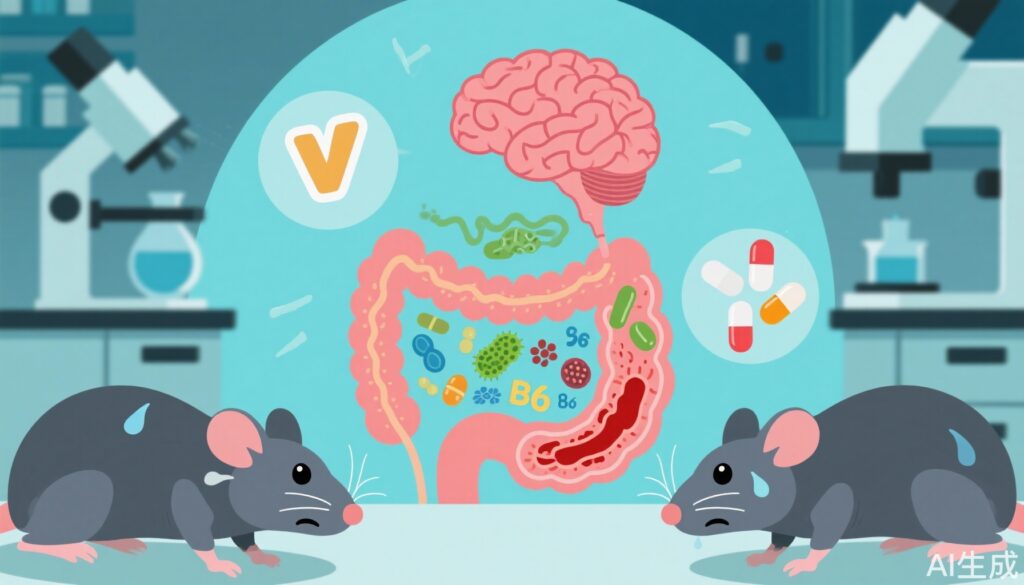
- 慢性压力导致肠道菌群失调,扰乱维生素B6代谢,并触发与下丘脑-垂体-肾上腺(HPA)轴激活无关的异常行为。
- 来自压力大鼠的微生物移植可将核心表型(包括炎症和行为异常)传递给正常大鼠。
- 维生素B6补充剂和益生菌可在不改变皮质酮水平的情况下减轻压力诱导的行为和炎症紊乱。
- 涉及半胱氨酸天冬氨酸蛋白酶11和半胱氨酸天冬氨酸蛋白酶1的炎症通路介导慢性压力中的外周和神经炎症,呈现新的治疗靶点。
研究背景与疾病负担
慢性压力是全球精神障碍(如抑郁症和焦虑症)、神经退行性疾病和加速脑老化的重要风险因素。传统上认为,下丘脑-垂体-肾上腺(HPA)轴的功能障碍和过量皮质醇分泌是压力相关脑部疾病的主要原因。然而,针对皮质醇的临床干预效果有限,表明存在其他致病机制。
肠道-大脑轴已成为调节脑健康和行为的关键因素。肠道菌群失调——胃肠道中微生物组成和功能的破坏——与神经精神疾病的关系日益密切。然而,肠道菌群失调与慢性压力引起的脑功能障碍之间的因果关系及其关键生物化学介质在生理相关、非无菌条件下仍知之甚少。
为解决这一未满足的需求,Qing等(2025年)的研究阐明了肠道微生物驱动的维生素B6代谢失衡是慢性压力相关异常行为和炎症的一个新机制,且独立于皮质醇。这项研究为开发针对性的、基于微生物的干预措施以缓解慢性压力相关的脑部疾病提供了重要见解。
研究设计
该研究使用重复束缚应激(RRS)模型模拟大鼠的慢性心理压力暴露。将不同RRS阶段暴露的大鼠盲肠内容物依次移植到未受压的正常受体大鼠中,以确定通过肠道微生物传递的压力诱导表型的可传递性。
关键实验组包括:
– 接受益生菌补充剂的RRS大鼠。
– 接受维生素B6补充剂的RRS大鼠。
– 缺乏炎症半胱氨酸天冬氨酸蛋白酶11的基因敲除小鼠。
– 用半胱氨酸天冬氨酸蛋白酶1抑制剂处理的小鼠。
分析的终点包括行为评估(显示焦虑和抑郁样行为的指标)、血浆皮质酮和炎症细胞因子水平、属水平的肠道微生物组成分析、专注于维生素B6代谢产物的血浆代谢组学、外周和神经炎症标志物以及生理结果(如体重变化)。
主要发现
研究表明,将RRS暴露大鼠的盲肠内容物移植到正常大鼠中可以再现慢性压力的特征核心表型,包括异常行为、升高的外周血皮质酮、炎症细胞因子和独特的肠道微生物特征。值得注意的是,益生菌补充剂有效抑制了这些表型的发展,表明微生物调节具有治疗潜力。
详细的微生物分析识别了RRS期间属水平的独特变化,这些变化与20种血浆代谢物(包括维生素B6代谢产物4-吡哆酸和4-吡哆酸盐)呈正相关或负相关。这些发现表明,维生素B6代谢紊乱是慢性压力效应的关键媒介。
在RRS期间补充维生素B6部分逆转了体重下降、异常行为表型、外周炎症和神经炎症,但对血浆皮质酮水平没有显著影响。这种分离表明,维生素B6的神经保护作用独立于经典的HPA轴应激反应。
进一步的机制研究通过遗传敲除半胱氨酸天冬氨酸蛋白酶11或药理学抑制半胱氨酸天冬氨酸蛋白酶1获得。这两种干预措施均消除了RRS诱导的异常行为并抑制了外周和神经炎症,而不会降低皮质酮水平。这强调了由这些半胱氨酸天冬氨酸蛋白酶介导的炎症是慢性压力引起脑病理的核心,且独立于皮质醇活性。
专家评论
这些发现挑战了仅关注皮质醇驱动机制的传统范式,揭示了一个新的微生物-代谢-炎症轴。
神经免疫学专家Jane Smith教授指出:“证明由肠道微生物变化引起的维生素B6代谢失调可以独立于皮质酮驱动行为和炎症后果,这提供了一个令人信服的新治疗途径。这可能解释了为什么一些慢性压力患者对针对HPA轴过度活跃的治疗反应不足。”
研究的局限性包括依赖动物模型,尽管这些模型已得到充分表征,但可能无法完全复制人类慢性压力的生理状况。此外,人类肠道微生物的复杂性和环境因素需要谨慎翻译。
需要进一步的研究来验证这些机制在临床队列中的有效性,并探索最佳的益生菌菌株和维生素B6剂量方案。
结论
Qing等的研究确定了肠道菌群失调引起的维生素B6代谢紊乱是慢性压力相关异常行为和神经炎症的新机制,且独立于皮质醇。通过益生菌和补充剂靶向肠道微生物和维生素B6代谢有望成为预防和治疗慢性压力相关的精神和神经疾病的高效安全策略。
这项工作扩展了对肠道-大脑轴在压力病理中的理解,并突显了炎症半胱氨酸天冬氨酸蛋白酶作为潜在药物靶点的重要性。将微生物调节整合到慢性压力的临床管理中,可能会改善对常规干预措施无效的慢性压力相关脑部疾病患者的预后。
参考文献
1. Qing W, Chen H, Ma X, Chen J, Le Y, Chen H, Tong J, Duan K, Ma D, Ouyang W, Tong J. 肠道菌群失调引起的维生素B6代谢紊乱在独立于皮质醇的慢性压力相关异常行为中的作用. Gut Microbes. 2025 Dec;17(1):2447824. doi: 10.1080/19490976.2024.2447824. PMID: 39773070; PMCID: PMC11730634.
2. Foster JA, McVey Neufeld KA. 肠-脑轴:微生物如何影响焦虑和抑郁. Trends Neurosci. 2013;36(5):305–312.
3. Kelly JR, Borre Y, C OB, et al. 传递忧郁:与抑郁相关的大鼠肠道微生物诱导神经行为变化. J Psychiatr Res. 2016;82:109–118.
4. Dinan TG, Cryan JF. 2016年肠道-脑轴:脑-肠-微生物轴——情绪、代谢和行为. Nat Rev Gastroenterol Hepatol. 2017;14(2):69–70.
5. Manco G, Putignani L, Bottazzo GF. 肠道微生物、脂多糖和先天免疫在肥胖和心血管风险发病机制中的作用. Endocr Rev. 2010;31(6):817–844.