背景
急性増悪性慢性肝不全(ACLF)は、異なる原因を持つ慢性肝疾患患者の急性悪化から生じる多面的な症候群で、短期死亡率が高く、世界的な健康影響が大きいです。欧州のCLIF基準(主にアルコールやC型肝炎に関連する集団から得られたもの)や中国のCOSSH基準(B型肝炎ウイルス(HBV)が流行している地域で開発されたもの)など、地域的に確立された複数の診断枠組みがありますが、現在では、世界中で適用可能な実用的な診断および予後システムがありません。特に、C型肝炎の減少とアルコール関連肝障害の増加という世界的な疫学的傾向の変化により、多様な集団で良好な成績を収めるフレームワークの評価が不可欠です。
研究デザイン
この前向き多施設研究では、2018年1月から2023年8月まで、慢性肝疾患の急性悪化で入院した5,288人の患者が登録されました。HBVおよび非HBV原因(アルコール、自己免疫性、寄生虫性、薬剤誘発性、HCV関連原因)を含む多様な原因が含まれています。患者は入院時に、欧州CLIF基準と中国COSSH基準の両方を使用してACLFの存在を評価しました。さらに、7つの予後スコア(COSSH-ACLF IIスコア(COSSH-ACLF IIs)、China-CLIFs(CLIF-C ACLFsを改訂)、CLIF-C ACLFs、MELD、MELD-Na、MELD 3.0、NACSELD-ACLFs)が、28日および90日の肝移植(LT)なし死亡予測の性能を評価しました。検証は、ヨーロッパとラテンアメリカ(CANONIC、PREDICT、ACLARA)からの3つの大規模な非アジア系コホートで行われ、合計4,072人の患者が対象となりました。広範な臨床、検査所見、結果データが系統的に収集され、分析されました。
主要な知見
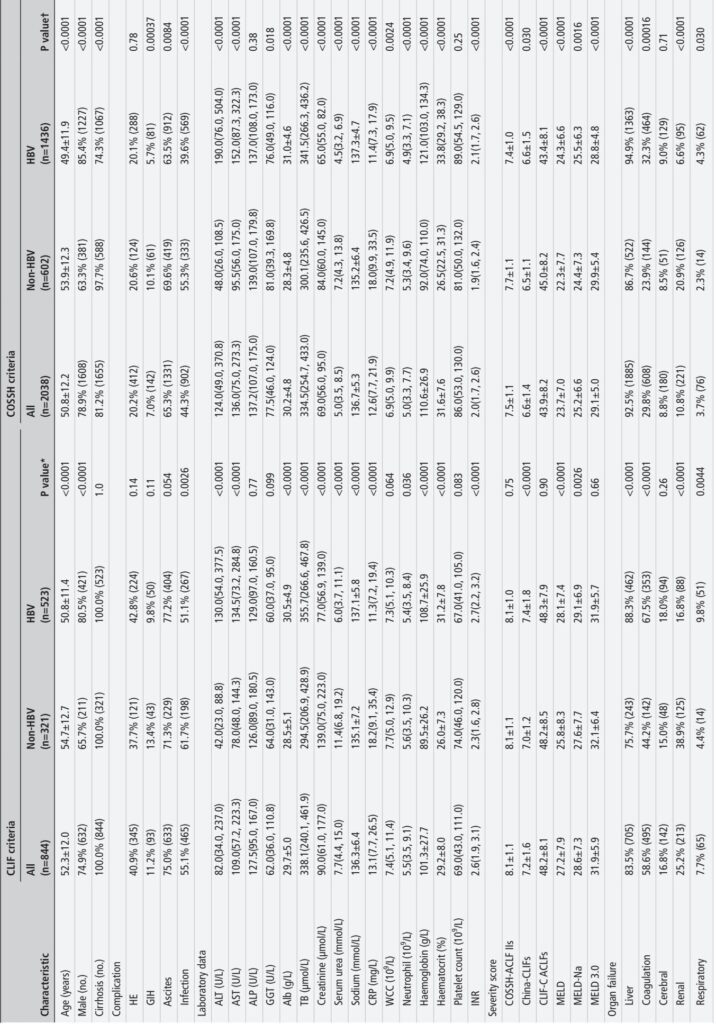
1. 診断性能: COSSH基準は2,038人のACLF患者(38.5%)を特定し、CLIF基準で特定された844人(16.0%)よりも大幅に多かったです。COSSH基準は、器官障害と高い死亡率を示す22.6%の重症患者を追加で捉え、そのうち14.2%はCLIF基準で見逃されていた非HBV患者でした。
2. 死亡率と重症度分布: COSSHで分類されたACLF患者の28日/90日のLTなし死亡率(27.3%/41.0%)は、CLIFで分類された患者(40.7%/57.0%)よりも有意に低く、COSSHがより軽度だが臨床的に重要な疾患を持つ患者を含むことを反映しています。COSSH基準は、ACLFグレード1から3までの合理的なピラミッド型分布(63.4%/27.5%/9.1%)を生成し、CLIFのグレード2への偏り(25.8%/56.3%/17.9%)よりも優れています。
3. 器官障害プロファイル: 原因によって異なる器官障害パターンが観察されました。HBV-ACLFは肝臓と凝固機能障害の頻度が高いのに対し、非HBV-ACLF患者は腎機能障害が主でした。COSSH基準は、非肝硬変患者や単一の肝障害とINR上昇を伴う患者を含めることで、これらの違いをよりよく反映しています。
4. 予後性能: COSSH-ACLF IIスコアは、すべてのACLF患者と原因において28日および90日のLTなし死亡予測の識別力が優れており、CLIF-C ACLFや他の確立されたスコアを上回りました。優れた校正性能と、低リスク、中リスク、高リスクグループに有意に異なる死亡リスクを有する効果的なリスク層別化を示しました。
5. 外部検証: 非アジア系検証コホートでは、China-CLIFsスコアが主に非HBV原因の肝硬変患者の死亡予測においてCLIF-C ACLFと同等の性能を示し、MELDベースのモデルやNACSELD-ACLFsを大幅に上回りました。尿素値が欠落していたためCOSSH-ACLF IIsの直接的な外部検証は困難でしたが、マッチしたサブセット解析では同等の予後精度が示されました。
専門家コメント
この包括的な研究は、HBVと非HBV人口を含むACLFの全スペクトラムを対象とした診断および予後フレームワークの評価に重要なギャップを埋めています。多様な世界的なコホートでの厳密な検証により、既存の基準(CLIFは過小診断、NACSELDは非常に重症な症例に焦点を当てる)の限界が明らかになり、中国-CLIFフレームワーク(COSSHとCLIFの要素を統合)の感度とバランスの取れた特異性が確認されました。
COSSHの拡張された包含基準は、早期の集中的管理や移植の検討が必要な高リスク患者の大きな部分を捉えます。特に、COSSH-ACLF II予後スコアの予測有効性が高く、変数が少ないため、臨床的な実装が容易になる可能性があります。
ただし、制限点として、地域による診断のばらつき、単一時間点のスコアリングに依存すること(動的な評価なし)、異なる医療システムや新興原因(代謝機能障害関連脂肪肝疾患(MASLD)など)における広範な外部検証の必要性があります。将来の研究では、多オミクスバイオマーカーを統合することで、生物学的に駆動される分類が得られ、ACLFの個別化治療が改善される可能性があります。
結論
中国-CLIFフレームワークは、多様な肝疾患の原因と地理的範囲にわたって敏感な、堅牢で広く適用可能なACLFの診断および予後システムを提供します。アジアと西洋の定義間の以前のギャップを橋渡しすることで、ACLFの命名法の調和、リスクのある患者の早期識別、治療の優先順位付けの向上に貢献します。このフレームワークの採用は、ACLF管理の格差を削減し、国際協力を通じて治療の進歩を促進することが期待されます。
参考文献
1. Arroyo V, Moreau R, Jalan R. Acute-on-Chronic Liver Failure. N Engl J Med. 2020;382:2137–45.
2. Moreau R, Gao B, Papp M, et al. Acute-on-chronic liver failure: A distinct clinical syndrome. J Hepatol. 2021;75:S27–35.
3. Wu T, Li J, Shao L, et al. Development of diagnostic criteria and a prognostic score for hepatitis B virus-related acute-on-chronic liver failure. Gut. 2018;67:2181–91.
4. Moreau R, Jalan R, Gines P, et al. Acute-on-chronic liver failure is a distinct syndrome that develops in patients with acute decompensation of cirrhosis. Gastroenterology. 2013;144:1426–37.
5. Jalan R, Yurdaydin C, Bajaj JS, et al. Toward an Improved Definition of Acute-onChronic Liver Failure. Gastroenterology. 2014;147:4–10.
6. Bernal W, Jalan R, Quaglia A, et al. Acute-on-chronic liver failure. Lancet. 2015;386:1576–87.
7. Sarin SK, Choudhury A. Acute-on-chronic liver failure: terminology, mechanisms and management. Nat Rev Gastroenterol Hepatol. 2016;13:131–49.
8. Karvellas CJ, Bajaj JS, Kamath PS, et al. AASLD Practice Guidance on Acute-on-chronic liver failure and the management of critically ill patients with cirrhosis. Hepatology. 2024;79:1463–502.
9. Luo J, Li J, Li P, et al. Acute-on-chronic liver failure: far to go—a review. Crit Care. 2023;27:259.
10. Zaccherini G, Weiss E, Moreau R. Acute-on-chronic liver failure: Definitions, pathophysiology and principles of treatment. JHEP Rep. 2021;3:100176.