ハイライト
- レティファニリマブをカルボプラチンとパクリタキセルに追加すると、進行性肛門扁平上皮がん患者の無増悪生存期間(PFS)が有意に改善した。
- 併用療法は管理可能な安全性プロファイルを示し、有害事象の頻度は標準化学療法と同等であった。
- この第3相試験の結果、レティファニリマブとカルボプラチン・パクリタキセルの併用は、進行性肛門扁平上皮がんの一線治療として新たな標準となる可能性がある。
研究背景と疾患負荷
肛門扁平上皮がん(SCAC)は希少だが、近年その発生率が増加しており、ヒトパピローマウイルス(HPV)感染との関連性が高い。進行性または転移性の症例では予後が不良で、プラチナ製剤ベースの化学療法後の治療選択肢は限られている。歴史的に、手術不能な局所再発または転移性SCACの一線治療は、InterAACT試験により確立されたカルボプラチンとパクリタキセルが標準となってきた。しかし、予後は依然として不十分であり、より効果的な治療法に対する明確な未充足ニーズがある。PD-1/PD-L1経路を標的とする免疫療法は、SCACを含むいくつかの上皮性がんにおいて有望な結果を示しており、特に疾患進行後に効果が見られる。レティファニリマブはPD-1阻害薬であり、プラチナ製剤による治療を受けた後のPD-L1陽性進行性SCACにおいて臨床効果を示している。POD1UM-303/InterAACT-2試験は、標準的なカルボプラチン・パクリタキセルにレティファニリマブを組み込むことで、この高リスク集団の臨床成績が改善するかどうかを評価することを目的として設計された。
研究デザイン
POD1UM-303/InterAACT-2は、世界規模の多施設、二重盲検、プラセボ対照、ランダム化第3相試験である。EU、オーストラリア、日本、英国、米国など12カ国の70施設で実施され、手術不能な局所再発または転移性SCACを持つ成人(18歳以上)、ECOGパフォーマンスステータス0または1、既往の全身療法なし、HIV陽性の場合は感染が良好に制御されている(CD4+ >200/μL、ウイルス量検出不能)患者が対象となった。対象患者(n=308)は1:1で、レティファニリマブ(500 mg 静脈内投与、4週間ごと)またはプラセボを、標準的なカルボプラチン・パクリタキセルと併用して最大1年間投与される群に無作為に割り付けられた。疾患進行が確認された場合、プラセボ群の患者はレティファニリマブ単剤療法に切り替えることができた。主要評価項目はRECIST v1.1に基づく独立評価者による無増悪生存期間(PFS)であり、副次評価項目には全生存期間、奏効率、安全性が含まれていた。有効性分析は、インテンション・トゥ・トリート(ITT)解析で行われた。
主要な知見
2020年11月から2023年7月の間に、308人の患者が2つの群に均等に無作為に割り付けられた。対象集団は主に女性(72%)で、地理的に多様な地域からの患者が含まれていた。レティファニリマブの追加は、PFSの臨床的および統計学的に有意な改善をもたらした。
– 中央値PFS:レティファニリマブ群では9.3か月(95% CI 7.5-11.3)、プラセボ群では7.4か月(7.1-7.7)。
– 無増悪または死亡のハザード比(HR):0.63(95% CI 0.47-0.84)、一側p=0.0006。これは、進行または死亡のリスクが37%減少することを示している。
重篤なまたはグレード3以上の有害事象は、レティファニリマブ群(47.4%と83.1%)でプラセボ群(38.8%と75.0%)よりも頻繁に観察された。最も一般的なグレード≥3の事象は、中性粒球減少症(35.1% vs 29.6%)と貧血(19.5% vs 20.4%)であった。レティファニリマブ群では4件の致死的有害事象が発生した(うち1件が治療関連と判断された:全血球減少症)、プラセボ群では1件(治療関連ではない)。
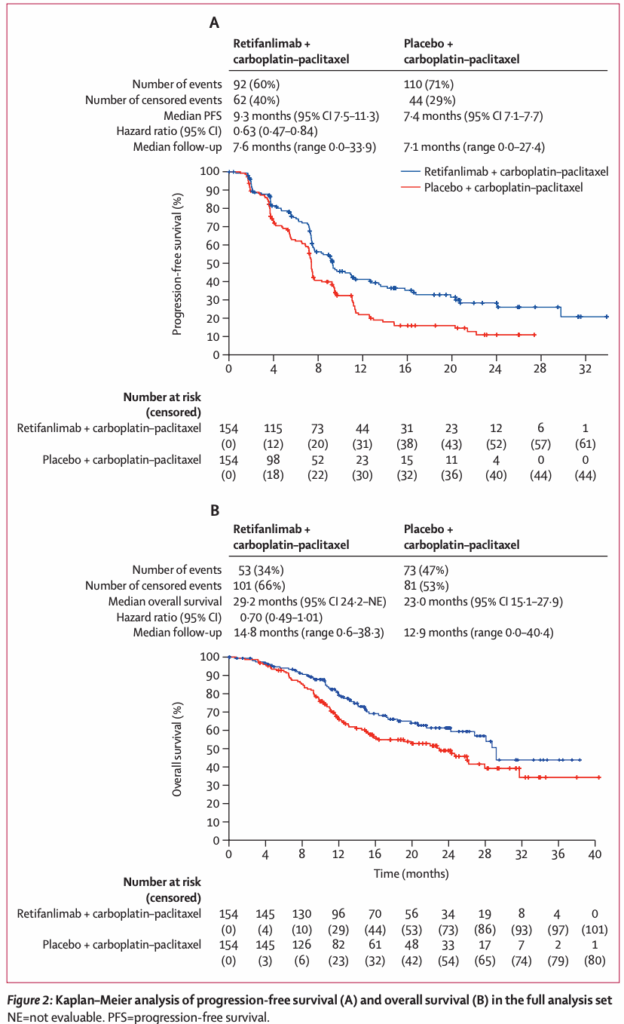
全生存期間(OS)に関するデータは報告時点では未熟であったが、観察されたPFSの利益と管理可能な毒性プロファイルは、臨床的に意義のある進歩を示している。試験のクロスオーバー設計は、免疫療法試験における一般的な課題であるため、OSの違いを緩和する可能性がある。
専門家のコメント
カルボプラチン・パクリタキセルにレティファニリマブを追加することは、10年以上にわたって進行性SCACの一線治療における初めての大きな進歩を代表している。PFSの改善幅(約2か月)は、歴史的に選択肢が限られていた疾患において顕著である。安全性プロファイルは、高グレードの有害事象の頻度が増加しているものの、免疫チェックポイント阻害薬と細胞障害性化学療法の期待通りである。
最近の編集後記やガイドラインの解説で示されるように、専門家の意見は、この試験が新しい標準治療を設定する上で重要であることを強調している。試験には、重要なリスク集団であるHIV感染者が含まれているため、汎用性が向上している。制限点としては、未熟なOSデータと高い毒性負荷があり、これは慎重な患者モニタリングが必要であることを意味する。また、倫理的に適切なクロスオーバー設計は、初期併用療法による長期生存利益を不明瞭にする可能性がある。
メカニズム的には、HPV関連SCACの免疫原性と、同様の腫瘍タイプでのPD-1阻害の確立された効果を考えると、レティファニリマブの活性は生物学的に説明可能である。免疫療法を補助療法ではなく早期の治療過程に組み込むことは、固形腫瘍オンコロジーにおける進化するパラダイムに沿っている。
結論
POD1UM-303/InterAACT-2試験は、手術不能な局所再発または転移性SCACの一線治療として、レティファニリマブとカルボプラチン・パクリタキセルの併用を新たなエビデンスに基づく治療法として確立した。PFSの改善と管理可能な安全性プロファイルは、即時的な臨床実践への統合を支持している。全体生存期間の継続的なフォローアップとさらなる現実世界の研究は、この治療法の長期的影響と最適な患者選択についての情報を提供する。医師は、免疫関連毒性のモニタリングと多職種チームによる管理を行うことによって、患者の利益を最大化すべきである。
参考文献
1. Rao S, Samalin-Scalzi E, Evesque L, Ben Abdelghani M, Morano F, Roy A, Dahan L, Tamberi S, Dhadda AS, Saunders MP, Casanova N, Guimbaud R, Lievre A, Maurel J, Fakih M, Tian C, Harrison J, Jones MM, Cornfeld M, Spano JP, Rochefort P; POD1UM-303/InterAACT-2 study investigators. Retifanlimab with carboplatin and paclitaxel for locally recurrent or metastatic squamous cell carcinoma of the anal canal (POD1UM-303/InterAACT-2): a global, phase 3 randomised controlled trial. Lancet. 2025 Jun 14;405(10495):2144-2152. doi: 10.1016/S0140-6736(25)00631-2 IF: 88.5 Q1 . PMID: 40517007 IF: 88.5 Q1 .
2. Kim S, et al. Immunotherapy in the management of anal cancer: From current evidence to future directions. J Immunother Cancer. 2023;11(7):e006745.
3. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Anal Carcinoma. Version 2.2024. Accessed June 2024.