序論
心拍出量維持型心不全(HFpEF)は最も一般的な心不全の形態で、肥満や2型糖尿病などの代謝性疾患を頻繁に合併します。これらの併存疾患は症状の負担、機能障害、心血管リスクを増大させます。この大きな疾患負担にもかかわらず、特に代謝機能障害のある集団における有効な治療法は限られています。
最近の無作為化比較試験では、グルカゴン様ペプチド-1(GLP-1)受容体作動薬であるセマグルチドと、二重のグルコース依存性インスリン促進ポリペプチド(GIP)/GLP-1受容体作動薬であるティルゼパチドが、肥満関連のHFpEFの臨床症状を改善することが示されています。しかし、これらの研究はサンプルサイズが小さく、臨床イベントが少ないこと、および選択性の高い適合基準によって制限されており、汎用性が限られ、規制承認や臨床ガイドラインへの取り組みが阻害されていました。
本研究では、大規模な米国の保険請求データベースを使用して、セマグルチドとティルゼパチドの有効性と安全性について堅固な実世界の証拠を生成することを目指しました。研究では、解析手法を基軸試験(セマグルチドのSTEP-HFpEF DMとティルゼパチドのSUMMIT)と比較し、より広範な患者集団を対象に適合基準を拡大し、セマグルチドとティルゼパチドの直接比較を行い、臨床判断を支援しました。
研究デザインと方法
メディケアA・B・D部分、オプトム・クリンフォーマティクス・データ・マート、メラティブ・マーケットスキャン(2018年〜2024年)のデータを使用し、研究者は5つの活性比較新規使用者コホート研究を構築しました。これは、STEP-HFpEF DM(セマグルチド)とSUMMIT(ティルゼパチド)試験のコホートエミュレーションを用いて研究デザインを基準化した後、適合基準を拡大して通常の臨床実践を反映する患者を含むようにしました。
セマグルチドまたはティルゼパチドの新規使用者は、DPP-4阻害薬であるシタグリプチンの新規使用者と比較されました。シタグリプチンは、以前の試験で心不全に対して中立的な影響を示しているため、心不全のアウトカムに対するプラセボプロキシとして考慮されました。最終的なコホートでは、ティルゼパチドの新規使用者とセマグルチドの新規使用者を直接比較しました。対象となる患者は、HFpEFの診断、肥満(BMIの閾値は試験と一致または拡大)、2型糖尿病、心血管および代謝性併存疾患の安定した臨床プロファイルを有することが必要でした。
主要なアウトカムは、治療開始後52週間内の心不全入院または全原因死亡の複合アウトカムでした。二次アウトカムには、静脈内利尿薬が必要な緊急心不全訪問や主要複合アウトカムの個々の成分が含まれました。安全性のエンドポイントは、消化器系の有害事象、重症細菌感染症、尿路感染症を評価しました。
混雑因子は、人口統計学的特性、代謝性疾患の負荷、併存疾患、併用薬、医療利用、虚弱指数、利用可能な場合の検査値を含む広範な共変量を用いたプロペンシススコア重み付けによって厳密に対処されました。
基準化指標は、データベースエミュレーションと無作為化試験結果との整合性を評価し、方法論的妥当性への信頼性を高めました。負のコントロールアウトカム(腰部神経根症、腹部ヘルニア)が含まれて、潜在的な残存混雑因子を評価しました。事前に指定されたサブグループ解析では、年齢、性別、BMIによる治療効果が検討されました。
主要な知見
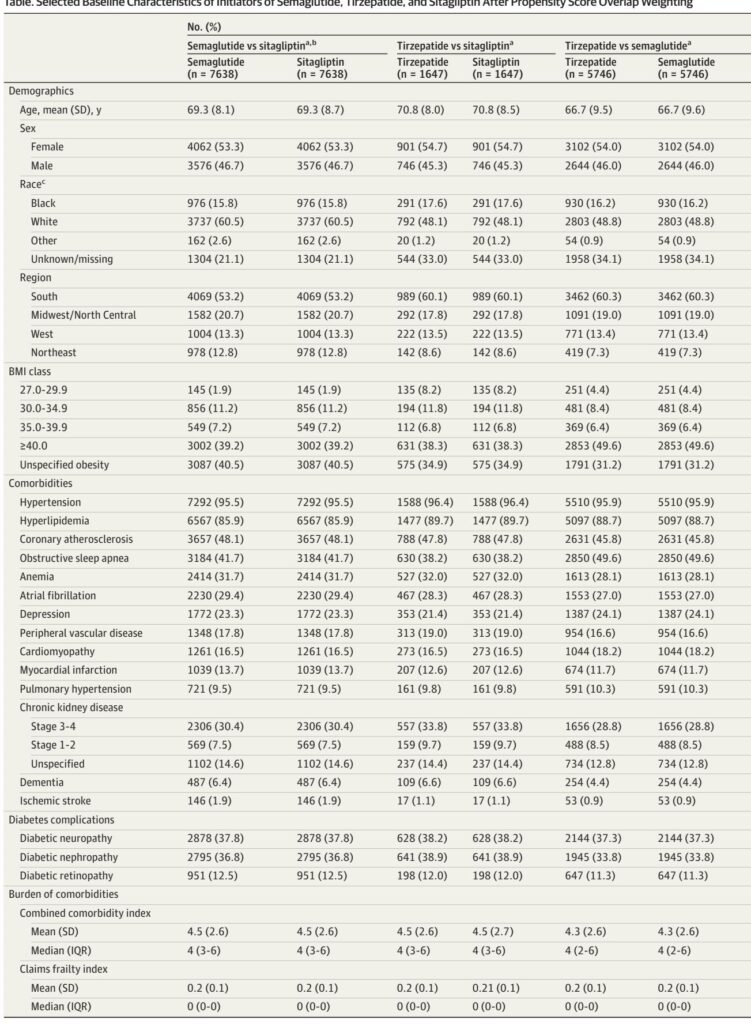
1. 患者集団:適合基準を適用した後、セマグルチド対シタグリプチンのコホートは58,333人、ティルゼパチド対シタグリプチンのコホートは11,257人、拡大された適合基準に基づくティルゼパチド対セマグルチドの比較コホートは28,100人となりました。プロペンシススコア重み付け後の基本的特性は良好にバランスが取れており、平均年齢は66.7〜70.8歳、女性の割合は約53〜55%、平均BMIは36.6〜40.2でした。
2. 基準化:STEP-HFpEF DMとSUMMIT試験のデータベースエミュレーションは、心不全入院と死亡アウトカムの試験ハザード比と高い一致を示し、解析手法の妥当性を確認しました。
3. 主要アウトカム – セマグルチド対シタグリプチン:1年間の心不全入院または全原因死亡のリスクは、セマグルチド群では5.5%(95%信頼区間、4.9〜6.1)、シタグリプチン群では8.6%(95%信頼区間、7.9〜9.3)であり、相対リスク低減率は42%(ハザード比0.58;95%信頼区間、0.51〜0.65)に対応しました。1件のイベントを防ぐために必要な治療数(NNT)は31でした。
4. 主要アウトカム – ティルゼパチド対シタグリプチン:ティルゼパチドは、相対リスク低減率が58%(ハザード比0.42;95%信頼区間、0.31〜0.57)であり、1年間のイベント発生率は3.6%対7.5%、NNTは26でした。
5. 直接比較 – ティルゼパチド対セマグルチド:主要複合アウトカムに有意な違いは見られず(ハザード比0.86;95%信頼区間、0.70〜1.06)、1年間の観察リスクはほぼ同一(3.3%対3.4%)であり、有効性が同等であることを示唆しました。
6. 二次アウトカム:セマグルチドとティルゼパチドは、シタグリプチンと比較して、より広範な複合アウトカムや個別のエンドポイント、特に心不全入院と全原因死亡を低減させ、効果サイズは一貫していました。
7. 安全性:セマグルチドやティルゼパチドでは、消化器系の有害事象、重症細菌感染症、尿路感染症の有意な増加は見られませんでした。
8. サブグループと感度解析:年齢、性別、BMIのサブグループ間で治療効果は一貫しており、広範な感度解析、特に広範なアウトカム定義の使用や意図治療アプローチにおいても堅牢でした。負のコントロール解析では有意な関連は見られず、妥当性を支持しました。
専門家のコメント
これらの実世界の知見は、早期の臨床試験の証拠を補強し、心不全と代謝性疾患を合併するHFpEFにおけるGLP-1受容体作動薬ベースの治療法の使用を支持しています。観察された心血管ベネフィットの急速な発現はSELECT試験の結果と一致し、体重減少以外の早期心不全改善メカニズムが介在している可能性を示唆しています。
ティルゼパチドは他の設定では優れた血糖低下効果と体重減少効果を示していますが、本研究では心不全の低減においてセマグルチドよりも明確な優位性は見られず、医師は患者特異的な要因、可用性、耐容性に基づいてどちらの薬剤を選択してもよいことを支持しています。
重要なのは、本研究が堅固な観察研究の強さを示していることです。大規模なデータベースを活用することで、無作為化試験の知見を確認し、拡張し、規制決定やガイドライン決定を支援し、臨床試験で過小評価されている集団のギャップを埋めています。
制限点には、観察研究のデザイン、広範な調整にもかかわる残存混雑因子の可能性、治療曝露の処方調剤データへの依存、標準化された臨床測定(心不全症状評価や左室駆出率測定など)の欠如があります。しかし、無作為化試験との基準化と検証された請求データアルゴリズムの使用により、一部の懸念が緩和されます。
結論
肥満関連のHFpEFと2型糖尿病を有する患者において、セマグルチドまたはティルゼパチドの投与開始は、中立的な血糖低下薬であるシタグリプチンと比較して、心不全の入院や全原因死亡を大幅に削減(40%以上)させることが示されました。ティルゼパチドとセマグルチドの有効性に有意な違いは見られませんでした。
これらの知見は、心不全と代謝性疾患を合併するHFpEFの管理におけるGLP-1受容体作動薬治療法の統合を支持し、ランダム化試験を補完する実世界の証拠の価値を強調しています。
視覚的プレゼンテーションプロンプト
左室駆出率が維持されたMRIまたは心エコー画像を表示し、GLP-1受容体作動薬の心臓および代謝組織への作用を示す分子経路をオーバーレイ表示します。心不全と代謝性疾患を合併するHFpEFの潜在的な治療ターゲットを強調します。