亮点
- BIOLAP试验是首个大规模、随机、自身对照研究,比较了双侧腹腔镜下腹股沟疝修补术中生物网片与合成网片的效果。
- 术后6个月时,患者报告的疼痛水平在生物网片与合成网片之间没有显著差异。
- 与合成网片相比,生物网片表现出显著更高的2年疝复发率(11.2% vs 2.5%)和更高的血清肿形成率(33.4% vs 21.6%)。
- 这些发现不支持在常规腹腔镜下腹股沟疝修补术中从合成网片转向生物网片。
研究背景
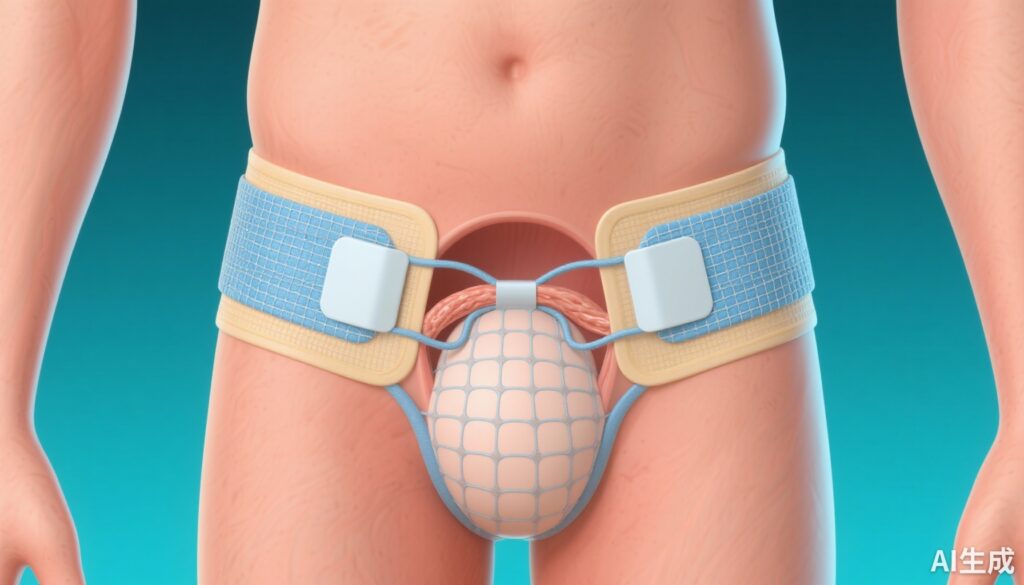
腹股沟疝修补术是全球最常进行的一般外科手术之一。尽管技术有所进步,但慢性术后疼痛和疝复发仍然是影响患者生活质量及长期预后的重大并发症。合成网片植入物一直是加强腹股沟底部的标准选择,可降低复发风险,但关于慢性疼痛和异物反应的担忧仍然存在。
生物网片由可吸收的天然材料制成,被提议作为可能通过减少慢性炎症反应来减轻术后疼痛的替代品。然而,关于疼痛、复发和术后并发症等结果的有力比较数据仍缺乏,特别是在可以进行无张力修补的腹腔镜方法中,网片的选择可能会对结果产生影响。
研究设计
生物网片与合成网片在腹腔镜下腹股沟疝修补术中的对比(BIOLAP)试验是一项多中心、随机、患者和评估者盲法、自身对照临床试验,涉及491名成年患者,均为原发性双侧腹股沟疝。该试验于2017年8月至2021年2月在德国21个认证的疝中心进行,采用随机分配网片类型的方法,即每名患者的右侧或左侧接受一种类型的网片,确保每位患者作为自身的对照。
所有患者均接受了标准化的腹腔镜修补技术——经腹膜前修补术(TAPP)或全腹膜外修补术(TEP)。一侧接受生物网片植入,另一侧接受合成网片。主要结局指标包括6个月时的疼痛强度(通过视觉模拟量表(VAS)评估)和2年时的疝复发率。次要结局指标包括血清肿、血肿、手术部位感染和患者满意度。
关键发现
试验纳入的患者主要是男性(93.1%),平均年龄为58.5岁。分析显示,术后6个月时,生物网片侧和合成网片侧在静息状态下的疼痛水平没有显著差异,两组的VAS评分均非常低(0.3 ± 0.9;P = .76)。
然而,在长期疝复发方面出现了显著差异:生物网片的2年复发率明显较高(11.2%,53例复发)相比合成网片(2.5%,12例复发),具有高度统计学意义(P < .001)。这代表生物网片的复发相对风险增加了约四倍。
次要结局进一步突显了生物网片的安全问题。生物网片侧的血清肿形成率显著增加(33.4% vs 21.6%;P < .001),这是一种可能延长恢复时间并增加发病率的并发症。未报告血肿或手术部位感染率有显著差异。
患者满意度在不同网片类型之间没有显著差异,与报告的低疼痛水平一致。
专家评论
BIOLAP试验的自身对照设计是一种强有力的方法学优势,有效控制了个体间的变异性,这是网片比较研究中常见的局限性。患者和评估者的盲法进一步减少了偏倚。
尽管理论上生物网片具有生物相容性,但未能减少疼痛,这挑战了其在减少慢性术后疼痛方面的假设。观察到的显著较高的复发率表明,生物网片可能无法提供足够的机械强度或耐久性以承受腹股沟疝修补术中的应力,尤其是在腹腔镜方法中。
生物网片的血清肿形成增加可能与其固有的吸收和组织重塑过程有关,导致液体积聚。这引发了对术后并发症和需要额外干预的担忧。
局限性包括2年的随访期;需要更长期的结果。此外,研究人群主要为男性,且在德国的高度专业化中心治疗,这可能影响其在其他人群或手术环境中的推广性。
结论
BIOLAP随机临床试验明确表明,生物网片在腹腔镜下腹股沟疝修补术中并不比合成网片具有术后疼痛优势。更重要的是,它们与显著增加的疝复发风险和血清肿形成相关。这些发现不支持在使用腹腔镜技术的原发性双侧腹股沟疝修补术中常规使用生物网片。
对于临床医生而言,合成网片仍然是在这种情况下耐用且安全的疝修补加固材料的金标准。未来的研究应集中在改进网片材料以减少疼痛和并发症而不损害耐久性,以及探索个性化的治疗方法。
参考文献
Seefeldt CS, Knievel J, Deeb M, Hoedt NT, Rudroff C, Essen R, Antoine D, Kaiser GM, Jacobi CA, Gross-Weege W, Gänsler W, Lammers BJ, Bonk C, Hildebrandt F, Carus T, Meyer M, Bebobru M, Krökel A, Dornbusch J, Schneider M, Cerasani N, Stechemesser B, Lefering R, Bulian DR, Ströhlein MA, Rieger A, Lange J, Meyer-Zillekens JS, Eisenberger CF, Heiss MM. 生物网片与合成网片在腹腔镜下腹股沟疝修补术中的对比:BIOLAP随机临床试验。JAMA Surg. 2025年10月8日。doi: 10.1001/jamasurg.2025.4071. 网络首发。PMID: 41060645。试验注册:德国临床试验注册号:DRKS00010178。