ハイライト
- プロヌクレア転移(PNT)によるミトコンドリア寄与は、胚の生存可能性と互換性があり、mtDNA疾患の伝播を大幅に軽減します。
- 着床前遺伝子検査(PGT)は、病原性mtDNAヘテロプラズミーが低または存在しない胚を効果的に識別し、ヘテロプラズミック変異を持つ女性にとっての代替手段を提供します。
- 最近のコホートでは、PNTにより8人の生児が生まれ、病原性mtDNA負荷が著しく軽減されました。PGTでは、ヘテロプラズミーが最小限に抑えられた18人の生児が生まれました。
- PNTとPGTを組み合わせた統合的なアプローチは、ホモプラズミックおよびヘテロプラズミックmtDNA変異を持つ女性のニーズに対応し、生殖選択肢を拡大します。
臨床的背景と疾患負担
ミトコンドリアDNA(mtDNA)疾患は、mtDNAの病原性変異によって引き起こされる重篤な多臓器障害です。母系のみから遺伝するこれらの疾患は、神経学的、筋肉系、心臓系、代謝系に影響を与える多様な症状を呈します。ヘテロプラズミー—細胞内に野生型と変異型のmtDNAが共存すること—は疾患の重症度と現象性を決定します。ホモプラズミック(すべてのmtDNAコピーが影響を受けている)または高レベルのヘテロプラズミック病原性変異を持つ女性は、これらの疾患を子孫に伝える高いリスクがあります。現在の管理オプションは限られており、しばしば困難な生殖的決定を強いられることがあります。
研究方法
この研究は、New England Journal of Medicine(Hyslop LA et al., 2025)に発表され、病原性mtDNA変異を持つ女性に対する2つの先進的な生殖介入法—プロヌクレア転移(PNT)によるミトコンドリア寄与と着床前遺伝子検査(PGT)—を評価しました。
ヘテロプラズミック変異を持つ女性にはPGTが提供され、変異型mtDNAが低または検出できない胚を選択することができます。ホモプラズミックまたは高レベルのヘテロプラズミック変異を持つ女性、つまりPGTが実行不可能な女性には、PNTが提供されます。PNTは、変異型ミトコンドリアを持つ卵子から核ゲノムを取り出し、健康なミトコンドリアを持つ脱核化された寄与者卵子に移植し、その後、単精虫卵子内注射(ICSI)を行うことを含みます。主要エンドポイントには、胚の生存可能性、妊娠率、生児数、子供のヘテロプラズミーレベルが含まれます。
主要な知見
コホートでは、22人の女性がPNTを受け、39人がPGTを受け、それぞれICSIに従いました。PNTグループでは36%(8/22)、PGTグループでは41%(16/39)で臨床的妊娠が確認されました。PNTは8人の生児と1つの継続中の妊娠につながり、PGTは18人の生児を産みました。
PNT後に生まれた乳児の血中ヘテロプラズミーレベルは、検出不能から16%まででした。特に、6人の乳児では、脱核化された受精卵と比較して病原性mtDNA変異レベルが95〜100%減少しており、残りの2人は77〜88%減少していました。PGTでは、18人の乳児のうち10人にヘテロプラズミーデータがあり、レベルは検出不能から7%まででした。これらの結果は、子供のmtDNA疾患のリスクが大幅に軽減していることを示しています。
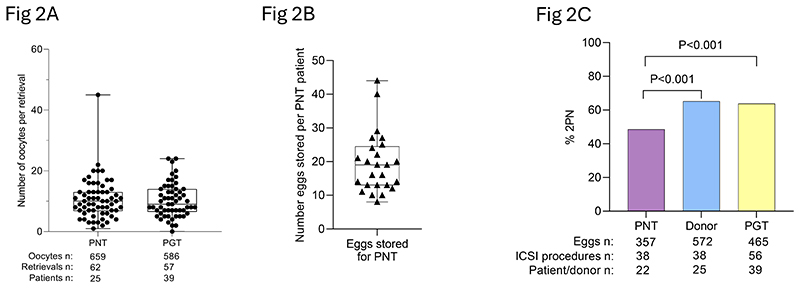
Oocyte retrieval and fertilization outcomes of pronuclear transfer patient, PGT patient and donor eggs.
PNT後の胚の生存可能性は、標準的なART手順と同等でした。PNTとPGT患者の卵子採取と受精率は、一般的に健康な寄与者卵子よりも低く、これは影響を受けた女性の潜在的な不妊問題を反映していると考えられます。しかし、患者と寄与者の正常に受精した卵子の割合の差は有意でした(P<0.001)、これは技術的な課題があることを示しつつも、これらの介入の実現可能性を示しています。
メカニズムの洞察
PNTは、細胞質のミトコンドリアを置き換えつつ、親の核遺伝的同一性を保つことで、mtDNAの母系遺伝を根本的に解決します。このアプローチは、すべての母系mtDNAが変異している(ホモプラズミー)場合や、高レベルのヘテロプラズミーが無病胚の選択を許さない場合のPGTの制限を回避します。子供の変異型ミトコンドリアがほぼ完全に置き換わったことは、この方法の生物学的妥当性と効率性を示しています。
専門家のコメント
ミトコンドリア研究の先駆者であるドグラ・ターナー博士は、「これらの結果は、ミトコンドリア疾患に影響を受けた家族にとっての転換点を示しています。初めて、ホモプラズミック変異を持つ女性が、遺伝的に関連する子供を持ち、疾患リスクが大幅に軽減される現実的な選択肢を得ることができます。」と述べています。
英国ヒューマン・フェルティライゼーション・アンド・エンブリオロジー局は、ミトコンドリア寄与を規制された臨床サービスとして認識しており、その安全性と効果性に対する信頼が高まっています。ただし、これらの技術を通じて生まれた子供の長期追跡が重要であり、その利点とリスクを完全に確立するために必要です。
議論と制限事項
結果は有望ですが、いくつかの制限事項について議論する必要があります。
- コホートの規模はまだ modest であり、子供の健康、発達、不妊能力に関する長期的な結果はまだ利用できません。
- 技術的な複雑さとリソース要件により、広範な普及が制限されています。
- PNT後、一部のケースでは残存する低レベルの母系mtDNAヘテロプラズミーが存在し、遅発性または軽微な疾患表現型の可能性が提起されています。
- 胚系修飾や寄与者匿名性などの倫理的な考慮事項は、医療界と公衆の両方で議論を呼び続けています。
結論
プロヌクレア転移によるミトコンドリア寄与と着床前遺伝子検査は、mtDNA疾患の伝播リスクのある女性に対する生殖医学における重要な進歩を代表しています。ヘテロプラズミー状態に基づいた個別化された統合アプローチは、疾患リスクを個別に軽減し、これらの深刻な状態に影響を受けた家族に希望をもたらします。これらの技術がより広範な臨床導入に向かうにつれて、継続的な監視、プロトコルのさらなる洗練、堅固な倫理的監督が不可欠となります。
参考文献
1. Hyslop LA, Blakely EL, Aushev M, et al. Mitochondrial Donation and Preimplantation Genetic Testing for mtDNA Disease. N Engl J Med. 2025 Jul 31;393(5):438-449. doi: 10.1056/NEJMoa2415539 IF: 78.5 Q1 . Epub 2025 Jul 16. PMID: 40673696 IF: 78.5 Q1 ; PMCID: PMC7617940 IF: 78.5 Q1 .2. Gorman GS, Chinnery PF, DiMauro S, et al. Mitochondrial diseases. Nat Rev Dis Primers. 2016;2:16080. doi:10.1038/nrdp.2016.80 IF: 60.6 Q1 .3. Craven L, Tuppen HA, Greggains GD, et al. Pronuclear transfer in human embryos to prevent transmission of mitochondrial DNA disease. Nature. 2010;465(7294):82-85. doi:10.1038/nature08958 IF: 48.5 Q1 .