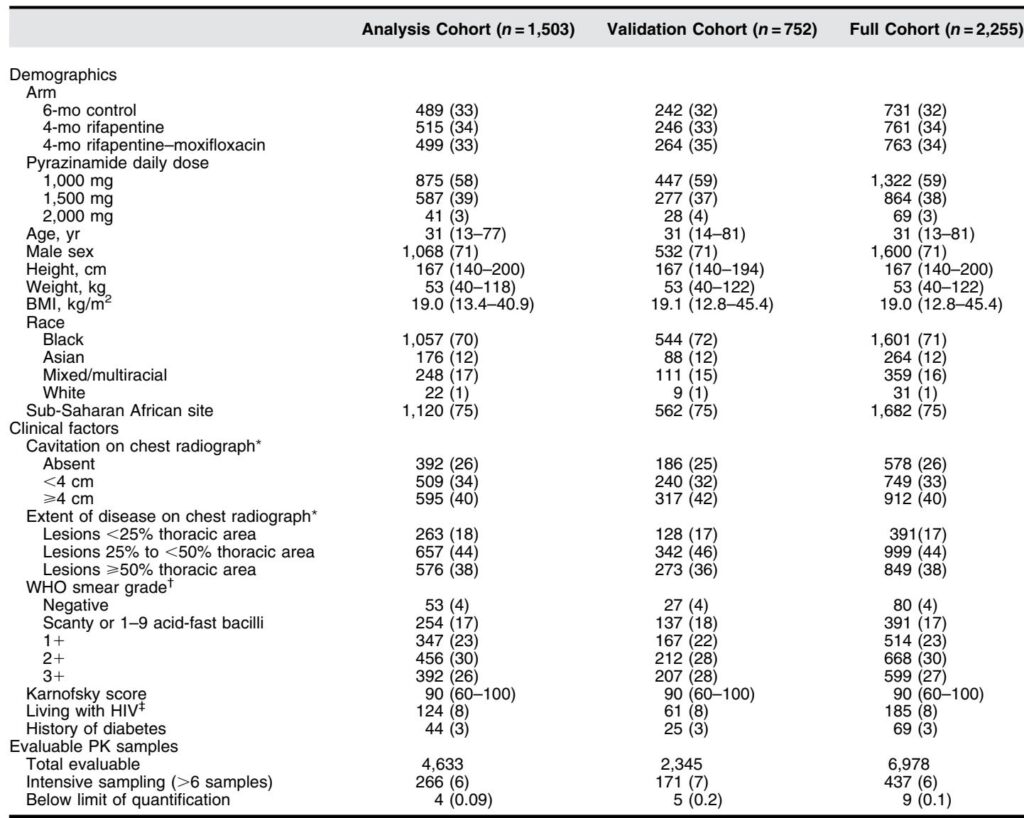
主要な知見
ピラジナミドの薬物動態と変動
ピラジナミドの薬物動態は、一室モデルで最初の一次吸収と排出が最もよく説明され、終末半減期は約6.6時間でした。特に、体重バンド用量を受けている参加者では、ピラジナミドの曝露量(AUC_ss 151~1,053 mg・h/L)に7倍の変動が見られ、薬物の吸収と代謝における個人差が強調されました。
共変量解析では、女性は男性よりも16.3%高い生物利用度を示し、アジア系参加者は黒人または混血の参加者に比べて41.8%低い平均通過時間を示しました。食事摂取も、食事と共に投与される4ヶ月間の治療レジメンでは吸収が著しく遅延しました。これに対して、6ヶ月間の対照群では空腹時に投与されました。また、体重はピラジナミドのクリアランスを予測する臨床的に重要な因子ではなく、現在の体重バンド用量の合理性を揺るがす結果となりました。
1,500 mgおよび2,000 mgの高用量では、1,000 mgの用量に比べて生物利用度が低下し、曝露量が比例以上に増加しないことが示されました。
効果に対する曝露反応関係
6ヶ月間の対照レジメンを受けている参加者では、ピラジナミドのAUC_ssが低い、Xpert MTB/RIFサイクル閾値が低い(バシラリー負荷が高い)、年齢が高いことが、結核に関連した不良な結果のリスク増加と相関していました。ピラジナミドの曝露量は持続的な完治の重要な予測因子であり、最適な効果を発揮するための治療窓は231~355 mg・h/LのAUC_ssで定義されました。
一方、4ヶ月間のリファペンチン含有レジメンでは、リファペンチンの曝露量が効果の主な決定因子でした。これらのレジメン内では、ピラジナミドの曝露量は予測モデルを大幅に強化せず、ピラジナミドの役割はレジメンや伴走薬に依存することが示されました。
安全性に対する曝露反応関係
6ヶ月間の対照群と4ヶ月間のリファペンチン-モキサフロキサシンレジメンでは、ピラジナミドの曝露量が増加すると、グレード3以上のイベント、毒性による治療中止、肝酵素の上昇、Hy’s法に基づく肝毒性のリスクが高まりました。これらの結果から、ピラジナミドのAUC_ssの安全曝露上限は、対照群で355 mg・h/L、リファペンチン-モキサフロキサシンレジメンで349 mg・h/Lと定義されました。
4ヶ月間のリファペンチンレジメンでは、重大な有害事象が少ないため、このグループでの曝露-安全性関係の検出が制限されました。
用量シミュレーションと治療窓の最適化
モンテカルロシミュレーションにより、体重バンド用量と1日に1,000 mgまたは1,500 mgの固定用量を比較しました。1日に1,000 mgの固定用量は、対照レジメンでは13.1%、リファペンチン-モキサフロキサシンレジメンでは9.2%の参加者が治療窓の曝露量を達成する割合が現在の用量ガイドラインと比較して増加しました。
1日に1,500 mgの高固定用量は、安全性閾値を超える曝露量が増加し、1,000 mgの固定用量が効果と安全性のバランスを取ることの利点を強調しました。
討論
この包括的分析は、薬剤感受性肺結核におけるピラジナミドの最大単一試験の薬物動態と曝露-反応評価を代表しています。本研究の知見は、体重バンド用量を支持する従来の考え方を覆し、ピラジナミドのクリアランスは体重に依存せず、用量に関連する生物利用度、性別、人種、食事摂取によって影響を受けることを示しています。
特にリファペンチン含有レジメンでの貢献が減少しているピラジナミドの曝露量が効果に及ぼすレジメン固有の影響を強調し、用量戦略を伴走薬の広い文脈内で解釈する必要性を示しています。
治療用量での曝露-毒性関係、特に肝毒性は依然として重要であり、過剰なピラジナミド曝露を避ける用量戦略の必要性を強調しています。本研究ではピラジナミド関連の毒性と他の薬剤を完全に分離することはできませんでしたが、上昇した肝酵素と重大な有害事象との関連性は、ピラジナミドの安全性プロファイルを強調しています。
実践的な意味合いは、1日に1,000 mgの固定用量への移行であり、これは臨床実践を簡素化し、持続的な完治と許容可能な安全性プロファイルのバランスを取った治療窓に合わせることで、より重い体重の人々での過剰投与リスクを低減し、全体的な治療成果を改善します。
制限点と強み
堅牢なデータを提供する一方で、本研究はいくつかの制限点を認識しています。観察された関連性は因果関係を確立せず、ピラジナミド代謝物の薬物動態はデータの欠如により研究されていません。リファペンチンの曝露量の影響は、短期レジメンでのピラジナミドの効果貢献をマスクしていた可能性があります。最後に、一部のアームでの少数の有害事象は、安全性解析の統計的力が低下しました。
強みには、前例のないサンプルサイズ、堅牢な薬物動態サンプリング、多大陸コホート全体での多様な共変量を組み込んだ包括的なモデリングが含まれており、研究結果の一般化可能性が向上しています。
結論
1日に1,000 mgの固定用量でピラジナミドを投与することは、薬剤感受性肺結核の治療において実現可能で、潜在的に優れた戦略であることが示されました。この用量レジメンは、治療効果と安全性のバランスを最適化し、治療プロトコルを簡素化し、固定用量複合療法の導入を容易にする可能性があります。ピラジナミドの高用量の評価を継続する研究は、進化する結核治療レジメンにおける最適な用量をさらに明確にするでしょう。